摘要:6.A.B.C为三种短周期元素.A.B在同一周期.A.C的最低价离子为A2-和C-.B2+和C-具有相同的电子层结构.下列说法正确的是 A.原子序数:A>B>C B.原子半径:A>B>C C.离子半径:A2->B2+>C- D.原子核外最外层电子数A>C>B
网址:http://m.1010jiajiao.com/timu3_id_176056[举报]
X、Y、Z为三种短周期元素,X+核外电子比Y-核外电子少一个电子层,且X+、Z2-具有与Ne原子相同的核外电子层结构。下列说法不正确的是
[ ]
A.X原子半径大于Y原子半径,Z2-半径大于X+半径
B.X+、Y-、Z2-核外最外层电子数相同
C.X与Y形成的化合物、X与Z形成的化合物的晶体中只存在离子键
D.工业上可以用电解熔融XY的方法得到X、Y元素的单质
查看习题详情和答案>>
B.X+、Y-、Z2-核外最外层电子数相同
C.X与Y形成的化合物、X与Z形成的化合物的晶体中只存在离子键
D.工业上可以用电解熔融XY的方法得到X、Y元素的单质
X、Y、Z是三种短周期元素,它们在周期表中的位置如下图所示。已知Y原子与Z原子核外电子数之和是X的4倍,则下列推断正确的是?

A.Z的原子半径比Y的大? B.X、Y、Z均为非金属元素?
C.X、Y、Z三者核电荷数之和为32? D.X、Y、Z三者可以共同形成一种离子化合物
查看习题详情和答案>>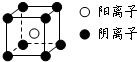 短周期元素A、B、C、D、E、F,原子序数依次增大.已知:①A与E同主族,E的单质与D2反应可生成E2D和E2D2两种固体;②F的单质在D2中燃烧的产物可使品红溶液褪色;B的单质在D2中燃烧可生成BD和BD2两种气体;③CA4++DA-=CA3↑+A2D,各种反应和生成物的电子数都与E+相等.请回答下列问题:
短周期元素A、B、C、D、E、F,原子序数依次增大.已知:①A与E同主族,E的单质与D2反应可生成E2D和E2D2两种固体;②F的单质在D2中燃烧的产物可使品红溶液褪色;B的单质在D2中燃烧可生成BD和BD2两种气体;③CA4++DA-=CA3↑+A2D,各种反应和生成物的电子数都与E+相等.请回答下列问题:(1)BD2的结构式为
O=C=O
O=C=O
,F的离子结构示意图为

三角锥型
三角锥型
.(2)废旧印刷电路板上含有铜,以往回收的方法是将其灼烧使用铜转化为氧化铜,再用稀硫酸来溶解.现改用A2D2和稀硫酸浸泡即达目的,又保护了环境,其反应的化学方程式为
Cu+H2O2+H2SO4=CuSO4+2H2O
Cu+H2O2+H2SO4=CuSO4+2H2O
;(3)在火箭推进器中装有强还原剂C2A4和强氧化剂A2D2,已知0.5mol液态C2A4和足量液态A2D2反应,生成一种无色无味无毒的气体和水蒸气,放出320kJ热量,写出该反应的热化学方程式
N2H4(1)+2H2O2(1)=N2(g)+4H2O(g);△H=-640kJ?mol-1
N2H4(1)+2H2O2(1)=N2(g)+4H2O(g);△H=-640kJ?mol-1
.(4)离子化合物CA5的电子式为


| ||
| 2 |
| 3 |
| ||
| ||
| 2 |
| 3 |
| ||
六种短周期元素aA、bB、cC、dD、eE、fF,已知原子序数大小关系是:a<e<c<b<f<d,且a+b=
;六种元素在周期表中的位置关系是:A、B同主族,C、D也同主族;C、E相邻,B、F也相邻.
(1)E、F形成的化合物甲的电子式为
 ,该化合物与A2C反应的化学方程式:
,该化合物与A2C反应的化学方程式:
(2)写出分别由A、B、C、D四种元素所形成的两种化合物的水溶液相互反应的离子方程式:
(3)已知B+BEC3-B2C+E2,请将方程式配平后用双线桥表示电子的转移情况
 .
.
(4)A、E形成的四原子核化合物丙容易液化,其原因是:
(5)经检测,某固体粉末中仅含有B、C两种元素组成的化合物,请设计实验方案探究该固体粉末的成分
查看习题详情和答案>>
| (c+d) | 2 |
(1)E、F形成的化合物甲的电子式为


Mg3N2+6H2O=3Mg(OH)2+2NH3↑
Mg3N2+6H2O=3Mg(OH)2+2NH3↑
.(2)写出分别由A、B、C、D四种元素所形成的两种化合物的水溶液相互反应的离子方程式:
H++HSO3-=SO2↑+H2O
H++HSO3-=SO2↑+H2O
.(3)已知B+BEC3-B2C+E2,请将方程式配平后用双线桥表示电子的转移情况


(4)A、E形成的四原子核化合物丙容易液化,其原因是:
氨分子之间易形成氢键
氨分子之间易形成氢键
.由A、C、E三种元素形成的离子化合物溶液中,离子浓度由大到小顺序为NO3->NH4+>H+>OH-
NO3->NH4+>H+>OH-
.(5)经检测,某固体粉末中仅含有B、C两种元素组成的化合物,请设计实验方案探究该固体粉末的成分
可能的组成为Na2O2,Na2O或两个都有.将粉末加入水中,若无气体生成,则为Na2O,若有气体生成,可根据一定量该固体粉末产生气体的量确定其全部为Na2O2或是两者的混合物
可能的组成为Na2O2,Na2O或两个都有.将粉末加入水中,若无气体生成,则为Na2O,若有气体生成,可根据一定量该固体粉末产生气体的量确定其全部为Na2O2或是两者的混合物
.四种短周期元素A、B、C、D的性质或结构信息如下.
信息①原子半径大小:A>B>C>D
信息②四种元素之间形成的某三种分子的比例模型及部分性质:

请根据上述信息回答下列问题.
(1)①C元素在周期表中的位置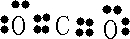
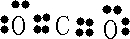 .
.
②A元素的单质与物质甲发生反应的离子方程式
③以Pt为电极,KOH为电解质溶液,两极分别通入乙和C的单质可组成燃料电池,写出电池的电极反应式.负极
(2)A所在周期中,E元素的单质还原性最强,A、E单质反应得到的化合物M是一种重要的化工原料,如图是电解100ml饱和M溶液的装置,X、Y都是惰性电极,实验开始时,同时在两边各滴入几滴酚酞试液,则

①电解池中Y极上的电极反应式
②电解一段时间后,若阴极收集到112ml标准状况下的气体,此时电解液的PH为
查看习题详情和答案>>
信息①原子半径大小:A>B>C>D
信息②四种元素之间形成的某三种分子的比例模型及部分性质:

请根据上述信息回答下列问题.
(1)①C元素在周期表中的位置
第二周期ⅥA族
第二周期ⅥA族
,请写出BC2分子的电子式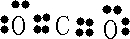
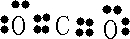
②A元素的单质与物质甲发生反应的离子方程式
Cl2+H2O H++Cl-+HClO
H++Cl-+HClO
 H++Cl-+HClO
H++Cl-+HClOCl2+H2O H++Cl-+HClO
H++Cl-+HClO
. H++Cl-+HClO
H++Cl-+HClO③以Pt为电极,KOH为电解质溶液,两极分别通入乙和C的单质可组成燃料电池,写出电池的电极反应式.负极
CH4-8e-+10OH-=CO32-+7H2O
CH4-8e-+10OH-=CO32-+7H2O
;正极2O2+8e-+4H2O=8OH-
2O2+8e-+4H2O=8OH-
(2)A所在周期中,E元素的单质还原性最强,A、E单质反应得到的化合物M是一种重要的化工原料,如图是电解100ml饱和M溶液的装置,X、Y都是惰性电极,实验开始时,同时在两边各滴入几滴酚酞试液,则

①电解池中Y极上的电极反应式
2Cl-2e-=Cl2↑
2Cl-2e-=Cl2↑
.检验Y电极反应产物的方法是把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色
把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色
.②电解一段时间后,若阴极收集到112ml标准状况下的气体,此时电解液的PH为
13
13
(假设电解液的体积保持不变,常温下)