摘要:①3 FeCl2+4H2O= Fe3O4+6 HCl+ H2↑,②2Fe3O4+3 Cl2+12HCl=6 FeCl3+6H2O+ O2↑,③6 FeCl3=6 FeCl2+3 Cl2↑.某人设想利用以上三个反应的联合与循环来生产能解决环境和能源问题的某种气体.该气体是 A.O2 B.Cl2 C.H2 D.HCl
网址:http://m.1010jiajiao.com/timu3_id_174184[举报]
LiAlH4是金属储氢材料又是有机合成中的常用试剂,遇水能剧烈反应释放出氢气,LiAlH4在125℃分解为LiH、H2和Al.下列叙述错误的是( )
| A、LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂 | B、LiAlH4与D2O反应,所得氢气的摩尔质量为4 g?mol-1 | C、1 mol LiAlH4在125℃完全分解,转移3 mol电子 | D、LiAlH4与水反应生成三种物质时,化学方程式可表示为:LiAlH4+4H2O═Al(OH)3+LiOH+4H2↑ |
下列转化中,不能通过化合反应一步实现的是( )
①SiO2→CaSiO3 ②CuO→Cu(OH)2 ③Fe(OH)2→Fe(OH)3
④FeCl2→FeCl3 ⑤FeCl3→FeCl2⑥CuSO4→CuCl2.
①SiO2→CaSiO3 ②CuO→Cu(OH)2 ③Fe(OH)2→Fe(OH)3
④FeCl2→FeCl3 ⑤FeCl3→FeCl2⑥CuSO4→CuCl2.
查看习题详情和答案>>
下表中,物质Y通过化合反应得到物质W的是( )
| ① | ② | ③ | ④ | |
| Y | Fe(OH)2 | FeCl3 | CO2 | Cu |
| W | Fe(OH)3 | FeCl2 | CO | Cu2(OH)2CO3 |
| A、①② | B、②③ |
| C、①②③ | D、①②③④ |
 金属及其化合物在人类生活、生产中发挥着重要的作用.
金属及其化合物在人类生活、生产中发挥着重要的作用.(1)将一小块金属钠投入盛有水的烧杯中,发生反应的化学方程式为:
2Na+2H2O=2NaOH+H2↑
2Na+2H2O=2NaOH+H2↑
,可观察到的实验现象是
bc
bc
(填序号).a.钠沉到水底 b.钠熔成小球 c.钠球四处游动 d.溶液呈红色
(2)在钠、铝、铁三种金属元素中,其所形成氧化物种类最多的是
铁
铁
,所形成的氧化物中适宜做耐火材料的是
铝
铝
.向盛有硫酸铝溶液的试管中滴加氨水,反应的离子方程式为Al3++3NH3.H2O=Al(OH)3↓+3NH4+
Al3++3NH3.H2O=Al(OH)3↓+3NH4+
,得到的胶状沉淀物因具有吸附性或弱碱
吸附性或弱碱
性,可用于吸附性、净水或治疗胃酸过多
吸附性、净水或治疗胃酸过多
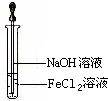
.(3)取少量FeCl2溶液,按如图所示的操作,使其跟NaOH溶液反应.可观察到的现象是
产生白色沉淀,迅速变灰绿,直至红褐色
产生白色沉淀,迅速变灰绿,直至红褐色
,与上述现象相关的反应的化学方程式:FeCl2+2NaOH=Fe(OH)2↓+2NaCl,4Fe(OH)2+O2+2H2O=4Fe(OH)3↓
FeCl2+2NaOH=Fe(OH)2↓+2NaCl,4Fe(OH)2+O2+2H2O=4Fe(OH)3↓
.(4)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
B
B
.A.有铜无铁B.有铁无铜 C.铁、铜都有 D.铁、铜都无.