摘要:3.Na2SiO3的性质:Na2SiO3易溶于水.水溶液俗称“水玻璃 .是建筑行业的黏合剂.也用于木材的防腐和防火. 化学性质主要表现如下: (1)水溶液呈碱性.通CO2有白色沉淀:Na2SiO3 + CO2 + H2O == Na2CO3 + H2SiO3↓.离子方程式:SiO32- + CO2 + H2O == CO32- + H2SiO3↓. 硅酸受热分解:H2SiO3 H2O + SiO2 . 原硅酸和硅酸都是难溶于水的弱酸.酸性:H2CO3强于H4SiO4或H2SiO3. (2)硅酸钠溶液中滴加稀盐酸有白色沉淀: Na2SiO3 + 2HCl == 2NaCl + H2SiO3↓.离子方程式:SiO32- + 2H+ == H2SiO3↓. (3)硅酸和氢氧化钠反应:H2SiO3 + 2NaOH == Na2SiO3 + 2H2O. 离子方程式:H2SiO3 + 2OH- ==SiO32- +2H2O .
网址:http://m.1010jiajiao.com/timu3_id_164280[举报]
(11分)(1)现有A、B、C、D、E五种原子序数递增的主族元素,A的原子核中没有中子;B、D元素处于同一周期,D的原子半径较小,B、D的质子数之和为27,质子数之差为5;C的单质跟盐酸反应,生成C3+和氢气;E和D能形成E2D型离子化合物,且E、D两元素的简单离子具有相同电子层结构。
① 写出元素符号:A ,D ,E 。
② B、C的最高价氧化物对应水化物相互反应的离子方程式为:
。
③ 写出A2D的电离方程式: , 。
(2)元素在周期表中的位置,反映了元素的原子结构和元素的性质。N P AS ;O S Se 分别是VA族、VIA族连续三元素。
①根据元素周期律,预测:酸性强弱 H3AsO4 H3PO4。(用“>”或“<”表示)
② 元素S的最高正价和最低负价的代数和为____________,在一定条件下,S与H2反应有一定限度,请判断:在相同条件下Se与H2反应的限度比S与H2反应限度 。(选填“更大”、“更小”或“相同”)
③将SO2气体通入溴水恰好完全反应后,溶液中存在的离子浓度由大到小的顺序是_________________。
查看习题详情和答案>>
(2008?广东)某些高分子催化剂可用于有机合成.下面是一种高分子催化剂(Ⅶ)合成路线的一部分(Ⅲ和Ⅵ都是Ⅶ的单体;反应均在一定条件下进行;化合物Ⅰ-Ⅲ和Ⅶ中含N杂环的性质类似于苯环):

回答下列问题:
(1)写出由化合物Ⅰ合成化合物Ⅱ的反应方程式
 (不要求标出反应条件).
(不要求标出反应条件).
(2)下列关于化合物Ⅰ、Ⅱ和Ⅲ的说法中,正确的是
A.化合物Ⅰ可以发生氧化反应
B.化合物Ⅰ与金属钠反应不生成氢气
C.化合物Ⅱ可以发生水解反应
D.化合物Ⅲ不可以使溴的四氯化碳深液褪色
E.化合物Ⅲ属于烯烃类化合物
(3)化合物Ⅵ是
A.醇B.烷烃C.烯烃D.酸E.酯
(4)写出2种可鉴别V和Ⅵ的化学试剂
(5)在上述合成路线中,化合物Ⅳ和V在催化剂的作用下与氧气反应生成Ⅵ和水,写出反应方程式
 (不要求标出反应条件)
(不要求标出反应条件)
查看习题详情和答案>>

回答下列问题:
(1)写出由化合物Ⅰ合成化合物Ⅱ的反应方程式


(2)下列关于化合物Ⅰ、Ⅱ和Ⅲ的说法中,正确的是
AC
AC
(填字母).A.化合物Ⅰ可以发生氧化反应
B.化合物Ⅰ与金属钠反应不生成氢气
C.化合物Ⅱ可以发生水解反应
D.化合物Ⅲ不可以使溴的四氯化碳深液褪色
E.化合物Ⅲ属于烯烃类化合物
(3)化合物Ⅵ是
E
E
(填字母)类化合物.A.醇B.烷烃C.烯烃D.酸E.酯
(4)写出2种可鉴别V和Ⅵ的化学试剂
酸性高锰酸钾溶液、饱和碳酸钠溶液
酸性高锰酸钾溶液、饱和碳酸钠溶液
(5)在上述合成路线中,化合物Ⅳ和V在催化剂的作用下与氧气反应生成Ⅵ和水,写出反应方程式


(2013?临沂一模)二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义.
(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2:4FeS2+11O2
8SO2+2Fe2O3,该反应中被氧化的元素是
(2)实验室中用如图1所示的装置测定SO2催化氧化为SO3,的转化率.(已知SO3熔点为16.8℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响.)
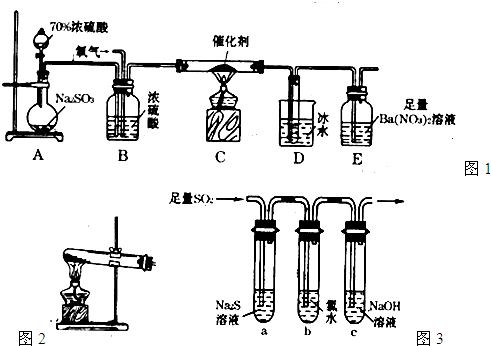
①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是
②实验过程中,需要通入氧气.试写出一个用图2所示装置制取氧气的化学方程式
③当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是
④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是
×100%
×100%(用含字母的代数式表示,不用化简).
(3)某学习小组设计用如图3装置验证二氧化硫的化学性质.
①能说明二氧化硫具有氧化性的实验现象为
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是
③当通入二氧化硫至试管c中溶液显中性时,该溶液中c(Na+)=
查看习题详情和答案>>
(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2:4FeS2+11O2
| ||
Fe、S
Fe、S
(填元素符号).当该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为11.2
11.2
L.(2)实验室中用如图1所示的装置测定SO2催化氧化为SO3,的转化率.(已知SO3熔点为16.8℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响.)

①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是
打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,慢慢滴加
打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,慢慢滴加
.②实验过程中,需要通入氧气.试写出一个用图2所示装置制取氧气的化学方程式
2KClO3
2KCl+3O2↑
| ||
| △ |
2KClO3
2KCl+3O2↑
.
| ||
| △ |
③当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是
使残留在装置中的二氧化硫和三氧化硫被充分吸收
使残留在装置中的二氧化硫和三氧化硫被充分吸收
.④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是
| ||||
|
| ||||
|
(3)某学习小组设计用如图3装置验证二氧化硫的化学性质.
①能说明二氧化硫具有氧化性的实验现象为
试管a中出现淡黄色浑浊
试管a中出现淡黄色浑浊
.②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是
Ⅲ
Ⅲ
(填“I”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为SO2+Cl2+2H2O=4H++SO42-+2Cl-
SO2+Cl2+2H2O=4H++SO42-+2Cl-
.③当通入二氧化硫至试管c中溶液显中性时,该溶液中c(Na+)=
2c(SO32-)+c(HSO3-)
2c(SO32-)+c(HSO3-)
(用含硫微粒浓度的代数式表示).两组同学对铁及其化合物的性质进行探究.
(1)一组同学用图1所示装置对铁与浓硫酸的反应进行实验.已知:
2Fe+6H2SO4(浓)
Fe2(SO4)3+3SO2↑+6H2O.请你参与探究并回答相关问题.
①检查装置气密性后,将过量的铁屑和一定量的浓硫酸放入烧瓶,塞紧橡皮塞,开始计时.t1时开始加热,在铁屑表面逐渐产生气泡,当有大量气泡产生时,控制反应温度基本不变.甲同学将收集到的气体体积与时间的关系粗略地表示为图2.
在0~t1时间段,铁屑表面没有气泡生成,说明铁在浓硫酸中发生了
②t2时,取少量反应液,先滴加少量新制饱和氯水,然后滴加KSCN溶液,呈现血红色.若再滴加过量新制氯水,却发现红色褪去.同学们对红色褪去的原因提出各自的假设.乙同学的假设是:溶液中的+3价铁被氧化为更高的价态.你的另一种假设是
(2)另一组同学对铁和稀硝酸的反应进行探究.他们用a mol Fe和含有b mol HNO3的稀硝酸进行实验,若HNO3只被还原成NO,且反应结束后溶液中含有Fe3+和Fe2+,则
的取值范围是
<
<
<
<
;若反应结束后的溶液中n(Fe3+):n(Fe2+)=2:1,则
的值为
.

查看习题详情和答案>>
(1)一组同学用图1所示装置对铁与浓硫酸的反应进行实验.已知:
2Fe+6H2SO4(浓)
| ||
①检查装置气密性后,将过量的铁屑和一定量的浓硫酸放入烧瓶,塞紧橡皮塞,开始计时.t1时开始加热,在铁屑表面逐渐产生气泡,当有大量气泡产生时,控制反应温度基本不变.甲同学将收集到的气体体积与时间的关系粗略地表示为图2.
在0~t1时间段,铁屑表面没有气泡生成,说明铁在浓硫酸中发生了
钝化
钝化
;t1~t2时间段,反应生成的气体是SO2
SO2
.②t2时,取少量反应液,先滴加少量新制饱和氯水,然后滴加KSCN溶液,呈现血红色.若再滴加过量新制氯水,却发现红色褪去.同学们对红色褪去的原因提出各自的假设.乙同学的假设是:溶液中的+3价铁被氧化为更高的价态.你的另一种假设是
溶液中的SCN-被氧化;
溶液中的SCN-被氧化;
;为了验证你的假设,请设计一种简便的实验方案向褪色后的溶液中加入FeCl3溶液,若不恢复红色,则我的假设成立(或:向褪色后的溶液中加入KSCN溶液,若恢复红色,则我的假设成立)
向褪色后的溶液中加入FeCl3溶液,若不恢复红色,则我的假设成立(或:向褪色后的溶液中加入KSCN溶液,若恢复红色,则我的假设成立)
.(2)另一组同学对铁和稀硝酸的反应进行探究.他们用a mol Fe和含有b mol HNO3的稀硝酸进行实验,若HNO3只被还原成NO,且反应结束后溶液中含有Fe3+和Fe2+,则
| a |
| b |
| 1 |
| 4 |
| a |
| b |
| 3 |
| 8 |
| 1 |
| 4 |
| a |
| b |
| 3 |
| 8 |
| a |
| b |
| 9 |
| 32 |
| 9 |
| 32 |
