摘要:①溶解:Al2O3+2NaOH === 2NaAlO2+H2O ②过滤:除去杂质 ③酸化:NaAlO2+CO2+2H2O === Al(OH)3↓+NaHCO3 通电 ④过滤:保留氢氧化铝 ⑤灼烧:2Al(OH)3 ======= 4Al+3O2↑ 铝合金特点:1.密度小2.强度高3.塑性好4.制造工艺简单5.成本低6.抗腐蚀力强
网址:http://m.1010jiajiao.com/timu3_id_164272[举报]
某地有丰富的铝土矿和石灰石资源,拟用铝土矿(主要成分是Al2O3,还有少量的Fe2O3、SiO2)为原料冶炼铝,工艺流程如图2所示:

(1)原料A的名称是 ,可循环使用的物质的化学式为
(2)如果省去步骤①,即溶解铝土矿从直接加入B溶液开始,则最终会对氧化铝的生产产生的影响是
(3)写步骤③的离子方程式
(4)步骤⑤是在铝电解槽中进行,电解槽的两极材料均用石墨,写出阴极的电极反应方程式
(5)工业常用阳极氧化法使铝的表面生成致密的氧化膜.如图1是铝阳极氧化实验装置图:a端是电源的 极.铝片表面形成氧化铝的原理是(用电极方程式表示) , (填“能”或“不能”)用NaCl溶液代替20%H2SO4作电解液进行铝的阳极氧化,若不能,请说明理由 .
查看习题详情和答案>>

(1)原料A的名称是
(2)如果省去步骤①,即溶解铝土矿从直接加入B溶液开始,则最终会对氧化铝的生产产生的影响是
(3)写步骤③的离子方程式
(4)步骤⑤是在铝电解槽中进行,电解槽的两极材料均用石墨,写出阴极的电极反应方程式
(5)工业常用阳极氧化法使铝的表面生成致密的氧化膜.如图1是铝阳极氧化实验装置图:a端是电源的
 (1)环境专家认为可以用铝将水中的NO3- 转化为N2,从而清除污染.该反应中涉及的粒子有:H2O、Al、OH-、Al(OH)3、NO3-、N2,请将各粒子分别填入以下空格(请将整个方程式配平后写在答题纸上).
(1)环境专家认为可以用铝将水中的NO3- 转化为N2,从而清除污染.该反应中涉及的粒子有:H2O、Al、OH-、Al(OH)3、NO3-、N2,请将各粒子分别填入以下空格(请将整个方程式配平后写在答题纸上).NO3-+
10Al
10Al
+18H2O
18H2O
→10Al(OH)3
10Al(OH)3
+3N2
3N2
+6OH-
6OH-
该反应过程中,被氧化与被还原的元素的物质的量之比为5:3
5:3
.(2)若4Al(s)+3O2(g)=2Al2O3(s)△H=-a KJ/mol
Fe2O3(s)+
| 3 |
| 2 |
| 3 |
| 2 |
C(s)+O2(g)=CO2(g)△H=-c KJ/mol
写出Al与氧化铁发生铝热反应的热化学方程式:
2Al(s)+Fe2O3(s)=2Fe(s)+Al2O3(s)△H=-(
a-b-
c)KJ/mol
| 1 |
| 2 |
| 3 |
| 2 |
2Al(s)+Fe2O3(s)=2Fe(s)+Al2O3(s)△H=-(
a-b-
c)KJ/mol
.| 1 |
| 2 |
| 3 |
| 2 |
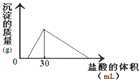
(3)将一定质量的钠铝合金置于水中,合金全部溶解,得到20mL PH=14的溶液,然后用2mol/L的盐酸滴定,可得到沉淀量与消耗的盐酸体积关系如图:则反应过程中产生氢气的总体积为
2.016
2.016
L(标准状况).(2010?潮州二模)重铬酸钠(Na2Cr2O7)广泛用于合成颜料、媒染剂等,以铬铁矿(主要成分为Cr2O3,还有FeO、Al2O3、SiO2等杂质)为原料制取重铬酸钠的流程图如下:
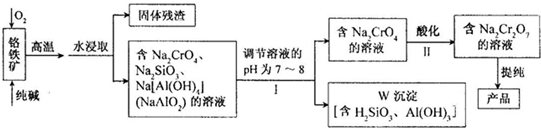
请回答下列问题.
(1)铬铁矿中的Cr2O3与纯碱、O2在高温下反应的化学方程式为
(2)若Ⅰ中只用一种试剂调节溶液的pH,应选用
A.稀硫酸 B.氧化钠固体 C.氢氧化钾溶液
(3)Ⅰ中,调节溶液pH后,如果溶液的pH过小,可能导致W沉淀部分溶解,原因是:
3中,Na2CrO4转化为Na2Cr2O7的离子反应如下:
2CrO42-(黄色)+2H+?Cr2O72-(橙红色)+H2O
①该反应
②若往Na2Cr2O7溶液(橙红色)中加入足量NaOH固体,溶液
A.变黄色B.颜色不变C.橙红色变深
③已知:25℃,Ag2CrO4的Ksp=1.12×10-12,Ag2Cr2O7的Ksp=2×10-7.25℃,往Na2Cr2O7溶液中加入AgNO3溶液,最终只生成一种砖红色沉淀,该沉淀的化学式是
查看习题详情和答案>>

请回答下列问题.
(1)铬铁矿中的Cr2O3与纯碱、O2在高温下反应的化学方程式为
2Cr2O3+4Na2CO3+3O2
4Na2CrO4+4 CO2
| ||
2Cr2O3+4Na2CO3+3O2
4Na2CrO4+4 CO2
.
| ||
(2)若Ⅰ中只用一种试剂调节溶液的pH,应选用
A
A
(填标号).A.稀硫酸 B.氧化钠固体 C.氢氧化钾溶液
(3)Ⅰ中,调节溶液pH后,如果溶液的pH过小,可能导致W沉淀部分溶解,原因是:
Al(OH)3+3H+═Al3++3H2O
Al(OH)3+3H+═Al3++3H2O
.(用离子方程式表示).3中,Na2CrO4转化为Na2Cr2O7的离子反应如下:
2CrO42-(黄色)+2H+?Cr2O72-(橙红色)+H2O
①该反应
不是
不是
(填“是”或“不是”)氧化还原反应.②若往Na2Cr2O7溶液(橙红色)中加入足量NaOH固体,溶液
A
A
(填标号).A.变黄色B.颜色不变C.橙红色变深
③已知:25℃,Ag2CrO4的Ksp=1.12×10-12,Ag2Cr2O7的Ksp=2×10-7.25℃,往Na2Cr2O7溶液中加入AgNO3溶液,最终只生成一种砖红色沉淀,该沉淀的化学式是
Ag2CrO4
Ag2CrO4
.(2013?江门一模)化工原料红矾钠(重铬酸钠:Na2Cr207-2H20)主要是以铬铁矿(主要成份为FeO-Cr2O3,还含有A1203,Si02等杂质)为主要原料生产,其主要工艺流程如图1:
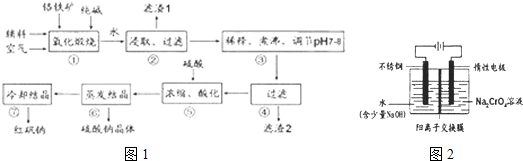
步骤①中主要反应的化学方程式为:Fe0?Cr2O3+8Na2C03+702=8Na2Cr04+2Fe2O3+8C02
(I)①中反应是在回转窑中进行,反应时需不断搅拌,其作用是
(2)杂质A1203,SiO2在①中转化的化学反应方程式为
(3)用化学平衡移动原理说明③中煮沸的作用是
(4)⑤中酸化是使Cr042一转化为Cr2072一,写出该反应的离子方程式:
(5)工业上还可用电解法制备重铬酸钠,其装置示意图如图2:
阴极发生的电极反应式为:
阳极发生的电极反应式为:
查看习题详情和答案>>

步骤①中主要反应的化学方程式为:Fe0?Cr2O3+8Na2C03+702=8Na2Cr04+2Fe2O3+8C02
(I)①中反应是在回转窑中进行,反应时需不断搅拌,其作用是
增大反应物的接触面积,加快反应速率
增大反应物的接触面积,加快反应速率
.(2)杂质A1203,SiO2在①中转化的化学反应方程式为
Al2O3+Na2CO3
2NaAlO2+CO2↑;SiO2+Na2CO3
Na2SiO3+CO2↑
| ||
| ||
Al2O3+Na2CO3
2NaAlO2+CO2↑;SiO2+Na2CO3
Na2SiO3+CO2↑
| ||
| ||
(3)用化学平衡移动原理说明③中煮沸的作用是
水解吸热,煮沸促进AlO2-+2H2O?Al(OH)3+OH-,SiO32-+H2O?HSiO3-+OH-水解平衡向右移动,生成氢氧化铝、硅酸沉淀
水解吸热,煮沸促进AlO2-+2H2O?Al(OH)3+OH-,SiO32-+H2O?HSiO3-+OH-水解平衡向右移动,生成氢氧化铝、硅酸沉淀
(用离子方程式结合文字说明),若调节pH过低产生的影响是H+将水解生成的氢氧化铝沉淀溶解,杂质Al3+难与Na2CrO4分离
H+将水解生成的氢氧化铝沉淀溶解,杂质Al3+难与Na2CrO4分离
(4)⑤中酸化是使Cr042一转化为Cr2072一,写出该反应的离子方程式:
2CrO42-+2H+ Cr2O72-+H2O
Cr2O72-+H2O
 Cr2O72-+H2O
Cr2O72-+H2O2CrO42-+2H+ Cr2O72-+H2O
Cr2O72-+H2O
 Cr2O72-+H2O
Cr2O72-+H2O(5)工业上还可用电解法制备重铬酸钠,其装置示意图如图2:
阴极发生的电极反应式为:
阴极:4H2O+4e-═4OH-+2H2↑或2H2O+2e-═2OH-+H2↑
或4H++4e═2H2↑或2H++2e═H2↑
或4H++4e═2H2↑或2H++2e═H2↑
阴极:4H2O+4e-═4OH-+2H2↑或2H2O+2e-═2OH-+H2↑
或4H++4e═2H2↑或2H++2e═H2↑
或4H++4e═2H2↑或2H++2e═H2↑
阳极发生的电极反应式为:
阳极:2H2O-4e-═O2↑+4H+或4OH--4e-═O2↑+2H2O
阳极:2H2O-4e-═O2↑+4H+或4OH--4e-═O2↑+2H2O
.(2010?丰台区一模)(1)环境专家认为可以用金属铝将水体中的NO3-转化为N2,从而清除污染.该反应中涉及的粒子有:H2O、Al、OH-、Al(OH)3、NO3-、N2,请将各粒子分别填入以下空格内(不用配平).该反应过程中,被氧化与被还原的元素的物质的量之比为
(2)我国首创的海洋电池以海水为电解质溶液,电池总反应为:4Al+3O2+6H2O=4Al(OH)3.电池正极的电极反应式为
(3)已知:4Al(s)+3O2(g)=2Al2O3(g)△H=-2834.9kJ/mol
Fe2O3(s)+
C(s)=
CO2(g)+2Fe(s)△H=234.1kJ/mol
C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol
写出铝与氧化铁发生铝热反应的热化学方程式
(4)将一定质量的钠铝合金置于水中,合金全部溶解,得到20mol,pH=14的溶液,然后2mol/L盐酸滴定,可得沉淀质量与消耗的盐酸体积关系如下图:则反应过程中产生氢气的总体积为

查看习题详情和答案>>
5:3
5:3
.(2)我国首创的海洋电池以海水为电解质溶液,电池总反应为:4Al+3O2+6H2O=4Al(OH)3.电池正极的电极反应式为
2H2O+O2+4e-=4OH-
2H2O+O2+4e-=4OH-
;正极材料采用了铂网,利用铂网为正极的优点是铂性质稳定不与氧气反应,网状结构可以增大与氧气的接触面积
铂性质稳定不与氧气反应,网状结构可以增大与氧气的接触面积
.(3)已知:4Al(s)+3O2(g)=2Al2O3(g)△H=-2834.9kJ/mol
Fe2O3(s)+
| 3 |
| 2 |
| 3 |
| 2 |
C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol
写出铝与氧化铁发生铝热反应的热化学方程式
2Al(s)+Fe2O3(s)=2Fe(s)=2Fe(s)+Al2O3(s)△H=-593.1kJ/mol
2Al(s)+Fe2O3(s)=2Fe(s)=2Fe(s)+Al2O3(s)△H=-593.1kJ/mol
.(4)将一定质量的钠铝合金置于水中,合金全部溶解,得到20mol,pH=14的溶液,然后2mol/L盐酸滴定,可得沉淀质量与消耗的盐酸体积关系如下图:则反应过程中产生氢气的总体积为
2.016
2.016
L(标准状况).