网址:http://m.1010jiajiao.com/timu3_id_162027[举报]
(17分)Ⅰ:现有如下物质:①酒精、②铜、③氢氧化钡、④氨气、⑤蔗糖、 ⑥高氯酸、⑦碳酸氢钠、⑧磷酸、⑨硫化氢、⑩Al2(SO4)3。请用物质的序号填写下列空白
(1)属于强电解质的有: 。
(2)液态时能导电且为物理变化的有: 。
(3)⑦在水溶液的电离方程式为 。
Ⅱ:A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
(1)若A是淡黄色固体,C、D是氧化物,且C是造成酸雨的主要物质。处理C物质可得到有价值的化学品,写出该化学品中的1种酸和1种盐的名称 、 。
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气主要成分,写出该反应的化学方程式 。
(3)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。判断单质A的元素在周期表中的位置是___ _____。写④反应离子方程 。
(4)若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种非金属单质。C的溶液用于蚀刻印刷铜电路板,写该反应的离子方程式 。
某化学课外兴趣小组为探究铜与浓硫酸的反应,用下图所示的装置进行实验:
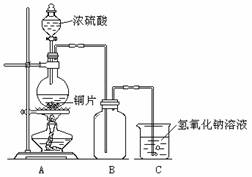
请回答下列问题:
(1)实验中他们取6.4g铜片和12mL18mol?L-1浓硫酸放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余,该小组中的同学认为还有一定量的硫酸剩余。
①下列试剂中,能证明反应停止后烧瓶中有硫酸剩余的是_______(填写字母编号)。
A.硫酸钠溶液 B.氯化钡溶液 C.银粉 D.碳酸钠溶液
②实验中若有m g铜参加了反应,则有______mol硫酸被还原。
(2)为了测定剩余硫酸的物质的量浓度,该兴趣小组设计了三个实验方案:
方案1:将装置A产生的气体缓缓通过已称量过的装有碱石灰的干燥管,反应停止后再次称量,两次质量差即是吸收的二氧化硫。
方案2:将装置A产生的气体缓缓通入足量的用硫酸酸化的高锰酸钾溶液,再加入足量的氯化钡溶液,过滤、洗涤、干燥,称得沉淀的质量即是二氧化硫转化为硫酸钡沉淀的质量。
方案3:当铜和浓硫酸的反应结束后,在装置A中加入足量的锌粉,用排水法测得产生氢气的体积为V L(已换算为标准状况)。
实际上,以上方案1、2均不可取,请你说出原因?
方案1: 。方案2: 。
方案3:写出剩余硫酸的物质的量浓度的计算式(假设反应后溶液的体积仍为12mL) ___________________ _。
查看习题详情和答案>>某化学课外兴趣小组为探究铜与浓硫酸的反应,用下图所示的装置进行实验:

请回答下列问题:
(1)B是用来收集实验中产生气体的装置,但未将导管画全,请将装置图补充完整。
(2)实验中他们取6.4g铜片和12mL18mol·L-1浓硫酸放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余,该小组中的同学认为还有一定量的硫酸剩余。
①写出铜与浓硫酸反应的化学方程式:
______________________________________________________________________,
实验中若有m g铜参加了反应,则有___________mol硫酸被氧化,电子转移数目为_______mol。
②下列试剂中,能证明反应停止后烧瓶中有硫酸剩余的是__________(填写字母编号)。
A.硫酸钠溶液 B.氯化钡溶液 C.银粉 D.碳酸钠溶液
③为什么有一定量的硫酸剩余但未能使铜片完全溶解?你认为的原因是
_________________________________________________________________ _。(3)为了测定剩余硫酸的物质的量浓度,该兴趣小组设计了三个实验方案:
方案一:将装置A产生的气体缓缓通过已称量过的装有碱石灰的干燥管,反应停止后再次称量,两次质量差即是吸收的二氧化硫。
方案二:将装置A产生的气体缓缓通入足量的用硫酸酸化的高锰酸钾溶液,再加入足量的氯化钡溶液,过滤、洗涤、干燥,称得沉淀的质量即是二氧化硫转化为硫酸钡沉淀的质量。
方案三:当铜和浓硫酸的反应结束后,在装置A中加入足量的锌粉,用排水法测得产生氢气的体积为V L(已换算为标准状况)。
实际上,以上方案一、二均不可取,请你说出原因?
方案一 ;
方案二 。
方案三:写出剩余硫酸的物质的量浓度的计算式(假设反应后溶液的体积仍为12mL) _________________________ _。
查看习题详情和答案>>A.氯化铵与氢氧化钠两种浓溶液混合加热OH-+NH4+
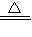 H2O+NH3↑
H2O+NH3↑B.碳酸氢钠溶液与少量石灰水反应 HCO3-+Ca2++OH-═CaCO3↓+H2O
C.氢氧化镁与稀硫酸反应 H++OH-═H2O
D.单质铜与稀硝酸反应 Cu+2H++2NO3-═Cu2++2NO↑+H2O
查看习题详情和答案>>
(1)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡,再平行插入一块铜片,可观察到铜片上____________(填“有”或“没有”)气泡产生.再用导线把锌片和铜片连接起来(见图A),组成一个原电池,负极为___________,正极的电极反应式为___________.
(2)如果烧杯中最初装入的是2mol/L500mL的稀硫酸溶液,构成铜锌原电池(见图B,假设产生的气体没有损失),当在标准状况下收集到11.2L的氢气时,则此时烧杯内溶液中溶质的物质的量浓度应为(溶液体积变化忽略不计)___________.
(3)金属的腐蚀分为两种:化学腐蚀(与化学物质直接接触而发生化学反应)和电化学腐蚀(由于构成原电池而发生电极反应),电化学腐蚀中又分为吸氧腐蚀和析氢腐蚀.如果电极材料分别是铁片和石墨并进行连接,插入氯化钠溶液中(见图C),放置数天后,主要发生___________电化学腐蚀,写出正极的电极反应式一.

(4)生活中利用原电池原理生产了各种各样的电池,废电池必须进行集中处理的问题已被提到议事日程,其最主要原因是___________.
(A)回收利用电池外壳的金属
(B)防止电池中汞、镉和铅等重金属离子对土壤、水源的污染
(C)防止电池中渗泄的电解液腐蚀其他物品
(D)回收其中的石墨电极
查看习题详情和答案>>