摘要:重铬酸钾[(NH4)2Cr2O7]是一种受热易分解的盐.下列各组对重铬酸钾受热分解产物判断符合实际的是 A.CrO3+NH3+O2 B.Cr2O3+NH3+H2O C.Cr2O3+N2+H2O D.CrO3+N2+H2O
网址:http://m.1010jiajiao.com/timu3_id_161369[举报]
工业上用铬铁矿(主要成分FeO?Cr2O3,杂质为SiO2、Al2O3等)生产重铬酸钾(化学式K2Cr2O,)的流程如下:

(1)固体A中,除Na2CrO4、NaFeO2、NaOH外还有
(2)固体A水浸时,NaFeO2会发生强烈水解产生固体B,其化学反应方程式为
(3)固体C中含有2种物质,要先加入下列物质中的
A.氢氧化钠溶液 B.稀氨水 C.稀盐酸
(4)步骤④加入盐酸得到的溶液F中,除Na2Cr2O7外,还含有的溶质是
(5)在上述流程中,有氧化还原反应发生的是第
(6)已知20℃时K2Cr2O7饱和溶液浓度为0.4mol?L-1,步骤⑤中加入固体氯化钾,若使K+离子浓度达到4mol?L-1(保持温度20℃),则溶液F中Cr2O2-7离子的浓度最大为
查看习题详情和答案>>

(1)固体A中,除Na2CrO4、NaFeO2、NaOH外还有
Na2SiO3、NaAlO2
Na2SiO3、NaAlO2
等;(2)固体A水浸时,NaFeO2会发生强烈水解产生固体B,其化学反应方程式为
NaFeO2+2H2O=NaOH+Fe(OH)3
NaFeO2+2H2O=NaOH+Fe(OH)3
;(3)固体C中含有2种物质,要先加入下列物质中的
C
C
,然后才能进行过滤分离.A.氢氧化钠溶液 B.稀氨水 C.稀盐酸
(4)步骤④加入盐酸得到的溶液F中,除Na2Cr2O7外,还含有的溶质是
NaCl
NaCl
;(5)在上述流程中,有氧化还原反应发生的是第
①
①
步.(6)已知20℃时K2Cr2O7饱和溶液浓度为0.4mol?L-1,步骤⑤中加入固体氯化钾,若使K+离子浓度达到4mol?L-1(保持温度20℃),则溶液F中Cr2O2-7离子的浓度最大为
0.016mol/L
0.016mol/L
.(2011?西城区一模)铬铁矿的主要成分可表示为FeO?Cr2O3,还含有SiO2、Al2O3等杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的过程如下图所示.
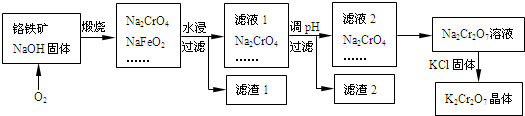
已知:①NaFeO2遇水强烈水解.②Cr2O72-+H2O 2CrO42-+2H+
2CrO42-+2H+
请回答:
(1)K2Cr2O7中Cr元素的化合价是
(2)生成滤渣1中红褐色物质的反应的化学方程式是
(3)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式是
(4)由滤液2转化为Na2Cr2O7溶液应采取的措施是
(5)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、
(6)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是
查看习题详情和答案>>

已知:①NaFeO2遇水强烈水解.②Cr2O72-+H2O
 2CrO42-+2H+
2CrO42-+2H+请回答:
(1)K2Cr2O7中Cr元素的化合价是
+6
+6
.(2)生成滤渣1中红褐色物质的反应的化学方程式是
NaFeO2+2H2O=NaOH+Fe(OH)3↓
NaFeO2+2H2O=NaOH+Fe(OH)3↓
.滤液1的成分除Na2CrO4外,还含有(填化学式)NaAlO2、Na2SiO3和NaOH
NaAlO2、Na2SiO3和NaOH
.(3)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式是
2Al2O3(熔融)
4Al+3O2↑
| ||
2Al2O3(熔融)
4Al+3O2↑
.
| ||
(4)由滤液2转化为Na2Cr2O7溶液应采取的措施是
加硫酸酸化
加硫酸酸化
.(5)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、
冷却结晶
冷却结晶
、过滤、洗涤、干燥.(6)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是
4FeO?Cr2O3+7O2+20NaOH
8Na2CrO4+4NaFeO2+10H2O
| ||
4FeO?Cr2O3+7O2+20NaOH
8Na2CrO4+4NaFeO2+10H2O
.
| ||
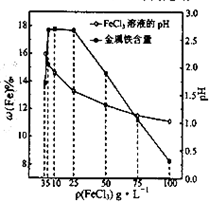 用氯化铁浸出重铬酸钾(K2Cr2O7)滴定法测定钛精粉试样中单质铁的质量分数[ω(Fe)%],实验步骤如下:
用氯化铁浸出重铬酸钾(K2Cr2O7)滴定法测定钛精粉试样中单质铁的质量分数[ω(Fe)%],实验步骤如下:步骤1:称取试样0.100g于250mL洗净的锥形瓶中.
步骤2:加入FeCl3溶液100mL,迅速塞上胶塞,用电磁搅拌器30min.
步骤3:过滤,用水洗涤锥形瓶和滤渣各3~4次,洗液全部并入滤液中.
步骤4:将滤液稀释至500mL,再移去100mL稀释液于锥形瓶中,加入20mL硫酸和磷酸的混合酸,加0.5%二苯胺磺酸钠指示剂4滴.
步骤5:以K2Cr2O7标准溶液滴定至出现明显紫色为终点.发生的反应为:Cr2O72-+6Fe2++14H+=2Cr3++Fe3++7H2O.
步骤6:重复测定两次.
步骤7:数据处理.
(1)步骤2中加入FeCl3溶液后锥形瓶中发生反应的离子方程式为
(2)步骤3中判断滤纸上残渣已洗净的方法是
(3)实验中需用到100mL浓度为0.01mol?L-1K2Cr2O7标准溶液,配置时用到的玻璃仪器有
(4)科研人员确定FeCl3溶液的最佳浓度,选用100mL不同浓度的FeCl3溶液(FeCl3溶液均过量)溶解同一钛精粉试样,其余条件控制相同,得到测定结果如图所示.则FeCl3溶液的浓度[用ρ(FeCl3)表示]范围应为
生活中常用某些化学知识解决实际问题,下列解释正确的是( )
| 选项 | 实际问题 | 解释 |
| A | 用食醋去除暖瓶内的水垢 | 因醋酸能与水垢反应生成可溶性物质 |
| B | 用酒精除去衣服上圆珠笔油油渍 | 因酒精能与圆珠笔油渍反应而水却不能 |
| C | 青、熟水果混合使青水果易熟化 | 因青水果具有吸收乙烯的能力 |
| D | 用酸性重铬酸钾溶液检查酒后驾车 | 因乙醇能将黄色重铬酸钾溶液还原为绿色 |
| A、A | B、B | C、C | D、D |
(2009?梅州模拟)重铬酸钾是工业生产和实验室的重要氧化剂,工业上常用铬铁矿(主要成份为FeO?Cr2O3,杂质主要是二氧化硅和氧化铝)为原料生产,实验室模拟工业法用铬铁矿制K2Cr2O7的主要工艺如下,涉及的主要反应是:
6FeO?Cr2O3+24NaOH+7KClO3
12Na2CrO4+3Fe2O3+7KCl+12H2O

试回答下列问题
(1)指出24Cr在周期表中的位置是
(2)NaFeO2能强烈水解,在操作②生成沉淀而除去,写出该反应的化学方程式:
(3)操作③调节pH=7~8的原因是
下表是铬酸(H2CrO4)溶液中离子的组成与pH的关系:
(4)操作④酸化的目的是
(5)在铬酸(H2CrO4)溶液中,电离出CrO42-的电离平衡常数为K2,电离出Cr2O72-的电离平衡常数为K3,则K2
(6)上表中铬酸的物质的量浓度为
查看习题详情和答案>>
6FeO?Cr2O3+24NaOH+7KClO3
| ||

试回答下列问题
(1)指出24Cr在周期表中的位置是
第四周期第ⅥB
第四周期第ⅥB
,(2)NaFeO2能强烈水解,在操作②生成沉淀而除去,写出该反应的化学方程式:
NaFeO2+2H2O=Fe(OH)3↓+NaOH
NaFeO2+2H2O=Fe(OH)3↓+NaOH
.(3)操作③调节pH=7~8的原因是
由于溶液在硅酸钠和偏铝酸钠发生水解,SiO32-+H2O?HSiO3-+OH-,HSiO3-+H2O?H2SiO3+OH-,AlO2-+H2O?Al(OH)3+OH-,降低pH值有利于平衡向正反应方向移动,当pH调到7~8时,使它们水解完全.
由于溶液在硅酸钠和偏铝酸钠发生水解,SiO32-+H2O?HSiO3-+OH-,HSiO3-+H2O?H2SiO3+OH-,AlO2-+H2O?Al(OH)3+OH-,降低pH值有利于平衡向正反应方向移动,当pH调到7~8时,使它们水解完全.
.(用简要的文字和离子方程式说明)下表是铬酸(H2CrO4)溶液中离子的组成与pH的关系:
| pH | C(CrO42-)mol/L | C(HCrO4-)mol/L | C(Cr2O72-)mol/L | C(H2CrO4)mol/L |
| 4 | 0.0003 | 0.104 | 0.448 | 0 |
| 5 | 0.0033 | 0.103 | 0.447 | 0 |
| 6 | 0.0319 | 0.0999 | 0.437 | 0 |
| 7 | 0.2745 | 0.086 | 0.3195 | 0 |
| 8 | 0.902 | 0.0282 | 0.0347 | 0 |
| 9 | 0.996 | 0.0031 | 0.0004 | 0 |
酸化使CrO42-转化为Cr2O72-
酸化使CrO42-转化为Cr2O72-
.(5)在铬酸(H2CrO4)溶液中,电离出CrO42-的电离平衡常数为K2,电离出Cr2O72-的电离平衡常数为K3,则K2
<
<
K3(填>、﹦、<)(6)上表中铬酸的物质的量浓度为
1.00mol/L
1.00mol/L
.(精确到小数点后2位)