摘要:C 2.D 3.A C 4.D 5.C
网址:http://m.1010jiajiao.com/timu3_id_161015[举报]
4-硫醚基喹唑啉类化合物是一种具有应用前景的抑菌药物,其合成路线如下:

已知:
(1)写出反应类型A→B
(2)满足下列条件的C的同分异构体的结构简式有
①苯的衍生物,且苯环上的一取代产物有两种;②苯环上有四个取代基,其中三个为甲氧基(-OCH3),其在苯环上位置与C相同;③含-COO-基团.
(3)写出C→D的化学方程式
 .由C→D的反应中还可能生成一种有机副产物,该副产物的结构简式为
.由C→D的反应中还可能生成一种有机副产物,该副产物的结构简式为
 .
.
(4)写出物质G的结构简式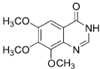
 .
.
(5)利用题给相关信息,以甲苯、HCONH2为原料,合成 .合成过程中无机试剂任选;合成路线流程图示例为:
.合成过程中无机试剂任选;合成路线流程图示例为:
提示:① ; ②
; ② ;③
;③

 .
.
查看习题详情和答案>>

已知:

(1)写出反应类型A→B
取代反应
取代反应
,E→F还原反应
还原反应
.(2)满足下列条件的C的同分异构体的结构简式有
4
4
种(不包含C).①苯的衍生物,且苯环上的一取代产物有两种;②苯环上有四个取代基,其中三个为甲氧基(-OCH3),其在苯环上位置与C相同;③含-COO-基团.
(3)写出C→D的化学方程式




(4)写出物质G的结构简式


(5)利用题给相关信息,以甲苯、HCONH2为原料,合成
 .合成过程中无机试剂任选;合成路线流程图示例为:
.合成过程中无机试剂任选;合成路线流程图示例为:
提示:①
 ; ②
; ② ;③
;③


5-氨基酮戊酸盐是一种抗肿瘤药,其合成路线如下:

已知:R-NO2
R-NH2
(1)5-氨基酮戊酸盐中非含氧官能团的名称是
(2)C→D的反应类型为
(3)已知A分子结构中有一个环,A不能使溴水褪色,且核磁共振氢谱图上只有一种环境的氢原子,则A的结构简式为
 .
.
(4)G是B的一种同分异构体,能与NaHCO3溶液反应,能发生银镜反应,1molG与足量金属Na反应能生成1molH2,且G分子中不含甲基,写出一种符合上述条件的G的结构简式 (任写一个)
(任写一个) (任写一个).
(任写一个).
(5)写出D→E反应的化学方程式
 .
.
(6)已知 ,请结合题中所给信息,写出由CH3CH2COOH、
,请结合题中所给信息,写出由CH3CH2COOH、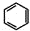 为原料合成
为原料合成 单体的第一步的合成路线和最后一步的化学方程式(无机试剂任选).
单体的第一步的合成路线和最后一步的化学方程式(无机试剂任选).
①第一步的合成路线:

②最后一步的化学方程式: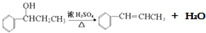
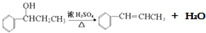 .
.
查看习题详情和答案>>

已知:R-NO2
| H2 | Pd/C |
(1)5-氨基酮戊酸盐中非含氧官能团的名称是
氨基
氨基
.(2)C→D的反应类型为
取代反应
取代反应
.(3)已知A分子结构中有一个环,A不能使溴水褪色,且核磁共振氢谱图上只有一种环境的氢原子,则A的结构简式为


(4)G是B的一种同分异构体,能与NaHCO3溶液反应,能发生银镜反应,1molG与足量金属Na反应能生成1molH2,且G分子中不含甲基,写出一种符合上述条件的G的结构简式
 (任写一个)
(任写一个) (任写一个)
(任写一个)(5)写出D→E反应的化学方程式


(6)已知
 ,请结合题中所给信息,写出由CH3CH2COOH、
,请结合题中所给信息,写出由CH3CH2COOH、 为原料合成
为原料合成 单体的第一步的合成路线和最后一步的化学方程式(无机试剂任选).
单体的第一步的合成路线和最后一步的化学方程式(无机试剂任选).①第一步的合成路线:


②最后一步的化学方程式:
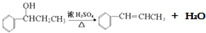
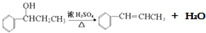
A.B.C.D.E、F是中学化学中常见的气体,它们均由短周期元素组成,具有如下性质:
①B能使湿润的红色石蕊试纸变蓝,D、F不能使湿润的石蕊试纸变色;
②A能使湿润的蓝色石蕊试纸先变红,后褪色;将红热的铜丝放入装有A的瓶中,瓶内充满棕黄色的烟;
③将点燃的镁条放入装有E的瓶中,镁条剧烈燃烧,生成白色粉末,瓶内壁附着黑色颗粒;
④D是最简单的有机物;F是空气中含量最多的气体.
⑤实验室中可用浓的C溶液与某黑色固体共热制A气体.
回答下列问题:
(1)B的化学式为
(2)③中发生反应的化学方程式是
(3)⑤中发生反应的化学方程式是
(4)已知标准状况下体积为1.12L的D完全燃烧生成E和液态水时,放出热量44.5kJ,写出表示1molD燃烧的热化学方程式
(5)一定条件下,向废水中加入CH3OH,将HNO3还原成F.若该反应消耗16gCH3OH转移3mol电子;该反应的化学方程式为
查看习题详情和答案>>
①B能使湿润的红色石蕊试纸变蓝,D、F不能使湿润的石蕊试纸变色;
②A能使湿润的蓝色石蕊试纸先变红,后褪色;将红热的铜丝放入装有A的瓶中,瓶内充满棕黄色的烟;
③将点燃的镁条放入装有E的瓶中,镁条剧烈燃烧,生成白色粉末,瓶内壁附着黑色颗粒;
④D是最简单的有机物;F是空气中含量最多的气体.
⑤实验室中可用浓的C溶液与某黑色固体共热制A气体.
回答下列问题:
(1)B的化学式为
NH3
NH3
,固态E可用作致冷剂
致冷剂
(写一种重要用途)(2)③中发生反应的化学方程式是
2Mg+CO2
2MgO+C
| ||
. |
2Mg+CO2
2MgO+C
;
| ||
. |
(3)⑤中发生反应的化学方程式是
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
;
| ||
(4)已知标准状况下体积为1.12L的D完全燃烧生成E和液态水时,放出热量44.5kJ,写出表示1molD燃烧的热化学方程式
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ/mol
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ/mol
.(5)一定条件下,向废水中加入CH3OH,将HNO3还原成F.若该反应消耗16gCH3OH转移3mol电子;该反应的化学方程式为
5CH3OH+6HNO3═5CO2+3N2+13H2O
5CH3OH+6HNO3═5CO2+3N2+13H2O
.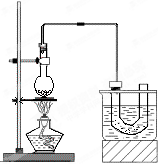 、实验室制备溴乙烷(C2H5Br)的装置和步骤如图:(已知溴乙烷的沸点38.4℃)
、实验室制备溴乙烷(C2H5Br)的装置和步骤如图:(已知溴乙烷的沸点38.4℃)①检查装置的气密性,向装置图所示的U形管和大烧杯中加入冰水;
②在圆底烧瓶中加入10mL95%乙醇、28mL80%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;
③小心加热,使其充分反应.
回答下列问题:
(1)该实验制取溴乙烷的化学方程式为:
NaBr+H2SO4+C2H5OH
NaHSO4+C2H5Br+H2O
| △ |
NaBr+H2SO4+C2H5OH
NaHSO4+C2H5Br+H2O
| △ |
(2)反应时若温度过高,可看到有红棕色气体产生,该气体分子式为
Br2
Br2
,同时还生成另一种无色气体.(3)U型管内可观察到的现象是
有油状液体生成
有油状液体生成
.(4)反应结束后,U形管中粗制的C2H5Br呈棕黄色.为了除去粗产品中的杂质,可选择下列试剂中的
C
C
(填字母)A.NaOH溶液 B.H2O C.Na2SO3溶液 D.CCl4
所需的主要玻璃仪器是
分液漏斗
分液漏斗
(填仪器名称).要进一步制得纯净的C2H5Br,可用水洗,然后加入无水CaCl2,再进行蒸馏
蒸馏
(填操作名称).(5)下列几项实验步骤,可用于检验溴乙烷中溴元素,其正确的操作顺序是:取少量溴乙烷,然后
④①⑤③②
④①⑤③②
(填代号).①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH溶液;⑤冷却
(6)溴乙烷(C2H5Br)多一个碳的同系物所有可能的物质在氢氧化钠的醇溶液中能发生反应,写出该反应的化学方程式
CH3CH2CH2Br+NaOH
CH3CH=CH2+NaBr+H2O
| 醇 |
| △ |
CH3CH2CH2Br+NaOH
CH3CH=CH2+NaBr+H2O
,| 醇 |
| △ |
CH3CHBrCH3+NaOH
CH3CH=CH2+NaBr+H2O
| 醇 |
| △ |
CH3CHBrCH3+NaOH
CH3CH=CH2+NaBr+H2O
.| 醇 |
| △ |
A、B均为无色盐溶液,B的焰色反应呈黄色,一定条件下A、B可以发生如图所示的物质之间的一系列变化:

若E为黄绿色气体,F为无色刺激性气味的气体,H不溶于稀硝酸.请填写下列空白.
(1)气体F的化学式为
(2)写出下列反应的离子方程式:C→E
(3)试分析E和F按下列两种情况分别通入水中,所得溶液分别滴入几滴石蕊溶液的现象:
①E和F物质的量相等,现象为:
②E和F物质的量不等,且E大于F,现象为:
(4)向C的溶液中加入AgNO3和KBr,当两种沉淀共存时,c(Br-)/c(Cl-)=
[已知:Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10].
查看习题详情和答案>>

若E为黄绿色气体,F为无色刺激性气味的气体,H不溶于稀硝酸.请填写下列空白.
(1)气体F的化学式为
SO2
SO2
,B中溶质的化学式为Na2SO3
Na2SO3
.(2)写出下列反应的离子方程式:C→E
2Cl-+2H2O
Cl2↑+H2↑+2OH-
| ||
2Cl-+2H2O
Cl2↑+H2↑+2OH-
;D+G→H
| ||
BaSO3+2H++SO42-=BaSO4↓+SO2↑+H2O
BaSO3+2H++SO42-=BaSO4↓+SO2↑+H2O
;(3)试分析E和F按下列两种情况分别通入水中,所得溶液分别滴入几滴石蕊溶液的现象:
①E和F物质的量相等,现象为:
变红色
变红色
;原因为(用化学方程式表示)Cl2+SO2+2H2O=H2SO4+2HCl
Cl2+SO2+2H2O=H2SO4+2HCl
.②E和F物质的量不等,且E大于F,现象为:
先变红后褪色(或褪色)
先变红后褪色(或褪色)
;原因为(文字说明)变红是因为溶液呈酸性,褪色是因为氯气过量生成次氯酸使溶液褪色
变红是因为溶液呈酸性,褪色是因为氯气过量生成次氯酸使溶液褪色
.(4)向C的溶液中加入AgNO3和KBr,当两种沉淀共存时,c(Br-)/c(Cl-)=
2.7×10-3
2.7×10-3
.[已知:Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10].