网址:http://m.1010jiajiao.com/timu3_id_160145[举报]
已知使用林德拉催化剂(Pd/PbO、CaCO3)可使炔烃的氢化停留在生成烯烃的阶段,而不再进一步氢化。现有一课外活动兴趣小组利用上述原理设计了一套由如下图所示的仪器组装而成的实验装置(铁架台未画出),由乙炔制得乙烯,并测定在氢化反应中乙炔的转化率。若用含0.020 mol CaC2的电石和含1.30 g锌的锌粒(杂质不与酸反应)分别与足量的饱和食盐水和稀硫酸反应,当反应完全后,假定在标准状况下测得G中收集到的水的体积为V mL(忽略乙炔在水中溶解的部分)。试回答下列问题:
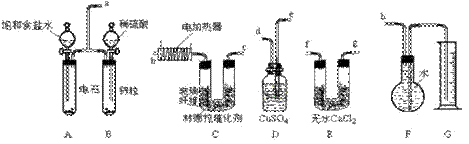
(1)各装置的连接顺序为
a→_________→_________→_________→_______→_______→_______→h。
(2)写出C中所发生反应的化学方程式:
______________________________________________________________。
(3)装置A中产生气体的反应速率往往太快,为了减慢反应速率,操作时还应采取的措施是
___________________________________________________ _。
(4)装置D的作用 。
(5)G所选用的量筒的容积较合理的是______________(填写选项字母)。
A.500 mL B.1000 mL C.1500mL
(6)若V=672(导管内气体体积忽略不计),
则乙炔的转化率为_________ _。
用18 mol/L浓硫酸配制100 ml 3.0 mol/L稀硫酸实验步骤如下:
①计算所用硫酸的体积
②量取一定体积的浓硫酸
③溶解
④转移、洗涤
⑤定容、摇匀
回答下列问题:
(1)所需浓硫酸的体积是________ml;
(2)所需要的仪器有:容量瓶(规格:________)、量筒(规格:________)
(从下列中选用填序号:A.10 ml B.25 ml C.500 ml D.250 ml E.100 ml),
除此之外还需要的仪器有:________.
(3)下列情况对所配制的稀硫酸浓度有何影响?(用偏高、偏低、无影响填写)
A.所用的溶解仪器未洗涤________;
B.容量瓶用蒸馏水洗涤后未干燥________;
C.所用的浓硫酸长时间放置在敞口容器内________;
D.定容时仰视溶液的凹液面________;
E.溶解后立即转移到容量瓶中定容________.
|
已知中和热的数值是57.3 kJ·mol-1.下列物质反应时,产生57.3 kJ热量的是 | |
| [ ] | |
A. |
稀HCl和稀NaOH |
B. |
1.0 mol·L-1 HCl和1.0 mol·L-1 NaOH |
C. |
500 mL 2.0 mol·L-1 HCl和500 mL 2.0 mol·L-1 NaOH |
D. |
500 mL 2.0 mol·L-1 H2SO4和500 mL 2.0 mol·L-1 Ba(OH)2 |
|
下列说法不正确的是 | |
| [ ] | |
A. |
500 mL 1 mol/LFe2(SO4)3溶液和250 mL 3 mol/L的Na2SO4溶液所含硫酸根离子的物质的量浓度相等 |
B. |
常温下可用铁、铝制品盛装浓硫酸或浓硝酸 |
C. |
制玻璃的主要原料是石灰石和黏土,SiO2是制光导纤维的主要材料, |
D. |
液氨可用作制冷剂,Na2O2常用作呼吸面具中的氧气源 |