题目内容
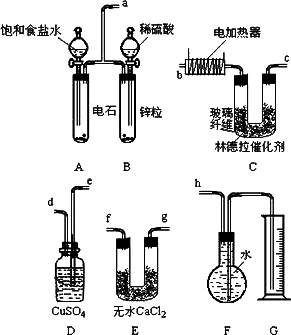
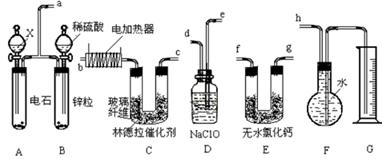
已知使用林德拉催化剂(Pd/PbO、CaCO3)可使炔烃的氢化停留在生成烯烃的阶段,而不再进一步氢化。现有一课外活动兴趣小组利用上述原理设计了一套由如下图所示的仪器组装而成的实验装置(铁架台未画出),由乙炔制得乙烯,并测定在氢化反应中乙炔的转化率。若用含0.020 mol CaC2的电石和含1.30 g锌的锌粒(杂质不与酸反应)分别与足量的饱和食盐水和稀硫酸反应,当反应完全后,假定在标准状况下测得G中收集到的水的体积为V mL(忽略乙炔在水中溶解的部分)。试回答下列问题:
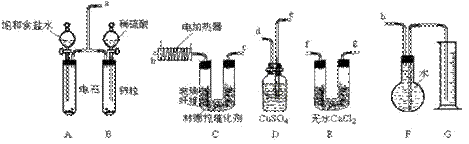
(1)各装置的连接顺序为
a→_________→_________→_________→_______→_______→_______→h。
(2)写出C中所发生反应的化学方程式:
______________________________________________________________。
(3)装置A中产生气体的反应速率往往太快,为了减慢反应速率,操作时还应采取的措施是
___________________________________________________ _。
(4)装置D的作用 。
(5)G所选用的量筒的容积较合理的是______________(填写选项字母)。
A.500 mL B.1000 mL C.1500mL
(6)若V=672(导管内气体体积忽略不计),
则乙炔的转化率为_________ _。
(1)e→d→f→g→b→c或e→d→g→f→b→c(2分)
(2)HC≡CH+H2![]() CH2=CH2(2分)
CH2=CH2(2分)
(3)通过调节分液漏斗的活塞,缓慢滴入饱和食盐水(1分)
(4)除去杂质气体
(5)B(1分);(6)50%(2分)