网址:http://m.1010jiajiao.com/timu3_id_159629[举报]
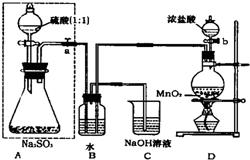 长期存放的亚硫酸钠可能会被空气中的氧气氧化.某化学兴趣小组通过实验来测定亚硫酸钠试剂的被氧化的程度,设计了如图实验:请回答下面的问题:
长期存放的亚硫酸钠可能会被空气中的氧气氧化.某化学兴趣小组通过实验来测定亚硫酸钠试剂的被氧化的程度,设计了如图实验:请回答下面的问题:(1)若将虚线框内的分液漏斗换成长颈漏斗,则应该怎样检查虚线框内装置的气密性?
(2)D装置中反应的化学方程式为
| ||
| ||
(3)称量ag Na2SO3样品放入锥形瓶中,向B装置反应后的溶液中加入足量的BaCl2溶液充分反应,过滤、洗涤、干燥,得白色沉淀bg,原样品中Na2SO3的质量分数为
| 126b |
| 233a |
| 126b |
| 233a |
(4)为保证实验测定的准确性,则C装置中反应的离子方程式为:
(5)现有以下试剂:①蒸馏水、②稀盐酸、③稀硝酸、④BaCl2溶液、⑤Ba(NO3)2溶液,请从中选择合适试剂,
长期存放的亚硫酸钠可能会被空气中的氧气氧化。某化学兴趣小组通过实验来测定亚硫酸钠试剂被氧化的程度,设计了下图实验,请回答下面的问题:
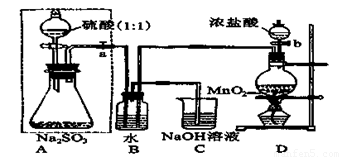
(1)D装置中反应的化学方程式为 。
B装置中反应的离子方程为 。
(2)称量ag Na2SO3样品放入锥形瓶中,向B装置反应后的溶液中加入足量的BaCl2溶液充分反应、过滤、洗涤、干燥,得白色沉淀bg,原样品中Na2SO3的质量分为数为: 。
(3)为保证实验测定的准确性,A中的硫酸什么时候滴加 ,
C装置中NaOH溶液的作用是 _________________。
(4)现有以下试剂:①蒸馏水、②稀盐酸、③稀硝酸、④BaCl2溶液、⑤Ba(NO3)2溶液,请从中选择合适试剂,设计一种不同的实验方法,测定试样中无水亚硫酸钠被氧化的程度,你使用试剂的顺序为: 。(填试剂编号)
查看习题详情和答案>>

请回答下列问题:
(1)若将虚线框内的分液漏斗换成长颈漏斗,则应该怎样检查虚线框内装置的气密性:____________________________________________________________________;
(2)C装置中氢氧化钠溶液的作用是______________________________________________;
(3)D装置中反应的化学方程式为________________________________________________;
(4)利用上述实验方案测原样品中亚硫酸钠的质量分数,除了已知亚硫酸钠样品的质量外,根据实验的可行性还需测定的数据是___________;
(5)现有以下试剂:蒸馏水、稀盐酸、稀硝酸、BaCl2溶液、Ba(NO3)2溶液,请从中选择合适的试剂,设计一种不同的实验方法测定试样中无水亚硫酸钠被氧化的程度,写出你设计的实验方法中所用到的试剂_______________。
查看习题详情和答案>>(14分)长期存放的亚硫酸钠可能会被空气中的氧气氧化。某化学兴趣小组通过实验来测定亚硫酸钠试剂被氧化的程度,设计了下图实验,请回答下面的问题: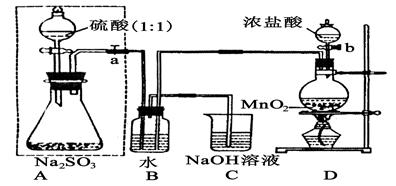
(1)D装置中反应的化学方程式为 。
B装置中反应的离子方程为 。
(2)称量ag Na2SO3样品放入锥形瓶中,向B装置反应后的溶液中加入足量的BaCl2溶液充分反应、过滤、洗涤、干燥,得白色沉淀bg,原样品中Na2SO3的质量分为数为: 。
(3)为保证实验测定的准确性,A中的硫酸什么时候滴加
C装置中的作用是 _________________。
(4)现有以下试剂:①蒸馏水、②稀盐酸、③稀硝酸、④BaCl2溶液、⑤Ba(NO3)2溶液,请从中选择合适试剂,设计一种不同的实验方法,测定试样中无水亚硫酸钠被氧化的程度,你使用试剂的顺序为: 。(填试剂编号)
(14分)长期存放的亚硫酸钠可能会被空气中的氧气氧化。某化学兴趣小组通过实验来测定亚硫酸钠试剂被氧化的程度,设计了下图实验,请回答下面的问题:
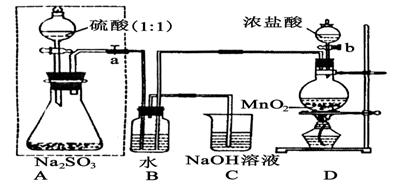
(1)D装置中反应的化学方程式为 。
B装置中反应的离子方程为 。
(2)称量ag Na2SO3样品放入锥形瓶中,向B装置反应后的溶液中加入足量的BaCl2溶液充分反应、过滤、洗涤、干燥,得白色沉淀bg,原样品中Na2SO3的质量分为数为: 。
(3)为保证实验测定的准确性,A中的硫酸什么时候滴加
C装置中的作用是 _________________。
(4)现有以下试剂:①蒸馏水、②稀盐酸、③稀硝酸、④BaCl2溶液、⑤Ba(NO3)2溶液,请从中选择合适试剂,设计一种不同的实验方法,测定试样中无水亚硫酸钠被氧化的程度,你使用试剂的顺序为: 。(填试剂编号)
查看习题详情和答案>>