摘要:有三种元素X.Y.Z.都是短周期元素.X和Y位于周期表的同一周期.可形成共价化合物XY2.此化合物在常温下呈气态.Z和X为同族元素.Z和Y可形成共价化合物ZY2.此化合物在常温下为固态.X的单质跟ZY2反应可生成Z的单质.Z的一种晶体是很好的半导体材料.根据以上事实.判断X.Y.Z各为什么元素.写出有关方程式.
网址:http://m.1010jiajiao.com/timu3_id_158488[举报]
有三种元素X、Y、Z,都是短周期元素;X和Y位于周期表的同一周期,可形成共价化合物XY2,此化合物在常温下呈气态;Z和X为同族元素;Z和Y可形成共价化合物ZY2,此化合物在常温下为固态;X的单质跟ZY2反应可生成Z的单质,Z的一种晶体是很好的半导体材料。
根据以上事实.判断X、Y、Z各为什么元素,写出有关方程式。
查看习题详情和答案>>
X、Y、Z分别是短周期元素的三种单质,它们都是常见的金属或非金属.M、N、R是常见的三种氧化物.其中一种具有高熔点,而且有如下反应(条件未标出,方程未配平):
⑴X + Z → N; ⑵M+X → N; ⑶ M+Y→ R+X 。
若X是非金属,则组成Y单质的元素在周期表中的位置是
| A.第二周期ⅣA族 | B.第二周期ⅥA族 | C.第三周期ⅡA族 | D.第三周期ⅣA族 |
X、Y、Z分别是短周期元素的三种单质,它们都是常见的金属或非金属.M、N、R是常见的三种氧化物.其中一种具有高熔点,而且有如下反应(条件未标出,方程未配平):
⑴X + Z → N; ⑵M+X → N; ⑶ M+Y→ R+X 。
若X是非金属,则组成Y单质的元素在周期表中的位置是
A.第二周期ⅣA族 B.第二周期ⅥA族 C.第三周期ⅡA族 D.第三周期ⅣA族
查看习题详情和答案>> X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化:
X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化:一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10.请回答下列问题:
(1)X元素在周期表中的位置是
第2周期VIA族
第2周期VIA族
.(2)分析同主族元素性质的递变规律,发现B、C物质沸点反常,这是因为它们的分子之间存在
氢键
氢键
.(3)①C在一定条件下反应生成A的化学方程式是
4NH3+5O2=4NO+6H2O
4NH3+5O2=4NO+6H2O
.②X、Y、Z三种元素可组成一种强酸W,C在适当条件下被W吸收生成一种盐.该盐的水溶液pH
小于
小于
7(填“大于”、“小于”、“等于”),其原因是(写出离子方程式)NH4++H2O NH3?H2O+H+
NH3?H2O+H+
 NH3?H2O+H+
NH3?H2O+H+NH4++H2O NH3?H2O+H+
NH3?H2O+H+
. NH3?H2O+H+
NH3?H2O+H+(4)已知Y单质与Z单质生成C的反应是可逆反应,△H<0.将等物质的量的Y、Z两种单质充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应.下列说法正确的有
ad
ad
.a.达到化学平衡时,正反应速率与逆反应速率相等
b.反应过程中,Y单质的体积分数始终为50%
c.达到化学平衡时,Y、Z两种单质在混合气体中的物质的量之比为1:1
d.达到化学平衡的过程中气体平均相对分子质量减小
e.达到化学平衡后,升高温度,C的体积分数增大.
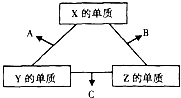 X、Y、Z三种短周期元素,它们的原子序数之和为16.在常温下,X、Y、Z三种元素的常见单质都是无色气体,它们在适当条件下可发生如图所示的转化.已知一个B分子中含有Z元素的原子个数比一个C分子中含有Z元素的原子个数少一个.请回答下列问题:
X、Y、Z三种短周期元素,它们的原子序数之和为16.在常温下,X、Y、Z三种元素的常见单质都是无色气体,它们在适当条件下可发生如图所示的转化.已知一个B分子中含有Z元素的原子个数比一个C分子中含有Z元素的原子个数少一个.请回答下列问题:(1)X元素在周期表中的位置是
第二周期VIA族
第二周期VIA族
.Y的原子序数为7
7
.(2)X的单质与Z的单质可制成新型的化学电源,该电源被称为
氢氧燃料电池
氢氧燃料电池
.(3)A的化学式为
NO
NO
.(4)已知Y的单质与Z的单质在适当催化剂和高温、高压条件下,生成C的反应是可逆反应,写出该反应的化学方程式
N2+3H2
2NH3
| 高温、高压 |
| 催化剂 |
N2+3H2
2NH3
.| 高温、高压 |
| 催化剂 |