摘要: 1L的溶液吸收.求所得溶液中溶质的成分及物质的量是多少?
网址:http://m.1010jiajiao.com/timu3_id_158435[举报]
用1L 1.0mol?L-1NaOH溶液吸收17.92L CO2(标准状况)后溶液体积不变.求所得溶液中的CO32-和HCO3-的物质的量浓度.
(已知可能的反应为:2NaOH+CO2═Na2CO3+H2O,Na2CO3+H2O+CO2═2NaHCO3)
查看习题详情和答案>>
(已知可能的反应为:2NaOH+CO2═Na2CO3+H2O,Na2CO3+H2O+CO2═2NaHCO3)
 硫酸生产主要有硫磺法和硫铁矿法等,这两种制法均经过催化氧化步骤.
硫酸生产主要有硫磺法和硫铁矿法等,这两种制法均经过催化氧化步骤.(1)钒触媒(V2O5)能加快SO2的氧化速率,此过程中SO2先与V2O5反应生成V2O4.该过程的化学方程式可表示为
SO2+V2O5?V2O4+SO3
SO2+V2O5?V2O4+SO3
.(2)为测定过程中混合气的SO2体积分数,选用0.0500mol/LI2的标准溶液、淀粉溶液进行测定.已知:V(耗用I2标准溶液)=10.00mL,V(采集烟气)=100.0mL(已折算为标准状况),则烟气中SO2的体积分数为
0.112
0.112
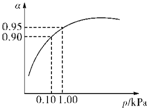
.(3)一定温度时,SO2的平衡转化率(α)与体系总压强(p)的关系如图所示.试分析工业生产中采用常压的原因是
在常压时,SO2的转化率已很高,若加压,则对设备、能源等有较高的要求,经济上不划算
在常压时,SO2的转化率已很高,若加压,则对设备、能源等有较高的要求,经济上不划算
.(4)在温度相同、体积均为1L的三个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下.
已知:2SO2(g)+O2(g)?2SO3(g);△H=-98.3kJ?mol-1.
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2molSO2、1molO2 | 2molSO3 | mmolSO2、nmolO2、pmolSO3 |
| c(SO3)/mol?L-1 | 1.4 | 1.4 | 1.4 |
| 能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| SO2或SO3的转化率 | α1 | α2 | 12.5% |
1
1
,p=1.6
1.6
mol,b+c=39.32
39.32
kJ.