摘要:20.将a mol Na202与a mol Ca(HCO3)2的固体混合物在密闭容器中加热至250oC左右.使其充分反应.容器内固体的量及成分是( ) ①a mol CaCO3 ②2a mol NaOH ③a mol Na2CO3 ④a mol NaHCO3 ⑤a mol Na202 ①.③ ③
网址:http://m.1010jiajiao.com/timu3_id_158162[举报]
 运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.
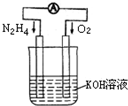
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.(1)发射卫星时可用肼(N2H4)作燃料,其方程式为:
N2H4+O2=N2+2H2O,若将此反应设计成如右图所示的原电池装置,请回答:
①负极反应式为:
N2H4+4OH--4e-=N2+4H2O
N2H4+4OH--4e-=N2+4H2O
;②工作一段时间后正极附近溶液的pH变化为
增大
增大
(填“增大”“减小”或“不变”);③若用该电池电解以石墨为电极的100mL氯化铜溶液,一段时间后,两极均收集到2.24L气体(已换算成标准状况下的体积),则原溶液中Cu2+的物质的量浓度为
0.5 mol?L-1
0.5 mol?L-1
.(2)在25℃时,向浓度均为0.1mol?L-1的MgCl2和CuCl2 混合溶液中逐滴加入氨水,首先生成
Cu(OH)2
Cu(OH)2
沉淀(填化学式),生成该沉淀的离子方程式为Cu2++2NH3?H20=Cu(OH)2↓+2NH4+
Cu2++2NH3?H20=Cu(OH)2↓+2NH4+
.(已知25℃Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20).(3)在25℃时,将a mol?L-1的氨水与0.01mol?L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显
中
中
性(填“酸”“碱”或“中”),用含a的代数式表示NH3?H2O的电离常数kb=| 10-9 |
| a-0.01 |
| 10-9 |
| a-0.01 |
 (2013?江西模拟)甲醇是一种很好的燃料,工业上用CH4和H2O为原料,通过下述反应Ⅰ和Ⅱ来制备甲醇.
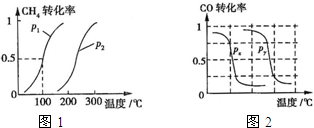
(2013?江西模拟)甲醇是一种很好的燃料,工业上用CH4和H2O为原料,通过下述反应Ⅰ和Ⅱ来制备甲醇.(1)将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L),在一定条件下发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g)…I.CH4的转化率与温度、压强的关系如图.
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为
0.003mol/(L?min)
0.003mol/(L?min)
.②图中的P1
<
<
P2(填“<”、“>”或“=”),100℃时平衡常数为2.25×10-4
2.25×10-4
.③该反应的△H
>
>
0(填“<”、“>”或“=”).(2)在压强为0.1MPa条件下,将a mol CO与3amol H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g)?CH3OH(g)△H<0
Ⅱ.
①若容器容积不变,下列措施可增加甲醇产率的是
BD
BD
.A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入1mol CO和3mol H2
②为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.
| 实验编号 | T(℃) | n(CO)/n(H2) | p(MPa) | ||
| l | 150 |
|
0.1 | ||
| 2 | n |
|
5 | ||
| 3 | 350 | m | 5 |
150
150
、b=| 1 |
| 3 |
| 1 |
| 3 |
B.根据反应Ⅱ的特点,右上图是在压强分别为0.1MPa和5MPa下CO的转化率随温度变化的曲线图,请指明图中的压强Px=
0.1
0.1
MPa.运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.
(1)合成氨反应,在2L密闭容器中通入2mol的N2和6mol的H2,5min时反应达到平衡,此时容器内的压强变为原来的3/4,0-5min该反应的化学反应速率为V(H2)=
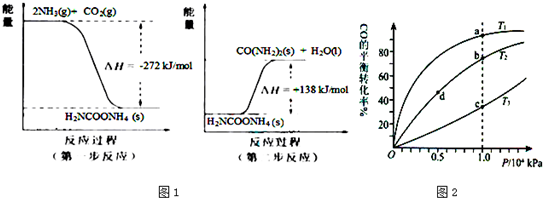
(2)NH3 (g)与CO2(g)经过两步反应生成尿素〔CO(NH2)2〕,两步反应的能量变化示意图1:
则NH3(g) 与CO2(g) 反应生成尿素的热化学方程式为
(3)用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)?CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图2所示.下列说法正确的是
A.温度:T1>T2>T3
B.平衡常数:K(a)>K(c)
C.平衡常数:K(b)=K(d)
D.正反应速率:v(b)>v(d)
E.平均摩尔质量:M(a)=M(c)
(4)在25℃下,将a mol?L-1的氨水与0.01mol?L-1的盐酸等体积混合,反应平衡时溶液中C(NH+4)=C(Cl?),则溶液显(
.
查看习题详情和答案>>
(1)合成氨反应,在2L密闭容器中通入2mol的N2和6mol的H2,5min时反应达到平衡,此时容器内的压强变为原来的3/4,0-5min该反应的化学反应速率为V(H2)=
0.3mol/(L.min)
0.3mol/(L.min)
,N2的转化率=50%
50%
,化学平衡常数K=0.59
0.59
.(2)NH3 (g)与CO2(g)经过两步反应生成尿素〔CO(NH2)2〕,两步反应的能量变化示意图1:
则NH3(g) 与CO2(g) 反应生成尿素的热化学方程式为
2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-134kJ/mol
2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-134kJ/mol
.(3)用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)?CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图2所示.下列说法正确的是
BCD
BCD
(填字母)A.温度:T1>T2>T3
B.平衡常数:K(a)>K(c)
C.平衡常数:K(b)=K(d)
D.正反应速率:v(b)>v(d)
E.平均摩尔质量:M(a)=M(c)
(4)在25℃下,将a mol?L-1的氨水与0.01mol?L-1的盐酸等体积混合,反应平衡时溶液中C(NH+4)=C(Cl?),则溶液显(
中
中
)性(填“酸”“碱”或“中”);用含a的代数式表示NH3?H2O的电离常数Kb=| 10-9 |
| a-0.01 |
| 10-9 |
| a-0.01 |

在0.1 mol?L-1的CH3COOH溶液中存在如下电离平衡:CH3COOH?CH3COO-+H+,
(1)请根据该平衡完成下列表格(电离平衡移动方向填“正方向”或“逆方向”,离子浓度、电离度的变化请用“增大”、“减小”或“不变”表示).
(2)在25℃下,将a mol/L的氨水与上述0.1 mol?L-1的CH3COOH溶液等体积混合,所得溶液中c(NH4+)=c(CH3COO-),则溶液显
.
查看习题详情和答案>>
(1)请根据该平衡完成下列表格(电离平衡移动方向填“正方向”或“逆方向”,离子浓度、电离度的变化请用“增大”、“减小”或“不变”表示).
| 改变条件 | 电离平衡移动 方向 |
电离度 | c(H+) | c(CH3COO-) |
| 加水稀释 | ||||
| 加少量HCl溶液 | ||||
| 加入少量CH3COONa固体 |
中
中
性(填“酸”、“碱”或“中”);请写出NH3?H2O的电离常数Kb=| c(NH4+).c(OH-) |
| c(NH3.H2O) |
| c(NH4+).c(OH-) |
| c(NH3.H2O) |
某同学设计下图装置进行铁和浓H2SO4反应的实验探究,请回答下列问题.
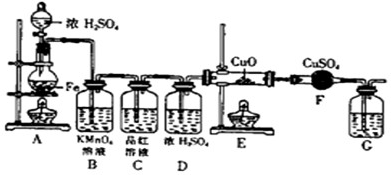
(1)将16克铁粉放入烧瓶中,由分液漏斗放入20mL 18mol/L的浓H2SO4,结果没有任何反应现象,原因是
(2)随着反应的进行,B中酸性KMnO4溶液颜色逐渐变浅(产物中有Mn2+),请用离子方程式表示:
(3)当G处有持续稳定的气泡时,再点燃E处酒精灯,这样操作的原因是
(4)反应一段时间后,E、F处可观察到明显的现象,F处的实验现象
(5)为了确保实验的严谨性和F中现象的可信性,通常在F装置后再接一个装置G,则G中盛放的液体可以是
A.CaCl2溶液 B.Ca(OH)2溶液 C.浓硫酸 D.CCl4
(6)将a mol Fe与含b mol H2SO4的浓硫酸共热,假设按本题的过程进行反应,如果Fe与H2SO4均恰好完全反应,则生成的有
气体1是
气体2是
查看习题详情和答案>>

(1)将16克铁粉放入烧瓶中,由分液漏斗放入20mL 18mol/L的浓H2SO4,结果没有任何反应现象,原因是
铁在冷的浓硫酸中钝化
铁在冷的浓硫酸中钝化
.随后点燃A处酒精灯,就有气体产生了.(2)随着反应的进行,B中酸性KMnO4溶液颜色逐渐变浅(产物中有Mn2+),请用离子方程式表示:
2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+
2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+
,C中品红溶液颜色始终没有变化.(3)当G处有持续稳定的气泡时,再点燃E处酒精灯,这样操作的原因是
待反应产生的H2将装置中的空气排尽再加热,防止H2与空气混合加热爆炸
待反应产生的H2将装置中的空气排尽再加热,防止H2与空气混合加热爆炸
.(4)反应一段时间后,E、F处可观察到明显的现象,F处的实验现象
白色粉末变为蓝色
白色粉末变为蓝色
.(5)为了确保实验的严谨性和F中现象的可信性,通常在F装置后再接一个装置G,则G中盛放的液体可以是
CD
CD
A.CaCl2溶液 B.Ca(OH)2溶液 C.浓硫酸 D.CCl4
(6)将a mol Fe与含b mol H2SO4的浓硫酸共热,假设按本题的过程进行反应,如果Fe与H2SO4均恰好完全反应,则生成的有
气体1是
H2
H2
,其物质的量为(2a-b)
(2a-b)
mol,气体2是
SO2
SO2
,其物质的量为(b-a)
(b-a)
mol.