摘要:某化学兴趣小组的同学为了体验“工业冶炼金属 的过程.在实验室做了CO还原CuO的实验.他们称得装有CuO粉末的试管重42g.反应完全后.恢复到室温称量.试管和固体残留物共重40.4g.并收集到CO2 4.4g.请你和他们一起计算: (1)42g – 40.4g = 1.6g.1.6g表示 的质量. (2)该反应制得铜的质量为多少克?
网址:http://m.1010jiajiao.com/timu3_id_15756[举报]
 (1)某化学兴趣小组的同学为了体验“工业冶炼金属”的过程.在实验室做了CO还原CuO的实验,他们称得装有CuO粉末的试管重102g,反应完全后,恢复到室温称量,试管和固体残留物共重100.4g,并收集到CO2 4.4g,请你和他们一起计算:
(1)某化学兴趣小组的同学为了体验“工业冶炼金属”的过程.在实验室做了CO还原CuO的实验,他们称得装有CuO粉末的试管重102g,反应完全后,恢复到室温称量,试管和固体残留物共重100.4g,并收集到CO2 4.4g,请你和他们一起计算:①102g-100.4g=1.6g,1.6g表示
②该反应制得铜的质量为
(2)某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢中,产生CO2气体的情况如下图所示:
①从图中可以看出,12.5g水垢与盐酸反应后生成的二氧化碳最多是
②求水垢中碳酸钙的质量分数.
③要配制10%的这种盐酸100g,至少需要38%的浓盐酸(密度1.19g?cm-3)多少毫升? 查看习题详情和答案>>
(2011?湘潭)某化学兴趣小组的同学为了探究Mg、Cu、Fe的金属活动性顺序开展了一下以下探究活动.
(1)进行试验,获得结论.完成如下实验报告,并回答有关问题.
(2)反思与交流.经过讨论,该小组同学一致认为:比较金属与酸反应产生氢气的快慢,有两种测定方法: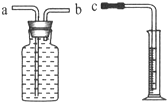
方法一是在相同时间内测量氢气体积的大小.若用右图所示装置测量,则接口c应与
方法二是测定产生相同体积氢气时
查看习题详情和答案>>
(1)进行试验,获得结论.完成如下实验报告,并回答有关问题.
| 实验方案 | 实验现象 | 实验结论 | |
| 方 案 一 | 将Fe丝浸入CuSO4溶液中 | Fe丝表面有红色物质析出 | 金属活动性:Fe > > Cu(填“>”或“<”)该反应的反应类型属于置换 置换 反应. |
| 方 案 二 | 将Mg和Cu分别在空气中灼烧 | 发现 Mg Mg (填元素符号)能剧烈燃烧,而另一种不能 | 金属活动性:Mg > > Cu(填“>”或“<”) |
方 案 三 | 分别将Mg和Fe放入 稀H2SO4 稀H2SO4 (一种酸)溶液中,观察现象 | 观察到 Fe Fe (填元素符号)产生气泡的速度较慢 | 金属活动性顺序:Mg>Fe |

方法一是在相同时间内测量氢气体积的大小.若用右图所示装置测量,则接口c应与
a
a
(填“a”或“b”)相连.方法二是测定产生相同体积氢气时
所需的时间
所需的时间
.Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件.某化学兴趣小组的同学为了测定某黄铜的组成,取20g该黄铜样品于烧杯中,向其中加入50g稀硫酸,使之恰好完全反应.反应后烧杯中的剩余物的质量为69.8g.试回答下列问题:
(1)反应后产生的H2的质量是 g.
(2)黄铜样品中铜的质量分数为是多少?
(3)所用稀硫酸中硫酸的质量分数是多少?
查看习题详情和答案>>
(1)反应后产生的H2的质量是
(2)黄铜样品中铜的质量分数为是多少?
(3)所用稀硫酸中硫酸的质量分数是多少?