网址:http://m.1010jiajiao.com/timu3_id_155224[举报]
物质的量浓度
物质的量浓度的概念:以________里所含溶质B的________来表示溶液组成的物理量,叫做溶质B的物质的量浓度(符号cB).此概念可理解到以下几个层面
(1)公式:由此概念,可统摄出计算cB的公式:cB=![]()
cB=![]()
(2)单位:物质的量浓度单位是物质的量单位与体积单位的合成,有许多,如:mol·mL-1、mol·m-3、kmol·L-1、mmol·L-1、mol·mL-1等,常用单位是mol·L-1.
浓硫酸在高中化学实验中有着很重要的作用
(1)①铜与浓硫酸反应实验时,发现试管底部有白色固体并夹杂有少量黑色固体。倒去试管中的浓硫酸,将剩余固体(含少量浓硫酸)倒入盛有少量水的烧杯中,发现所得溶液为蓝色,黑色固体未溶解。过滤、洗涤后,向黑色固体中加入过量浓硝酸,黑色固体溶解,溶液呈蓝色,所得溶液加BaCl2溶液后有白色沉淀生成。则黑色固体中含有________元素。
②实验室利用浓硫酸分别与氯化钠固体和碘化钾固体加热反应制取所需物质,分析这两个反应中浓硫酸作用的异同点:_________________________________ 。
(2)探究浓硫酸的吸水性。某同学把98%的硫酸10mL和63.3%的硫酸(用10mL 98%的硫酸与10mL水配成)约20mL分别放入两个相同的大表面皿中,根据室温环境下实验的数据绘成的曲线如图。由右图曲线你能得到的实验结论有哪些?(写两点)______、_______________。
(3)苯与浓硝酸、浓硫酸制硝基苯的实验中,三种原料混合的顺序是_____________;要得到纯净的硝基苯,需经过:水洗 → 5%NaOH溶液洗涤 → 水洗 → 无水CaCl2干燥→________(填写操作),得到纯硝基苯。
(4)探究浓硫酸在生成乙酸乙酯反应中的作用。
问题提出:浓硫酸存在条件下酯化反应是否进行得更快。
设计实验:____________________。实验现象:___________________ 。
(5)浓硫酸与蔗糖反应的演示实验装置修改如下:实验时在大试管中先放入2g细小颗粒的蔗糖,滴加2—3滴碳酸钠浓溶液,再加入1.5mL 98%的浓硫酸,迅速塞紧带干燥管的单孔橡皮塞。可以看到,蔗糖迅速变黑,体积急剧膨胀,形成多孔海绵状固体物质——“黑面包”。分析实验效果更加明显的原因:____________________________________________________ 。
(6)苯分子等芳香烃化合物里的氢原子被硫酸分子里的磺酸基(—SO3H)所取代的反应,称为磺化反应。浓硫酸有时也用SO3代替浓硫酸,其优点是____________________、__________________。(至少写出两点)
用浓硫酸吸收SO3可得发烟硫酸(H2SO4·SO3)。某化工厂用1.5m3 98.3%的浓硫酸(密度为1.84g/mL)吸收SO3形成发烟硫酸,再与水混合,可得到95%的硫酸(密度为1.79g/mL)________m3(保留2位小数)。
(1)①铜与浓硫酸反应实验时,发现试管底部有白色固体并夹杂有少量黑色固体。倒去试管中的浓硫酸,将剩余固体(含少量浓硫酸)倒入盛有少量水的烧杯中,发现所得溶液为蓝色,黑色固体未溶解。过滤、洗涤后,向黑色固体中加入过量浓硝酸,黑色固体溶解,溶液呈蓝色,所得溶液加BaCl2溶液后有白色沉淀生成。则黑色固体中含有________元素。
②实验室利用浓硫酸分别与氯化钠固体和碘化钾固体加热反应制取所需物质,分析这两个反应中浓硫酸作用的异同点:_________________________________ 。
(2)探究浓硫酸的吸水性。某同学把98%的硫酸10mL和63.3%的硫酸(用10mL 98%的硫酸与10mL水配成)约20mL分别放入两个相同的大表面皿中,根据室温环境下实验的数据绘成的曲线如图。由右图曲线你能得到的实验结论有哪些?(写两点)______、_______________。

(3)苯与浓硝酸、浓硫酸制硝基苯的实验中,三种原料混合的顺序是_____________;要得到纯净的硝基苯,需经过:水洗 → 5%NaOH溶液洗涤 → 水洗 → 无水CaCl2干燥→________(填写操作),得到纯硝基苯。
(4)探究浓硫酸在生成乙酸乙酯反应中的作用。
问题提出:浓硫酸存在条件下酯化反应是否进行得更快。
设计实验:____________________。实验现象:___________________ 。
(5)浓硫酸与蔗糖反应的演示实验装置修改如下:实验时在大试管中先放入2g细小颗粒的蔗糖,滴加2—3滴碳酸钠浓溶液,再加入1.5mL 98%的浓硫酸,迅速塞紧带干燥管的单孔橡皮塞。可以看到,蔗糖迅速变黑,体积急剧膨胀,形成多孔海绵状固体物质——“黑面包”。分析实验效果更加明显的原因:____________________________________________________ 。

(6)苯分子等芳香烃化合物里的氢原子被硫酸分子里的磺酸基(—SO3H)所取代的反应,称为磺化反应。浓硫酸有时也用SO3代替浓硫酸,其优点是____________________、__________________。(至少写出两点)
用浓硫酸吸收SO3可得发烟硫酸(H2SO4·SO3)。某化工厂用1.5m3 98.3%的浓硫酸(密度为1.84g/mL)吸收SO3形成发烟硫酸,再与水混合,可得到95%的硫酸(密度为1.79g/mL)________m3(保留2位小数)。
 X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:
X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:
已知一个B分子中含有的Z元素的原子个数比一个C分子中少一个.而M的单质在常温常压下为固体,并且M元素是形成化合物种类最多的元素.请回答下列问题:
(1)元素X在周期表中的位置______.
(2)化合物C在一定条件下生成化合物A的化学方程式______.
(3)常温下,将C通入元素Y的最高价氧化物的水化物的水溶液中,得到pH=5的溶液,反应后的溶液存在的平衡体系有______;溶液中离子浓度由大到小的顺序为______.
(4)实验室里为制取C,常在C的浓溶液中加入生石灰.请叙述产生C的原因______.
(5)已知Y单质和Z单质生成C的反应是可逆反应,△H<0.将等物质的量的单质Y和单质Z充入一密闭容器中,在适当催化剂和恒温条件下反应.下列说法中正确的是______
a.达到化学平衡时,正反应与逆反应速率相等
b.反应过程中,单质Y的体积分数始终为50%
c.达到化学平衡时,Y单质和Z单质在混合气体中的物质的量之比为1:1
d.达到化学平衡的过程中,气体的平均相对分子质量逐渐增大
e.达到化学平衡时,再升高温度,C的体积分数增大
(6)由X、Z、M三种元素可以形成化合物M2Z6X,其蒸汽通过灼热的氧化铜,黑色的氧化铜会逐渐变红,则发生的有关化学方程式为______.
查看习题详情和答案>>
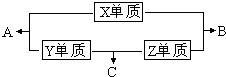 X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:
X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:已知一个B分子中含有的Z元素的原子个数比一个C分子中少一个.而M的单质在常温常压下为固体,并且M元素是形成化合物种类最多的元素.请回答下列问题:
(1)元素X在周期表中的位置
(2)化合物C在一定条件下生成化合物A的化学方程式
| ||
| △ |
| ||
| △ |
(3)常温下,将C通入元素Y的最高价氧化物的水化物的水溶液中,得到pH=5的溶液,反应后的溶液存在的平衡体系有
(4)实验室里为制取C,常在C的浓溶液中加入生石灰.请叙述产生C的原因
(5)已知Y单质和Z单质生成C的反应是可逆反应,△H<0.将等物质的量的单质Y和单质Z充入一密闭容器中,在适当催化剂和恒温条件下反应.下列说法中正确的是
a.达到化学平衡时,正反应与逆反应速率相等
b.反应过程中,单质Y的体积分数始终为50%
c.达到化学平衡时,Y单质和Z单质在混合气体中的物质的量之比为1:1
d.达到化学平衡的过程中,气体的平均相对分子质量逐渐增大
e.达到化学平衡时,再升高温度,C的体积分数增大
(6)由X、Z、M三种元素可以形成化合物M2Z6X,其蒸汽通过灼热的氧化铜,黑色的氧化铜会逐渐变红,则发生的有关化学方程式为
| 加热 |
| 加热 |