题目内容
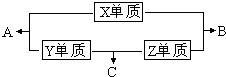 X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:
X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:已知一个B分子中含有的Z元素的原子个数比一个C分子中少一个.而M的单质在常温常压下为固体,并且M元素是形成化合物种类最多的元素.请回答下列问题:
(1)元素X在周期表中的位置
第2周期第ⅥA族
第2周期第ⅥA族
.(2)化合物C在一定条件下生成化合物A的化学方程式
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
.
| ||
| △ |
(3)常温下,将C通入元素Y的最高价氧化物的水化物的水溶液中,得到pH=5的溶液,反应后的溶液存在的平衡体系有
NH4++H2O?NH3?H2O+H+;H2O?OH-+H+;
NH4++H2O?NH3?H2O+H+;H2O?OH-+H+;
;溶液中离子浓度由大到小的顺序为c(NO3-)>c(NH4+)>c(H+)>c(OH-)
c(NO3-)>c(NH4+)>c(H+)>c(OH-)
.(4)实验室里为制取C,常在C的浓溶液中加入生石灰.请叙述产生C的原因
氧化钙溶于水放出大量热,温度升高,使氨的溶解度减小而放出;氧化钙吸水,促使氨放出;生成的氢氧化钙电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出.
氧化钙溶于水放出大量热,温度升高,使氨的溶解度减小而放出;氧化钙吸水,促使氨放出;生成的氢氧化钙电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出.
.(5)已知Y单质和Z单质生成C的反应是可逆反应,△H<0.将等物质的量的单质Y和单质Z充入一密闭容器中,在适当催化剂和恒温条件下反应.下列说法中正确的是
ab
ab
a.达到化学平衡时,正反应与逆反应速率相等
b.反应过程中,单质Y的体积分数始终为50%
c.达到化学平衡时,Y单质和Z单质在混合气体中的物质的量之比为1:1
d.达到化学平衡的过程中,气体的平均相对分子质量逐渐增大
e.达到化学平衡时,再升高温度,C的体积分数增大
(6)由X、Z、M三种元素可以形成化合物M2Z6X,其蒸汽通过灼热的氧化铜,黑色的氧化铜会逐渐变红,则发生的有关化学方程式为
CH3CH2OH+CuO
CH2CHO+Cu+H2O
| 加热 |
CH3CH2OH+CuO
CH2CHO+Cu+H2O
.| 加热 |
分析:X、Y、Z、W四种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,则三种气体单质为氢气、氮气、氧气.三种气体单质相互反应生成H2O、NH3、NO,一个B分子中含有的Z元素的原子个数比一个C分子中少一个,则B为H2O,C为NH3,Z为氢元素.由关系图可知:Z单质与X单质反应生成B(H2O),故X为氧元素;Z单质与Y单质反应生成C(NH3),故Y为氮元素;所以A为NO.W的单质在常温常压下为固体,并且W元素是形成化合物种类最多的元素,则W为碳元素.
解答:解:X、Y、Z、W四种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,则三种气体单质为氢气、氮气、氧气.三种气体单质相互反应生成H2O、NH3、NO,一个B分子中含有的Z元素的原子个数比一个C分子中少一个,则B为H2O,C为NH3,Z为氢元素.由关系图可知:Z单质与X单质反应生成B(H2O),故X为氧元素;Z单质与Y单质反应生成C(NH3),故Y为氮元素;所以A为NO.W的单质在常温常压下为固体,并且W元素是形成化合物种类最多的元素,则W为碳元素.
即X为氧元素,Y为氮元素,Z为氢元素,W为碳元素;A为NO,B为H2O,C为NH3.
(1)X为氧元素,原子核外有8个电子,有2个电子层,最外层电子数为6各电子,处于周期表中第2周期第ⅥA族.故答案为:第2周期第ⅥA族;
(2)C为NH3,A为NO,氨气在催化剂并加热的条件下生成一氧化氮与水,反应方程式为4NH3+5O2
4NO+6H2O,
故答案为:4NH3+5O2
4NO+6H2O;
(3)常温下,将C(NH3)通入元素Y(N)的最高价氧化物的水化物的水溶液HNO3中,Y为氮元素,最高价氧化物的水化物为HNO3,氨气与硝酸反应生成硝酸铵,得到pH=5的溶液,反应后的溶液存在的平衡体系有:NH4++H2O?NH3?H2O+H+;H2O?OH-+H+;硝酸铵属于强酸弱碱盐,铵根离子水解,溶液呈酸性,所以 c(NO3-)>c(NH4+),c(H+)>c(OH-);
故答案为:NH4++H2O?NH3?H2O+H+;H2O?OH-+H+; c(NO3-)>c(NH4+)>c(H+)>c(OH-);
(4)实验室里为制取C(NH3),常在C的浓溶液中加入生石灰.氧化钙溶于水放出大量热,温度升高,使氨的溶解度减小而放出;氧化钙吸水,促使氨放出;生成的氢氧化钙电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出.
故答案为:氧化钙溶于水放出大量热,温度升高,使氨的溶解度减小而放出;氧化钙吸水,促使氨放出;生成的氢氧化钙电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出;
(5)Y的单质(N2)与Z的单质(H2)生成C(NH3)的反应是可逆反应,△H<0,反应为:N2+3H2
2NH3;,△H<0;
a、化学平衡的标志是正逆反应速率相同,故a正确;
b、将等物质的量的Y(N2)、Z(H2)的单质充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应,设起始量都为1mol,则
N2+3H2
2NH3
起始量 1 1 0
变化量 x 3x 2x
平衡量 1-x 1-3x 2x
所以氮气所占体积分数为物质的量的百分数=
×100%=50%,所以Y(N2)的单质的体积分数始终为50%,故b正确;
c、达到化学平衡时,Y(N2)的单质的体积分数始终为50%,H2和NH3共占50%,所以两种单质在混合气体中的物质的量之比不为1:1,故c错误;
d、达到化学平衡的过程中,气体质量不变,气体物质的量减小,所以混合气体平均相对分子质量增大,故d错误;
e、到化学平衡后,再升高温度,反应是放热反应,平衡逆向进行,C(NH3)的体积分数减小.故e错误;
综上所述ab正确;
故答案为:ab.
(6)X为氧元素,Z为氢元素,W为碳元素,三种元素形成化合物C2H6O,其蒸汽通过灼热的氧化铜,黑色的氧化铜会逐渐变红,则该化合物为乙醇CH3CH2OH,该反应的化学方程式为
CH3CH2OH+CuO
CH2CHO+Cu+H2O,故答案为:CH3CH2OH+CuO
CH2CHO+Cu+H2O;
即X为氧元素,Y为氮元素,Z为氢元素,W为碳元素;A为NO,B为H2O,C为NH3.
(1)X为氧元素,原子核外有8个电子,有2个电子层,最外层电子数为6各电子,处于周期表中第2周期第ⅥA族.故答案为:第2周期第ⅥA族;
(2)C为NH3,A为NO,氨气在催化剂并加热的条件下生成一氧化氮与水,反应方程式为4NH3+5O2
| ||
| △ |
故答案为:4NH3+5O2
| ||
| △ |
(3)常温下,将C(NH3)通入元素Y(N)的最高价氧化物的水化物的水溶液HNO3中,Y为氮元素,最高价氧化物的水化物为HNO3,氨气与硝酸反应生成硝酸铵,得到pH=5的溶液,反应后的溶液存在的平衡体系有:NH4++H2O?NH3?H2O+H+;H2O?OH-+H+;硝酸铵属于强酸弱碱盐,铵根离子水解,溶液呈酸性,所以 c(NO3-)>c(NH4+),c(H+)>c(OH-);
故答案为:NH4++H2O?NH3?H2O+H+;H2O?OH-+H+; c(NO3-)>c(NH4+)>c(H+)>c(OH-);
(4)实验室里为制取C(NH3),常在C的浓溶液中加入生石灰.氧化钙溶于水放出大量热,温度升高,使氨的溶解度减小而放出;氧化钙吸水,促使氨放出;生成的氢氧化钙电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出.
故答案为:氧化钙溶于水放出大量热,温度升高,使氨的溶解度减小而放出;氧化钙吸水,促使氨放出;生成的氢氧化钙电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出;
(5)Y的单质(N2)与Z的单质(H2)生成C(NH3)的反应是可逆反应,△H<0,反应为:N2+3H2
| ||
| 高温高压 |
a、化学平衡的标志是正逆反应速率相同,故a正确;
b、将等物质的量的Y(N2)、Z(H2)的单质充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应,设起始量都为1mol,则
N2+3H2
| ||
| 高温高压 |
起始量 1 1 0
变化量 x 3x 2x
平衡量 1-x 1-3x 2x
所以氮气所占体积分数为物质的量的百分数=
| 1-x |
| 2-2x |
c、达到化学平衡时,Y(N2)的单质的体积分数始终为50%,H2和NH3共占50%,所以两种单质在混合气体中的物质的量之比不为1:1,故c错误;
d、达到化学平衡的过程中,气体质量不变,气体物质的量减小,所以混合气体平均相对分子质量增大,故d错误;
e、到化学平衡后,再升高温度,反应是放热反应,平衡逆向进行,C(NH3)的体积分数减小.故e错误;
综上所述ab正确;
故答案为:ab.
(6)X为氧元素,Z为氢元素,W为碳元素,三种元素形成化合物C2H6O,其蒸汽通过灼热的氧化铜,黑色的氧化铜会逐渐变红,则该化合物为乙醇CH3CH2OH,该反应的化学方程式为
CH3CH2OH+CuO
| 加热 |
| 加热 |
点评:本题考查元素位置结构性质的相互关系的推断,物质转化关系和物质性质的应用,化学平衡的影响条件分析判断,题目难度中等,本题注意解答该题的突破口为X、Y、Z三种短周期元素,它们的原子序数之和为16,一个B分子中含有的Z原子个数比C分子中少1个,元素化合物推断、常用化学用语、盐类水解等,难度中等,元素与物质推断是关键,答题时注意体会.

练习册系列答案
相关题目
 X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:
X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化: