摘要:有甲.乙.丙.丁.戊物种元素.甲.乙.丙为依次相邻的第三周期元素.乙.丁.戊为同一主族元素.五种元素原子序数之和为85.则乙元素为 元素.它在周期表中位置为 .
网址:http://m.1010jiajiao.com/timu3_id_154939[举报]
 甲、乙、丙、丁、戊是五种短周期元素,其原子序数依次增大,它们可以组成下列框图所有物质.甲与乙、丙与乙均可形成原子个数比为2:1和1:1的化合物,丁元素原子的最外层电子数是其电子层数的2倍,框图中溶液M为黄绿色.在一定条件下,下列各物质可发生如图所示的变化.试回答:
甲、乙、丙、丁、戊是五种短周期元素,其原子序数依次增大,它们可以组成下列框图所有物质.甲与乙、丙与乙均可形成原子个数比为2:1和1:1的化合物,丁元素原子的最外层电子数是其电子层数的2倍,框图中溶液M为黄绿色.在一定条件下,下列各物质可发生如图所示的变化.试回答:(1)戊元素的原子结构示意图为


(2)A的电子式为


(3)工业上由F制备H的条件是
常压、催化剂(或V2O5)、500℃左右(高温)
常压、催化剂(或V2O5)、500℃左右(高温)
(4)反应(Ⅰ)的离子方程式为
2OH-+SO2═SO32-+H2O
2OH-+SO2═SO32-+H2O
.(5)反应(Ⅱ)的化学方程式为
SO2+Cl2+2H2O=H2SO4+2HCl
SO2+Cl2+2H2O=H2SO4+2HCl
.甲、乙、丙、丁、戊为短周期原子序数依次增大的五种主族元素.乙、戊同主族,甲与乙的原子序数之和等于戊的原子序数.丙是短周期主族元素中原子半径最大的元素,丁元素在地壳中含量居金属元素的第一位.下列说法正确的是( )
| A、简单离子半径:丁>丙>乙>甲 | B、气态氢化物的稳定性:甲>乙 | C、甲与丙形成的化合物仅有一种 | D、丙、丁、戊的最高价氧化物对应的水化物之间两两均能反应 |
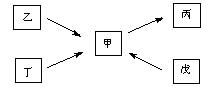 甲 、乙、丙、丁、戊均为中学化学常见的单质或化合物,且均含有同一种元素R,在一定条件下其转化关系如右图所示。
甲 、乙、丙、丁、戊均为中学化学常见的单质或化合物,且均含有同一种元素R,在一定条件下其转化关系如右图所示。
(1)若R为一种非金属元素,且上述五种物质含有不同的官能团,丁为带水果香味的液体,乙和丁均能在碱性条件下生成甲,戊是一种无色气体,相同条件下相对H2的密度为14,则由甲在一定条件下生成戊的化学方程式为 ,欲检验乙中官能团,所选用的试剂为(填序号) 。
① NaOH溶液 ② Br2的CCl4溶液 ③银氨溶液 ④ AgNO3溶液 ⑤ 稀HNO3
(2)若R为另一种非金属元素,甲与丙为常见大气污染物,且甲与丙的相对分子质量相差16。乙在常温下为气体,丁为空气的主要成分之一。则丁的电子式为 ,乙的空间构型为 ;戊的稀溶液能跟过量铁粉反应,其离子方程式为 。
(3)若R为一种金属元素,乙由两种元素组成,甲溶液的pH小于7,单质丁在一定条件下可生成戊。甲与戊两种溶液混合生成沉淀丙的离子方程式为 ,除去镁粉中混有少量的丁,涉及的离子方程式为 。
查看习题详情和答案>>甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙均为单质,它们的转化关系如下
图所示(某些条件和部分产物已略去)。下列说法不正确的是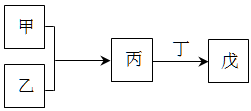
| A.若甲既能与盐酸反应又能与NaOH溶液反应,则丙可能属于两性氧化物 |
| B.若甲为短周期中原子半径最大的主族元素的单质,且戊为碱,则丙只能为Na2O2 |
| C.若丙、丁混合产生白烟,且丙为18电子分子,丁为10电子分子,则乙的水溶液可能具有漂白作用 |
| D.若甲、丙、戊含有同一种元素,则三种物质中该元素的化合价由低到高的顺序可能为:甲 < 丙 < 戊 |
 甲、乙、丙、丁、戊是中学化学常见的无机物,其中甲、乙均为单质,它们的转化关系如图所示(某些条中和部分产物已略去).
甲、乙、丙、丁、戊是中学化学常见的无机物,其中甲、乙均为单质,它们的转化关系如图所示(某些条中和部分产物已略去).