摘要: 工业制粗硅
网址:http://m.1010jiajiao.com/timu3_id_154564[举报]
工业由粗硅制取纯硅有以下反应:
①Si(s) + 3 HCl(g)![]() SiHCl3(g) + H2(g);△H = -318 kJ·mol-l
SiHCl3(g) + H2(g);△H = -318 kJ·mol-l
②SiHCl3(g) + H2(g)![]() Si(s) + 3 HCl(g);
Si(s) + 3 HCl(g);
下列关于上述反应的说法中不正确的是
A.反应①、②均为氧化还原反应
B.反应①、②均为置换反应
C.若反应①放热,则反应②一定吸热
D.欲提高SiHCl3产率,可减压或升温
查看习题详情和答案>>工业上用“三氯氢硅还原法”,提纯粗硅的工艺流程如图所示:
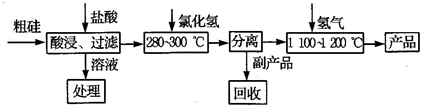
(1)三氯氢硅的制备原理:Si(s)+3HCl(g)?SiHCl3(g)+H2(g)△H=-210kJ/mol
工业上为了加快SiHCl的生成速率而又不降低硅的转化率,可以采用的方法是
(2)除上述反应外,还伴随着副反应:Si(s)+4HCl(g)?SiCl4(g)+2H2(g)△H=-241kJ/mol.已知:SiHCl、SiCl4常温下均为液体.
①工业上分离SiHCl、SiCl4的操作方法为
②反应SiHCl3(g)+HCl(g)?SiCl4(g)+H2(g)的△H=
(3)该生产工艺中可以循环使用的物质是
查看习题详情和答案>>

(1)三氯氢硅的制备原理:Si(s)+3HCl(g)?SiHCl3(g)+H2(g)△H=-210kJ/mol
工业上为了加快SiHCl的生成速率而又不降低硅的转化率,可以采用的方法是
升高温度或增大氢气与SiHCl3的物质的量之比或增大氢气浓度;
升高温度或增大氢气与SiHCl3的物质的量之比或增大氢气浓度;
.(2)除上述反应外,还伴随着副反应:Si(s)+4HCl(g)?SiCl4(g)+2H2(g)△H=-241kJ/mol.已知:SiHCl、SiCl4常温下均为液体.
①工业上分离SiHCl、SiCl4的操作方法为
蒸馏
蒸馏
.②反应SiHCl3(g)+HCl(g)?SiCl4(g)+H2(g)的△H=
-31
-31
kJ/mol.(3)该生产工艺中可以循环使用的物质是
氯化氢、氢气
氯化氢、氢气
(填物质名称). Si+2CO↑,在这个氧化还原反应中,氧化剂和还原剂的物质的量之比是
Si+2CO↑,在这个氧化还原反应中,氧化剂和还原剂的物质的量之比是