摘要: 主族元素A有1个价电子.主族元素B的最高价与最低价的绝对值相等.它们形成化合物的化学式是 A. AB3 B. BA4 C. A2B D. B2A3
网址:http://m.1010jiajiao.com/timu3_id_152210[举报]
主族元素A、B、C、D的原子序数都小于18,A与D同主族,B与C在同一周期,A、D原子的最外层电子数都是1,C原子最外层电子数比B原子少2个,且C最外层电子数是次外层电子数的2倍.A、B单质在常温下均为气体,它们在高温下以体积比2:1完全反应,生成物在常温下是液体.此液体与D单质能激烈反应生成A的单质.所得溶液滴入酚酞显红色,同时溶液中含有与氖原子的电子层结构相同的阳离子.回答下列问题:
(1)写出元素符号A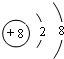
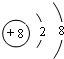 ;写出C元素在周期表中的位置第
;写出C元素在周期表中的位置第
(2)写出C在足量B中充分反应后生成物的电子式
 ,结构式
,结构式
(3)写出B、D在加热条件下形成化合物的电子式
 ,判断其中的化学键的类型
,判断其中的化学键的类型
 .
.
(4)写出一种有A、B、C、D组成的化合物的化学式
查看习题详情和答案>>
(1)写出元素符号A
H
H
,DNa
Na
.写出B阴离子结构示意图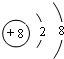
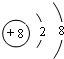
四
四
周期ⅣA
ⅣA
族;(2)写出C在足量B中充分反应后生成物的电子式


O=C=O
O=C=O
.(3)写出B、D在加热条件下形成化合物的电子式


离子键、共价键
离子键、共价键
.用电子式表示B、D在不加热条件下形成化合物的形成过程:

(4)写出一种有A、B、C、D组成的化合物的化学式
NaHCO3
NaHCO3
.元素A~G是元素周期表中的7种短周期元素,请根据表中信息回答下列问题:
(1)上表中与B元素同周期的元素符号是
(2)写出D离子的结构示意图
 .
.
(3)写出C单质与水反应的化学方程式
(4)写出G与烧碱溶液反应的离子方程式
(5)写出F元素常见的两种同素异形体的名称
(6)对元素B的单质或化合物描述正确的是(填序号)
①B元素的最高正价为+6 ②常温常压下,其单质很难与其他物质反应
③单质分子中含有18个电子 ④其氢化物极易溶于水
(7)C、E和F 三种元素的氢化物中,沸点最高的氢化物的化学式是
(8)A和D 两元素金属性较强的是(填元素符号)
查看习题详情和答案>>
| 元素 | A | B | C | D | E | F | G |
| 性 质 结 构 信 息 |
制成的高压灯,发出的黄光透雾能力强、射程远. | 工业上通过分离液态空气获得其单质.原子的最外层未达稳定结构. | 常温常压下是气体,元素的常见化合价为-1及多种正价. | +2价阳离子核外电子数与氖原子相同. | E和F是同主族元素,都有同素异形体.E的一种分子与F原子电子数目相同. | 常温下,其单质能与烧碱溶液反应放出气体,其氧化物能与强酸或强碱溶液反应. | |
N
N
.(2)写出D离子的结构示意图


(3)写出C单质与水反应的化学方程式
Cl2+H2O=HClO+HCl
Cl2+H2O=HClO+HCl
.(4)写出G与烧碱溶液反应的离子方程式
2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑
2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑
.(5)写出F元素常见的两种同素异形体的名称
斜方硫、单斜硫
斜方硫、单斜硫
.(6)对元素B的单质或化合物描述正确的是(填序号)
②④
②④
.①B元素的最高正价为+6 ②常温常压下,其单质很难与其他物质反应
③单质分子中含有18个电子 ④其氢化物极易溶于水
(7)C、E和F 三种元素的氢化物中,沸点最高的氢化物的化学式是
H2O
H2O
;C和F 两元素的氢化物中,还原性较强的是(填名称)硫化氢
硫化氢
.(8)A和D 两元素金属性较强的是(填元素符号)
Na
Na
.写出能证明该结论的一个实验事实Na与水反应比Mg与水反应剧烈或氢氧化钠的碱性比氢氧化镁强
Na与水反应比Mg与水反应剧烈或氢氧化钠的碱性比氢氧化镁强
.主族元素A、B、C、D、E的原子序数都小于18,A与D同主族,B与C在同一周期,A、D原子的最外层电子数都是1,C原子最外层电子数比B原子少2个,且C最外层电子数是次外层电子数的2倍.A、B单质在常温下均为气体,它们在一定条件下以体积比2:1完全反应,生成物在常温下是液体F.此液体与D单质能激烈反应生成A的单质,所得溶液滴入酚酞显红色,同时溶液中含有与氖原子的电子层结构相同的阳离子.E的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水.回答下列问题:
(1)写出元素符号A ,C .
(2)E元素的最高价氧化物和盐酸反应的离子方程式为: .
(3)用电子式表示F的形成过程 .在加热的条件下B、D形成的化合物的电子式为 ,其中的化学键的类型为 .
(4)写出一种有A、B、C、D组成的化合物的化学式 .
(5)B的气态氢化物是天然气的主要成分,它的空间结构为 .
查看习题详情和答案>>
(1)写出元素符号A
(2)E元素的最高价氧化物和盐酸反应的离子方程式为:
(3)用电子式表示F的形成过程
(4)写出一种有A、B、C、D组成的化合物的化学式
(5)B的气态氢化物是天然气的主要成分,它的空间结构为
元素A、B、C、D、E、F的原子序数依次增大,前五种元素为短周期元素,F元素为第四周期元素,且D、F为常见金属元素.A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g?L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(其它参与反应的物质未列出):

其中,均含D元素的乙(金属阳离子)、丙、丁微粒间的转化全为非氧化还原反应;均含F元素的乙、丙、丁微粒间的转化全为氧化还原反应;无论是含有D元素还是含有F元素,相邻的乙与丙或丙与丁两两间互不发生化学反应.请回答下列问题:
(1)写出化合物甲的电子式: .
(2)写出化合物甲的水溶液与D元素对应的金属阳离子反应的离子方程式 ;写出均含有F元素的乙与丁在溶液中发生反应的离子方程式 .
(3)复盐是指由2种或2种以上阳离子和一种阴离子组成的盐.请写出由A、B、C、E、F元素组成的一种具有还原性的复盐戊的化学式 .化合物己是制备复盐戊的必须物质之一,工业上常用氧气、水和FE2来制取,并得到E的高价态化合物,请写出工业上由FE2制取化合物己的化学方程式 .
(4)EC2是啤酒中含量较低而又重要的组分,大部分是在发酵过程中产生的,是啤酒内源抗氧化物的一种,它的存在量与啤酒的抗氧化性有很大的关系.图2是某啤酒样品不同时间段总EC2的变化情况,请运用所学的知识解释啤酒样品中总EC2随时间变化的主要原因是 .
(5)由A、C元素组成化合物庚和A、E元素组成的化合物辛,式量均为34.其中庚的熔沸点高于辛,其原因是: .
查看习题详情和答案>>

其中,均含D元素的乙(金属阳离子)、丙、丁微粒间的转化全为非氧化还原反应;均含F元素的乙、丙、丁微粒间的转化全为氧化还原反应;无论是含有D元素还是含有F元素,相邻的乙与丙或丙与丁两两间互不发生化学反应.请回答下列问题:
(1)写出化合物甲的电子式:
(2)写出化合物甲的水溶液与D元素对应的金属阳离子反应的离子方程式
(3)复盐是指由2种或2种以上阳离子和一种阴离子组成的盐.请写出由A、B、C、E、F元素组成的一种具有还原性的复盐戊的化学式
(4)EC2是啤酒中含量较低而又重要的组分,大部分是在发酵过程中产生的,是啤酒内源抗氧化物的一种,它的存在量与啤酒的抗氧化性有很大的关系.图2是某啤酒样品不同时间段总EC2的变化情况,请运用所学的知识解释啤酒样品中总EC2随时间变化的主要原因是
(5)由A、C元素组成化合物庚和A、E元素组成的化合物辛,式量均为34.其中庚的熔沸点高于辛,其原因是: