摘要: 0.8gA的单质与稀盐酸充分反应放出0.04g H2.B元素的阴离子结构与氩原子相同.B的气态氢化物的水溶液是强酸. ⑴求A的相对原子质量及化合价, ⑵写出A.B两元素的符号及B的气态氢化物的化学式, ⑶写出由A.B组成的化合物与Na2CO3溶液反应的离子方程式. 附加题:原子序数为1-20号元素中.某两种元素的原子序数相差3.电子层数相差1.它们形成化合物时原子数之比为1:2.试写出这些化合物的化学式.
网址:http://m.1010jiajiao.com/timu3_id_152030[举报]
几种短周期元素的原子半径及主要化合价见下表:下列说法正确的是( )
| 元素代号 | a | b | c | d | e |
| 原子半径/nm | 0.089 | 0.074 | 0.160 | 0.143 | 0.102 |
| 主要化合价 | +2 | -2 | +2 | +3 | +6,-2 |
查看习题详情和答案>>
(2009?朝阳区一模)有关元素A、B、C、D的信息如下:
请回答下列问题:
(1)用C单质来焊接钢轨的化学方程式是
(2)有关C与D元素,下列说法正确的是
①C或D的高价盐均可用做净水剂
②用C或D单质做成的槽车,都可用来运输甲的稀溶液
③C、D的单质与稀硫酸组成的原电池,C电极发生氧化反应
④C的合金可用来做车船材料和门窗等
(3)B的一种氢化物在碱性溶液中可与丙反应,生成物中A元素只显其最高价态,该反应的离子方程式是
(4)现取1mol/L 100mL的C的氯化物溶液,向其中加入1mol/L氢氧化钠溶液产生了3.9g的沉淀,则加入的氢氧化钠溶液体积可能是
(5)已知:2AB2(g) A2B4(g);△H<0.在恒温恒容条件下,将一定量AB2和A2B4的混合气体通入容积为2L的密闭
A2B4(g);△H<0.在恒温恒容条件下,将一定量AB2和A2B4的混合气体通入容积为2L的密闭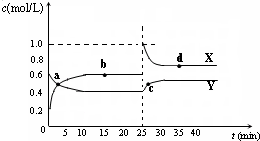 容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
①a、b、c、d四个点中,化学反应处于平衡状态的是
②25min时,增加了
③a、b、c、d四个点中所表示的反应体系中,气体颜色由深到浅的顺序是
查看习题详情和答案>>
| 元 素 | 有关信息 |
| A | 最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐 |
| B | 地壳中含量最高的元素,A与B可形成一种质量比为 7:12的化合物(丙) |
| C | 单质曾用于焊接钢轨 |
| D | 单质是生活中常见金属,其制品在自然环境中被腐蚀呈现红棕色 |
(1)用C单质来焊接钢轨的化学方程式是
Fe2O3+2Al
Al 2O3+2Fe
| ||
Fe2O3+2Al
Al 2O3+2Fe
.
| ||
(2)有关C与D元素,下列说法正确的是
①③④
①③④
(填序号).①C或D的高价盐均可用做净水剂
②用C或D单质做成的槽车,都可用来运输甲的稀溶液
③C、D的单质与稀硫酸组成的原电池,C电极发生氧化反应
④C的合金可用来做车船材料和门窗等
(3)B的一种氢化物在碱性溶液中可与丙反应,生成物中A元素只显其最高价态,该反应的离子方程式是
N2O3+2OH-+2H2O2=2NO3-+3H2O
N2O3+2OH-+2H2O2=2NO3-+3H2O
.(4)现取1mol/L 100mL的C的氯化物溶液,向其中加入1mol/L氢氧化钠溶液产生了3.9g的沉淀,则加入的氢氧化钠溶液体积可能是
150或350
150或350
mL.(5)已知:2AB2(g)
 容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.①a、b、c、d四个点中,化学反应处于平衡状态的是
b、d
b、d
点.②25min时,增加了
NO2
NO2
(填物质的化学式)0.8
0.8
mol.③a、b、c、d四个点中所表示的反应体系中,气体颜色由深到浅的顺序是
cdba
cdba
(填字母).几种短周期元素的原子半径及主要化合价如表所示:
|
查看习题详情和答案>>
(2013?长春一模)下表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是( )
|
查看习题详情和答案>>
(2010?宝鸡三模)几种短周期元素的原子半径及主要化合价见下表,下列叙述错误的是( )
|
查看习题详情和答案>>