摘要:21.(1)未用玻璃棒引流,未采用150 mL容量瓶. (2)砝码放在左盘.烧杯放在右盘(或砝码和物品的位置放反了),27.4g. (3)A.滴管口伸人试管中 B.试管口向上 C.混合气体从短导管进入洗气瓶
网址:http://m.1010jiajiao.com/timu3_id_150686[举报]
 为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):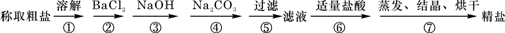
(1)第⑤步实验操作需要烧杯、
漏斗
漏斗
、玻璃棒
玻璃棒
等玻璃仪器.(2)步骤2中,判断加入BaCl2已过量的方法是:
在②步后的上层清液中,再滴入氯化钡溶液,若溶液未变浑浊,则说明所加的氯化钡已过量
在②步后的上层清液中,再滴入氯化钡溶液,若溶液未变浑浊,则说明所加的氯化钡已过量
(3)除杂试剂BaCl2、NaOH、Na2CO3、加入的顺序还可以是(用化学式回答)
NaOH、BaCl2、Na2CO3或BaCl2、NaOH、Na2CO3
NaOH、BaCl2、Na2CO3或BaCl2、NaOH、Na2CO3
.(4)若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是
在此酸度条件下,会有部分沉淀溶解,影响精盐的纯度
在此酸度条件下,会有部分沉淀溶解,影响精盐的纯度
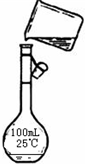
.(5)为检验精盐纯度,需配制200mL 1mol/L NaCl(精盐)溶液,如图是该同学转移溶液的示意图,图中的错误是:
未用玻璃棒引流,未使用200mL的容量瓶
未用玻璃棒引流,未使用200mL的容量瓶
(6)配制过程中,下列操作情况会使结果偏低的是
AD
AD
A.称量时,托盘天平左盘加砝码,右盘加氯化钠
B.移液前,容量瓶中有少量蒸馏水未倒出
C.定容时,俯视容量瓶刻度线观察液面
D.定容后,倒置容量瓶摇匀经平放静置,液面低于刻度线,再加水定容.
某同学用胆矾固体(CuSO4?5H2O )配制0.30mol/L的CuSO4溶液100mL,回答下列问题
(1)所需仪器为:容量瓶、托盘天平、药匙、胶头滴管,还需要那些玻璃仪器才能完成该实验,请写出:
(2)请写出该实验的简要的实验步骤:
①计算 ②称量胆矾
③
(3)称量的操作顺序为(填序号)
A、调天平零点 B、游码回零
C、向小烧杯中加入碳酸钠 D、称量空烧杯
E、向右盘加砝码并把游码移到所需位置 F、将砝码回盒
G、记录称量结果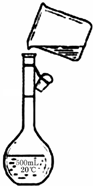
(4)如图是该同学转移溶液的操作示意图,图中的错误是:
(5)下列操作会使所配溶液的浓度偏高的是
A、称量时所用砝码已生锈
B、往容量瓶转移溶液时,有少量液体溅出
C、胆矾已失去部分结晶水
D、未洗涤溶解胆矾的烧杯
E、定容时,俯视刻度线
F、小烧杯洗净后未干燥即用来称量
G、容量瓶未干燥即用来配制溶液
H、该同学在定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度.
查看习题详情和答案>>
(1)所需仪器为:容量瓶、托盘天平、药匙、胶头滴管,还需要那些玻璃仪器才能完成该实验,请写出:
烧杯、玻璃棒
烧杯、玻璃棒
.(2)请写出该实验的简要的实验步骤:
①计算 ②称量胆矾
7.5
7.5
g③
溶解
溶解
④转移 ⑤洗涤并转移 ⑥定容 ⑦摇匀(3)称量的操作顺序为(填序号)
BADGECF
BADGECF
.A、调天平零点 B、游码回零
C、向小烧杯中加入碳酸钠 D、称量空烧杯
E、向右盘加砝码并把游码移到所需位置 F、将砝码回盒
G、记录称量结果

(4)如图是该同学转移溶液的操作示意图,图中的错误是:
未用玻璃棒引流; 未采用100 mL容量瓶
未用玻璃棒引流; 未采用100 mL容量瓶
.(5)下列操作会使所配溶液的浓度偏高的是
ACE
ACE
.A、称量时所用砝码已生锈
B、往容量瓶转移溶液时,有少量液体溅出
C、胆矾已失去部分结晶水
D、未洗涤溶解胆矾的烧杯
E、定容时,俯视刻度线
F、小烧杯洗净后未干燥即用来称量
G、容量瓶未干燥即用来配制溶液
H、该同学在定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度.
 为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):称取粗盐
| ||
| ① |
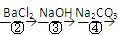
| ||
| ⑤ |
| ||
| ⑥ |
| ||
| ⑦ |
(1)判断BaCl2已过量的方法是
取第②步后的上层清液(或取少量上层清液于试管中),再滴入适量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量
取第②步后的上层清液(或取少量上层清液于试管中),再滴入适量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量
.(2)第④步中,相关的离子方程式是
Ca2++CO32-=CaCO3↓
Ca2++CO32-=CaCO3↓
;Ba2++CO32-=BaCO3↓
Ba2++CO32-=BaCO3↓
.(3)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是
在此酸度条件下,会有部分沉淀溶解,从而影响制得精盐的纯度
在此酸度条件下,会有部分沉淀溶解,从而影响制得精盐的纯度
.(4)为检验精盐纯度,需配制150mL 0.2mol?L-1NaCl(精盐)溶液,右图是该同学转移溶液的示意图,图中的错误是
未用玻璃棒引流,未采用150mL容量瓶
未用玻璃棒引流,未采用150mL容量瓶
.海水中蕴藏着丰富的资源.海水综合利用的流程图如图1.

(1)为检验精盐纯度,需配制250mL 0.2mol/L NaCl(精盐)溶液,图2是该同学转移溶液的示意图,图中有两点错误请指出:
(2)用NaCl做原料可以得到多种产品.
实验室用惰性电极电解100mL 0.1mol/LNaCl溶液,若阴阳两极均得到112mL气体(标准状况,假设气体物质全部从溶液中逸出),则所得溶液的pH为
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上.在这种工艺设计中,相关物料的传输与转化关系如图3所示,其中的电极未标出,所用的离子膜都只允许阳离子通过.

①图中X、Y分别是
(4)图4欲实现Cu+H2SO4═CuSO4+H2,在你认为能实现该转化的装置中的括号内,标出电极材料(填“Cu”或“C”).
查看习题详情和答案>>

(1)为检验精盐纯度,需配制250mL 0.2mol/L NaCl(精盐)溶液,图2是该同学转移溶液的示意图,图中有两点错误请指出:
未用玻璃棒引流;未采用250mL容量瓶
未用玻璃棒引流;未采用250mL容量瓶
(2)用NaCl做原料可以得到多种产品.
实验室用惰性电极电解100mL 0.1mol/LNaCl溶液,若阴阳两极均得到112mL气体(标准状况,假设气体物质全部从溶液中逸出),则所得溶液的pH为
13
13
(忽略反应前后溶液的体积变化).(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上.在这种工艺设计中,相关物料的传输与转化关系如图3所示,其中的电极未标出,所用的离子膜都只允许阳离子通过.

①图中X、Y分别是
Cl2
Cl2
、H2
H2
(填化学式),②写出燃料电池B中正极发生的电极反应O2+4e-+2H2O=4OH-
O2+4e-+2H2O=4OH-
;(4)图4欲实现Cu+H2SO4═CuSO4+H2,在你认为能实现该转化的装置中的括号内,标出电极材料(填“Cu”或“C”).
粗食盐常含有少量Ca2+、Mg2+、SO42-以及泥沙等杂质,实验室提纯NaCl的流程如下(加入的试剂稍过量)

(1)判断BaCl2已过量的方法是
(2)步骤③中加入的试剂A是
(3)步骤④中,相关的离子方程式
(4)若将步骤⑤与步骤⑥对调,先用盐酸调pH再过滤,将对实验结果产生的影响是
(5)用提纯的NaCl配制100mL 1.0mol/L的NaCl溶液,所用仪器除烧杯、玻璃棒、胶头滴管、药匙外,还需要
(6)实验室提纯NaCl的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,其中在蒸发时,使用玻璃棒的目的
(7)为检验精盐纯度,需配制250mL 0.2mol/L NaCl(精盐)溶液,题图是该同学转移溶液的示意图,图中的错误是
查看习题详情和答案>>

(1)判断BaCl2已过量的方法是
取第②步后的上层清液1~2滴于滴定板上(或取少量上层清液于试管中),再滴入1~2滴BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量
取第②步后的上层清液1~2滴于滴定板上(或取少量上层清液于试管中),再滴入1~2滴BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量
(2)步骤③中加入的试剂A是
NaOH
NaOH
(填化学式).(3)步骤④中,相关的离子方程式
Ca2++CO32-=CaCO3↓; Ba2++CO32-=BaCO3↓
Ca2++CO32-=CaCO3↓; Ba2++CO32-=BaCO3↓
(4)若将步骤⑤与步骤⑥对调,先用盐酸调pH再过滤,将对实验结果产生的影响是
先加HCl会有少量CaCO3、BaCO3、Mg(OH)2沉淀溶解,使NaCl混有杂质,从而影响制得NaCl的纯度
先加HCl会有少量CaCO3、BaCO3、Mg(OH)2沉淀溶解,使NaCl混有杂质,从而影响制得NaCl的纯度
(5)用提纯的NaCl配制100mL 1.0mol/L的NaCl溶液,所用仪器除烧杯、玻璃棒、胶头滴管、药匙外,还需要
100mL容量瓶、托盘天平
100mL容量瓶、托盘天平
(填仪器名称).(6)实验室提纯NaCl的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,其中在蒸发时,使用玻璃棒的目的
防止局部过热液滴或晶体飞溅
防止局部过热液滴或晶体飞溅
.
(7)为检验精盐纯度,需配制250mL 0.2mol/L NaCl(精盐)溶液,题图是该同学转移溶液的示意图,图中的错误是
未用玻璃棒引流;未采用250 mL容量瓶
未用玻璃棒引流;未采用250 mL容量瓶
.