网址:http://m.1010jiajiao.com/timu3_id_149682[举报]
(1)属于非金属元素但又具有一定的金属性,可作半导体材料的是
(2)甲、乙两种元素是同一周期的相邻元素,甲元素是形成有机物的主要元素,乙元素的L层上有5个电子.甲、乙元素可形成硬度大于金刚石的一种化合物,该化合物属于
(3)把去除了表面氧化膜的铝条浸入硝酸汞溶液,片刻后取出,放置一段时间后,可看到铝条表面生成白色毛状物,生成该物质的化学方程式为
美国化学家发现铝的“原子群”(如Al13、Al14、Al37)各具有与某种元素相似的化学性质,并符合元素周期律的某些规律.例如:Al13与卤素具有相似的化学性质,Al
- 13 |
 (2009?上海)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.
(2009?上海)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.(1)在光照条件下.氯气和氢气反应过程如下:
①Cl2→Cl+Cl ②Cl+H2→HCl+H ③H+Cl2→HCl+Cl …
反应②中形成的化合物的电子式为


(2)在短周期主族元素中,氯元素及与其相邻元素的原予半径从大到小的顺序是
(用元素符号表示).与氯元素同周期且金属性最强的元素位于周期表的第
(3)卤索单质及化合物在许多性质上都存在着递变规律.下列有关说法正确的是
a.卤化银的颜色按AgCl、AgBr、AgI的顺序依次加深
b?卤化氢的键长按H-F、H-Cl、H-Br、H-I的顺序依次减小
c?卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d?卤索单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
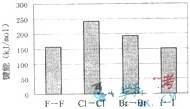
(4)卤素单质的键能大小如图.由图推断:
①非金属性强的卤素,其单质分子的化学键
②卤素单质键能大小与键长的关系为:
(8分)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。
(1)在光照条件下,氯气和氢气反应过程如下:①Cl2→Cl+Cl ②Cl+H2→HCl+H ③H+Cl2→HCl+Cl ……反应②中形成的化合物的 电子式为 ;反应③中被破坏的化学键属
电子式为 ;反应③中被破坏的化学键属 于 键(填“极性”或“非极性”)。
于 键(填“极性”或“非极性”)。
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是 (用元素符号表示)。与氯元素同周期且金属性最强的元素 位于周期表的第
位于周期表的第  周期 族。
周期 族。
( 3)卤素单质及化
3)卤素单质及化 合物在许多性质上都存在着递变规律。下列有关说法正确的是 。
合物在许多性质上都存在着递变规律。下列有关说法正确的是 。
a.卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深
b.卤化氢的键长按H—F、H—C1、H—Br、H—I的顺序依次减小
c.卤化 氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
(1)在光照条件下,氯气和氢气反应过程如下:
①Cl2![]() Cl+Cl ②Cl+H2
Cl+Cl ②Cl+H2![]() HCl+H ③H+Cl2
HCl+H ③H+Cl2![]() HCl+Cl……
HCl+Cl……
反应②中形成的化合物的电子式为__________________;反应③中被破坏的化学键属于__________________键(填“极性”或“非极性”)。
(2)在短周期主族元素中,氯元素及与相邻元素的原子半径从大到小的顺序是__________________ (用元素符号表示)。与氯元素同周期且金属性最强的元素位于周期表的第__________________周期__________________族。
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是__________________。
a.卤化银的颜色按AgCl、AgBr、AgI的顺序依次加深
b.卤化氢的键长按H—F、H—Cl、H—Br、H—I的顺序依次减小
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
(4)卤素单质的键能大小如下图。由图推断:

①非金属性强的卤素,其单质分子的化学键__________________断裂(填“容易”或“不容易”或“不一定容易”)。
②卤素单质键能大小与键长的关系为:__________________。
查看习题详情和答案>>(8分)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。
(1)在光照条件下,氯气和氢气反应过程如下:①Cl2→Cl+Cl ②Cl+H2→HCl+H ③H+Cl2→HCl+Cl ……反应②中形成的化合物的电子式为 ;反应③中被破坏的化学键属于 键(填“极性”或“非极性”)。
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是 (用元素符号表示)。与氯元素同周期且金属性最强的元素位于周期表的第 周期 族。
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是 。
a.卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深
b.卤化氢的键长按H—F、H—C1、H—Br、H—I的顺序依次减小
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
查看习题详情和答案>>