摘要:酸性氧化物一般不与酸反应.而SiO2却能与HF反应, SiO2+ HF=
网址:http://m.1010jiajiao.com/timu3_id_145883[举报]
硫酸亚铁铵的化学式为(NH4)2Fe(SO4)2?6H2O,商品名为摩尔盐.硫酸亚铁可与硫酸铵生成硫酸亚铁铵,一般硫酸亚铁盐在空气中易被氧化,而形成摩尔盐后就比较稳定了.三种盐的溶解度(单位为g/100g水)如下表
实验室欲制备硫酸亚铁铵晶体,设计了如下方案.
(1)完成实验步骤中的填空:
①称取4g铁屑,放入小烧杯,加入15mL10%Na2CO3溶液,小火加热10min以除去
②将处理好的铁屑放入小烧杯,加入15mL 3mol/L H2SO4溶液,水浴加热至不再有气体生成为止,趁热过滤去剩余铁屑,并用少量热水洗涤烧杯及滤纸,并将滤液和洗涤液一起转移到蒸发皿中,则蒸发皿中溶液的溶质为
③加入
(2)回答下列问题:
①硫酸亚铁溶液在空气中易被氧化变质,操作时应注意:a
②加热、浓缩溶液时,不浓缩至干的理由是
③硫酸亚铁和硫酸铵的混合溶液加热浓缩就能得到硫酸亚铁铵晶体,其原因是
④称取两份质量均为1.96g的该硫酸亚铁铵,制成溶液.用未知浓度的KMnO4酸性溶液进行滴定.
Ⅰ) 滴定时,将KMnO4酸性溶液装在
Ⅱ) 已知MnO4-被还原为Mn2+,试写出该滴定过程中的离子方程式:
Ⅲ) 判断该反应到达滴定终点的现象为
Ⅳ) 假设到达滴定终点时,用去V mL KMnO4酸性溶液,则该KMnO4酸性溶液的浓度为
mol/L.
查看习题详情和答案>>
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 70 |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4?7H2O | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| (NH4)2Fe(SO4)2?6H2O | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
(1)完成实验步骤中的填空:
①称取4g铁屑,放入小烧杯,加入15mL10%Na2CO3溶液,小火加热10min以除去
铁屑表面的油污
铁屑表面的油污
,倒掉溶液,用蒸馏水把铁冲洗干净,干燥,备用;②将处理好的铁屑放入小烧杯,加入15mL 3mol/L H2SO4溶液,水浴加热至不再有气体生成为止,趁热过滤去剩余铁屑,并用少量热水洗涤烧杯及滤纸,并将滤液和洗涤液一起转移到蒸发皿中,则蒸发皿中溶液的溶质为
硫酸亚铁
硫酸亚铁
(填名称,不考虑水解),其物质的量约为0.045
0.045
mol;③加入
5.94
5.94
g硫酸铵到蒸发皿中,缓缓加热、浓缩至表面出现结晶膜为止、冷却,得硫酸亚铁铵晶体.(2)回答下列问题:
①硫酸亚铁溶液在空气中易被氧化变质,操作时应注意:a
过滤洗涤操作速度要快
过滤洗涤操作速度要快
;b步骤③要缓缓加热,避免沸腾
步骤③要缓缓加热,避免沸腾
;②加热、浓缩溶液时,不浓缩至干的理由是
因为析出的是硫酸亚铁铵晶体,带有结晶水,蒸干会使晶体分解
因为析出的是硫酸亚铁铵晶体,带有结晶水,蒸干会使晶体分解
;③硫酸亚铁和硫酸铵的混合溶液加热浓缩就能得到硫酸亚铁铵晶体,其原因是
因为相同温度下硫酸亚铁铵晶体在水中的溶解度比硫酸亚铁和硫酸铵的溶解度小
因为相同温度下硫酸亚铁铵晶体在水中的溶解度比硫酸亚铁和硫酸铵的溶解度小
;④称取两份质量均为1.96g的该硫酸亚铁铵,制成溶液.用未知浓度的KMnO4酸性溶液进行滴定.
Ⅰ) 滴定时,将KMnO4酸性溶液装在
酸式
酸式
(酸式或碱式)滴定管,操作时用右
右
手拿锥形瓶;Ⅱ) 已知MnO4-被还原为Mn2+,试写出该滴定过程中的离子方程式:
5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
;Ⅲ) 判断该反应到达滴定终点的现象为
当滴加最后一滴溶液后,溶液变成紫红色,30S内不褪色,说明达到滴定终点
当滴加最后一滴溶液后,溶液变成紫红色,30S内不褪色,说明达到滴定终点
;Ⅳ) 假设到达滴定终点时,用去V mL KMnO4酸性溶液,则该KMnO4酸性溶液的浓度为
| 1 |
| V |
| 1 |
| V |
硫酸亚铁铵的化学式为(NH4)2Fe(SO4)2?6H2O,商品名为摩尔盐.硫酸亚铁可与硫酸铵生成硫酸亚铁铵,一般硫酸亚铁盐在空气中易被氧化,而形成摩尔盐后就比较稳定了.三种盐的溶解度(单位为g/100g水)如下表
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 70 |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4?7H2O | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| (NH4)2Fe(SO4)2?6H2O | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
(1)完成实验步骤中的填空:
①称取4g铁屑,放入小烧杯,加入15mL10%Na2CO3溶液,小火加热10min以除去______,倒掉溶液,用蒸馏水把铁冲洗干净,干燥,备用;
②将处理好的铁屑放入小烧杯,加入15mL 3mol/L H2SO4溶液,水浴加热至不再有气体生成为止,趁热过滤去剩余铁屑,并用少量热水洗涤烧杯及滤纸,并将滤液和洗涤液一起转移到蒸发皿中,则蒸发皿中溶液的溶质为______(填名称,不考虑水解),其物质的量约为______mol;
③加入______g硫酸铵到蒸发皿中,缓缓加热、浓缩至表面出现结晶膜为止、冷却,得硫酸亚铁铵晶体.
(2)回答下列问题:
①硫酸亚铁溶液在空气中易被氧化变质,操作时应注意:a______;b______;
②加热、浓缩溶液时,不浓缩至干的理由是______;
③硫酸亚铁和硫酸铵的混合溶液加热浓缩就能得到硫酸亚铁铵晶体,其原因是______;
④称取两份质量均为1.96g的该硫酸亚铁铵,制成溶液.用未知浓度的KMnO4酸性溶液进行滴定.
Ⅰ) 滴定时,将KMnO4酸性溶液装在______(酸式或碱式)滴定管,操作时用______手拿锥形瓶;
Ⅱ) 已知MnO4-被还原为Mn2+,试写出该滴定过程中的离子方程式:______;
Ⅲ) 判断该反应到达滴定终点的现象为______;
Ⅳ) 假设到达滴定终点时,用去V mL KMnO4酸性溶液,则该KMnO4酸性溶液的浓度为______mol/L. 查看习题详情和答案>>
硫酸亚铁铵的化学式为(NH4)2Fe(SO4)2?6H2O,商品名为摩尔盐.硫酸亚铁可与硫酸铵生成硫酸亚铁铵,一般硫酸亚铁盐在空气中易被氧化,而形成摩尔盐后就比较稳定了.三种盐的溶解度(单位为g/100g水)如下表
实验室欲制备硫酸亚铁铵晶体,设计了如下方案.
(1)完成实验步骤中的填空:
①称取4g铁屑,放入小烧杯,加入15mL10%Na2CO3溶液,小火加热10min以除去______,倒掉溶液,用蒸馏水把铁冲洗干净,干燥,备用;
②将处理好的铁屑放入小烧杯,加入15mL 3mol/L H2SO4溶液,水浴加热至不再有气体生成为止,趁热过滤去剩余铁屑,并用少量热水洗涤烧杯及滤纸,并将滤液和洗涤液一起转移到蒸发皿中,则蒸发皿中溶液的溶质为______(填名称,不考虑水解),其物质的量约为______mol;
③加入______g硫酸铵到蒸发皿中,缓缓加热、浓缩至表面出现结晶膜为止、冷却,得硫酸亚铁铵晶体.
(2)回答下列问题:
①硫酸亚铁溶液在空气中易被氧化变质,操作时应注意:a______;b______;
②加热、浓缩溶液时,不浓缩至干的理由是______;
③硫酸亚铁和硫酸铵的混合溶液加热浓缩就能得到硫酸亚铁铵晶体,其原因是______;
④称取两份质量均为1.96g的该硫酸亚铁铵,制成溶液.用未知浓度的KMnO4酸性溶液进行滴定.
Ⅰ) 滴定时,将KMnO4酸性溶液装在______(酸式或碱式)滴定管,操作时用______手拿锥形瓶;
Ⅱ) 已知MnO4-被还原为Mn2+,试写出该滴定过程中的离子方程式:______;
Ⅲ) 判断该反应到达滴定终点的现象为______;
Ⅳ) 假设到达滴定终点时,用去V mL KMnO4酸性溶液,则该KMnO4酸性溶液的浓度为______mol/L.
查看习题详情和答案>>
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 70 |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4?7H2O | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| (NH4)2Fe(SO4)2?6H2O | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
(1)完成实验步骤中的填空:
①称取4g铁屑,放入小烧杯,加入15mL10%Na2CO3溶液,小火加热10min以除去______,倒掉溶液,用蒸馏水把铁冲洗干净,干燥,备用;
②将处理好的铁屑放入小烧杯,加入15mL 3mol/L H2SO4溶液,水浴加热至不再有气体生成为止,趁热过滤去剩余铁屑,并用少量热水洗涤烧杯及滤纸,并将滤液和洗涤液一起转移到蒸发皿中,则蒸发皿中溶液的溶质为______(填名称,不考虑水解),其物质的量约为______mol;
③加入______g硫酸铵到蒸发皿中,缓缓加热、浓缩至表面出现结晶膜为止、冷却,得硫酸亚铁铵晶体.
(2)回答下列问题:
①硫酸亚铁溶液在空气中易被氧化变质,操作时应注意:a______;b______;
②加热、浓缩溶液时,不浓缩至干的理由是______;
③硫酸亚铁和硫酸铵的混合溶液加热浓缩就能得到硫酸亚铁铵晶体,其原因是______;
④称取两份质量均为1.96g的该硫酸亚铁铵,制成溶液.用未知浓度的KMnO4酸性溶液进行滴定.
Ⅰ) 滴定时,将KMnO4酸性溶液装在______(酸式或碱式)滴定管,操作时用______手拿锥形瓶;
Ⅱ) 已知MnO4-被还原为Mn2+,试写出该滴定过程中的离子方程式:______;
Ⅲ) 判断该反应到达滴定终点的现象为______;
Ⅳ) 假设到达滴定终点时,用去V mL KMnO4酸性溶液,则该KMnO4酸性溶液的浓度为______mol/L.
硫酸亚铁铵的化学式为(NH4)2Fe(SO4)2?6H2O,商品名为摩尔盐.硫酸亚铁可与硫酸铵生成硫酸亚铁铵,一般硫酸亚铁盐在空气中易被氧化,而形成摩尔盐后就比较稳定了.三种盐的溶解度(单位为g/100g水)如下表
实验室欲制备硫酸亚铁铵晶体,设计了如下方案.
(1)完成实验步骤中的填空:
①称取4g铁屑,放入小烧杯,加入15mL10%Na2CO3溶液,小火加热10min以除去______,倒掉溶液,用蒸馏水把铁冲洗干净,干燥,备用;
②将处理好的铁屑放入小烧杯,加入15mL 3mol/L H2SO4溶液,水浴加热至不再有气体生成为止,趁热过滤去剩余铁屑,并用少量热水洗涤烧杯及滤纸,并将滤液和洗涤液一起转移到蒸发皿中,则蒸发皿中溶液的溶质为______(填名称,不考虑水解),其物质的量约为______mol;
③加入______g硫酸铵到蒸发皿中,缓缓加热、浓缩至表面出现结晶膜为止、冷却,得硫酸亚铁铵晶体.
(2)回答下列问题:
①硫酸亚铁溶液在空气中易被氧化变质,操作时应注意:a______;b______;
②加热、浓缩溶液时,不浓缩至干的理由是______;
③硫酸亚铁和硫酸铵的混合溶液加热浓缩就能得到硫酸亚铁铵晶体,其原因是______;
④称取两份质量均为1.96g的该硫酸亚铁铵,制成溶液.用未知浓度的KMnO4酸性溶液进行滴定.
Ⅰ) 滴定时,将KMnO4酸性溶液装在______(酸式或碱式)滴定管,操作时用______手拿锥形瓶;
Ⅱ) 已知MnO4-被还原为Mn2+,试写出该滴定过程中的离子方程式:______;
Ⅲ) 判断该反应到达滴定终点的现象为______;
Ⅳ) 假设到达滴定终点时,用去V mL KMnO4酸性溶液,则该KMnO4酸性溶液的浓度为______mol/L.
查看习题详情和答案>>
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 70 |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4?7H2O | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| (NH4)2Fe(SO4)2?6H2O | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
(1)完成实验步骤中的填空:
①称取4g铁屑,放入小烧杯,加入15mL10%Na2CO3溶液,小火加热10min以除去______,倒掉溶液,用蒸馏水把铁冲洗干净,干燥,备用;
②将处理好的铁屑放入小烧杯,加入15mL 3mol/L H2SO4溶液,水浴加热至不再有气体生成为止,趁热过滤去剩余铁屑,并用少量热水洗涤烧杯及滤纸,并将滤液和洗涤液一起转移到蒸发皿中,则蒸发皿中溶液的溶质为______(填名称,不考虑水解),其物质的量约为______mol;
③加入______g硫酸铵到蒸发皿中,缓缓加热、浓缩至表面出现结晶膜为止、冷却,得硫酸亚铁铵晶体.
(2)回答下列问题:
①硫酸亚铁溶液在空气中易被氧化变质,操作时应注意:a______;b______;
②加热、浓缩溶液时,不浓缩至干的理由是______;
③硫酸亚铁和硫酸铵的混合溶液加热浓缩就能得到硫酸亚铁铵晶体,其原因是______;
④称取两份质量均为1.96g的该硫酸亚铁铵,制成溶液.用未知浓度的KMnO4酸性溶液进行滴定.
Ⅰ) 滴定时,将KMnO4酸性溶液装在______(酸式或碱式)滴定管,操作时用______手拿锥形瓶;
Ⅱ) 已知MnO4-被还原为Mn2+,试写出该滴定过程中的离子方程式:______;
Ⅲ) 判断该反应到达滴定终点的现象为______;
Ⅳ) 假设到达滴定终点时,用去V mL KMnO4酸性溶液,则该KMnO4酸性溶液的浓度为______mol/L.
查看习题详情和答案>>
 实验室制备乙酸正丁酯的化学方程式:
实验室制备乙酸正丁酯的化学方程式:CH3COOH+CH3CH2CH2CH2OH
| 浓H2SO4 |
| △ |
制备过程中还可能的副反应有:
CH3CH2CH2CH2OH
| 浓H2SO4 |
| △ |
主要实验步骤如下:
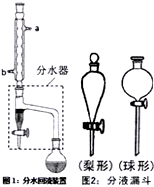
①在干燥的圆底烧瓶中加11.5mL正丁醇、7.2mL冰醋酸和3~4滴浓H2SO4,摇匀后,加几粒沸石,再如图1装置安装好分水器、冷凝管.然后小火加热.
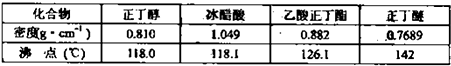
②将烧瓶中反应后的混后物冷却与分水器中的酯层合并,转入分液漏斗,③依次用10mL水,10mL 10%碳酸钠溶液洗至无酸性(pH=7),再水洗一次,用少许无水硫酸镁干燥.④将干燥后的乙酸正丁酯转入50mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品.主要试剂及产物的物理常数:
根据以上信息回答下列问题.
(1)图1装置中冷水应从
(2)在步骤①④中都用到沸石防暴沸,下列关于沸石的说法正确的是
A.实验室沸石也可用碎瓷片等代替 B.如果忘加沸石,可速将沸石加至将近沸腾的液体中
C.当重新进行蒸馏时,用过的沸石可继续使用 D.沸石为多孔性物质,可使液体平稳地沸腾
(3)在步骤③分液时,分液漏斗旋塞的操作方法与酸式滴定管的是否相同
(4)在提纯粗产品的过程中,用碳酸钠溶液洗涤主要除去的杂质
(5)步骤④的常压蒸馏,需收集