摘要:13.相同温度下.体积均为0.5 L的两个恒容密闭容器中发生可逆反应: 2XY2(g)+Y2(g) 2XY3(g) 实验测得反应在起始.达到平衡时的有关数据如下表所示: 容器 起始时各物质物质的/mol 达平衡时体系能量的变化 编号 XY2 Y2 XY3 ① 2 1 0 放热0.25QkJ ② 1.2 0.6 0.8 下列叙述不正确的是 A.达到平衡时.①和②两容器中气体的平均相对分子质量相同 B.容器②中反应达到平衡时放出的热量为0.15 Q kJ C.达到平衡时.两个容器中Y2的物质的量浓度均为1.5 mol·L-1 D.若容器①的其他条件不变.只增加1mol稀有气体.则达到平衡时放出的热量等于0.25 Q kJ
网址:http://m.1010jiajiao.com/timu3_id_1247894[举报]
相同温度下,体积均为0.5 L的两个恒容密闭容器中发生可逆反应:2XY2(g)+Y2(g)?2XY3(g)△H=-Q kJ?mol-1(Q>0)实验测得反应在起始、达到平衡时的有关数据如下表所示:
下列叙述不正确的是( )
| 容器 编号 |
起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| XY2 | Y2 | XY3 | ||
| ① | 2 | 1 | 0 | 放热 0.25 Q kJ |
| ② | 1.2 | 0.6 | 0.8 | |
A、容器①、②中反应的平衡常数均为
| ||
| B、达到平衡时,两个容器中Y2的物质的量浓度均为1.5 mol?L-1 | ||
| C、容器②中反应达到平衡时放出的热量为0.15 Q kJ | ||
| D、若容器①的其他条件不变,恒压下通入稀有气体,则达到平衡时放出的热量小于0.25 Q kJ |
相同温度下,体积均为0.5 L的两个恒容密闭容器中发生可逆反应:
2XY2(g)+Y2(g)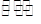 2XY3(g)
2XY3(g)
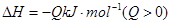
实验测得反应在起始、达到平衡时的有关数据如下表所示:
|
容器 |
起始时各物质物质的/mol |
达平衡时体系能量的变化 |
||
|
编号 |
XY2 |
Y2 |
XY3 |
|
|
① |
2 |
1 |
0 |
放热0.25QkJ |
|
② |
1.2 |
0.6 |
0.8 |
|
下列叙述不正确的是
A.达到平衡时,①和②两容器中气体的平均相对分子质量相同
B.容器②中反应达到平衡时放出的热量为0.15 Q kJ
C.达到平衡时,两个容器中Y2的物质的量浓度均为1.5 mol·L-1
D.若容器①的其他条件不变,只增加1mol稀有气体,则达到平衡时放出的热量等于0.25 Q kJ
查看习题详情和答案>>
相同温度下,体积均为0.5 L的两个恒容密闭容器中发生可逆反应:
2XY2(g)
+ Y2(g)  2XY3(g) △H=-Q kJ·mol-1(Q>0)
2XY3(g) △H=-Q kJ·mol-1(Q>0)
实验测得反应在起始、达到平衡时的有关数据如下表所示:
|
容器 编号 |
起始时各物质物质的量/mol |
达平衡时体系能量的变化 |
||
|
XY2 |
Y2 |
XY3 |
||
|
① |
2 |
1 |
0 |
放热 0.25 Q kJ |
|
② |
1.2 |
0.6 |
0.8 |
|
下列叙述不正确的是
A.容器①、②中反应的平衡常数均为1/13.5
B.达到平衡时,两个容器中Y2的物质的量浓度均为1.5 mol·L-1
C.容器②中反应达到平衡时放出的热量为0.15 Q kJ
D.若容器①的其他条件不变,恒压下通入稀有气体,则达到平衡时放出的热量小于0.25 Q kJ
查看习题详情和答案>>
相同温度下,体积均为0.5 L的两个恒容密闭容器中发生可逆反应:
2XY2(g)+Y2(g)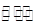 2XY3(g),
2XY3(g), 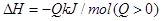
实验测得反应在起始、达到平衡时的有关数据如下表所示:
下列叙述不正确的是
A.达到平衡时,①和②两容器中气体的平均相对分子质量相同
B.容器②中反应达到平衡时放出的热量为0.15 Q kJ
C.达到平衡时,两个容器中Y2的物质的量浓度均为1.5 mol·L-1
D.若容器①的其他条件不变,只增加1mol稀有气体,则达到平衡时放出的热量等于0.25 Q kJ
2XY2(g)+Y2(g)
 2XY3(g),
2XY3(g), 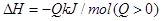
实验测得反应在起始、达到平衡时的有关数据如下表所示:
| 容器 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| 编号 | XY2 | Y2 | XY3 | |
| ① | 2 | 1 | 0 | 放热0.25QkJ |
| ② | 1.2 | 0.6 | 0.8 | |
A.达到平衡时,①和②两容器中气体的平均相对分子质量相同
B.容器②中反应达到平衡时放出的热量为0.15 Q kJ
C.达到平衡时,两个容器中Y2的物质的量浓度均为1.5 mol·L-1
D.若容器①的其他条件不变,只增加1mol稀有气体,则达到平衡时放出的热量等于0.25 Q kJ
相同温度下,体积均为0.5 L的两个恒容密闭容器中发生可逆反应:
2XY2(g) + Y2(g) 2XY3(g) △H=-Q kJ·mol-1(Q>0)
2XY3(g) △H=-Q kJ·mol-1(Q>0)
实验测得反应在起始、达到平衡时的有关数据如下表所示:
下列叙述不正确的是
A.容器①、②中反应的平衡常数均为1/13.5
B.达到平衡时,两个容器中Y2的物质的量浓度均为1.5 mol·L-1
C.容器②中反应达到平衡时放出的热量为0.15 Q kJ
D.若容器①的其他条件不变,恒压下通入稀有气体,则达到平衡时放出的热量小于0.25 Q kJ
2XY2(g) + Y2(g)
 2XY3(g) △H=-Q kJ·mol-1(Q>0)
2XY3(g) △H=-Q kJ·mol-1(Q>0)实验测得反应在起始、达到平衡时的有关数据如下表所示:
| 容器 编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| XY2 | Y2 | XY3 | ||
| ① | 2 | 1 | 0 | 放热 0.25 Q kJ |
| ② | 1.2 | 0.6 | 0.8 | |
A.容器①、②中反应的平衡常数均为1/13.5
B.达到平衡时,两个容器中Y2的物质的量浓度均为1.5 mol·L-1
C.容器②中反应达到平衡时放出的热量为0.15 Q kJ
D.若容器①的其他条件不变,恒压下通入稀有气体,则达到平衡时放出的热量小于0.25 Q kJ