摘要:(1)金属单质 + 酸 →盐 + 氢气 →另一种金属 + 另一种盐 (3)金属氧化物+木炭或氢气→金属+二氧化碳或水
网址:http://m.1010jiajiao.com/timu3_id_123546[举报]
金属在日常生活中随处可见,研究金属的性质可以更好地利用金属.
(1)铝、铁、铜是常见金属.下列生活用品中,主要利用金属导热性的是 (填序号).

(2)“淬火”是金属热处理常用的方法.宝剑淬火过程中,铁在高温下和水蒸气发生反应生成四氧化三铁和另一种气体单质,此反应的化学方程式为 ,该反应属于基本反应类型中的 反应.
(3)将一定量铁粉加入到硫酸锌、硫酸铜的混合液中,充分反应后过滤.滤液中的溶质一定有 .
(4)取一定量镁、锌、铁三种金属,分别加入溶质质量分数相等的稀盐酸,充分反应后,生成氢气的质量相等.下列做法与此结果相符的是 (填序号).
A.相同质量的三种金属与足量的稀盐酸反应
B.2.4g镁、6.5g锌、5.6g铁与足量的稀盐酸反应
C.向足量的镁、锌、铁中加入稀盐酸的质量比为2:3:2
D.足量的三种金属与等量的稀盐酸反应. 查看习题详情和答案>>
(1)铝、铁、铜是常见金属.下列生活用品中,主要利用金属导热性的是

(2)“淬火”是金属热处理常用的方法.宝剑淬火过程中,铁在高温下和水蒸气发生反应生成四氧化三铁和另一种气体单质,此反应的化学方程式为
(3)将一定量铁粉加入到硫酸锌、硫酸铜的混合液中,充分反应后过滤.滤液中的溶质一定有
(4)取一定量镁、锌、铁三种金属,分别加入溶质质量分数相等的稀盐酸,充分反应后,生成氢气的质量相等.下列做法与此结果相符的是
A.相同质量的三种金属与足量的稀盐酸反应
B.2.4g镁、6.5g锌、5.6g铁与足量的稀盐酸反应
C.向足量的镁、锌、铁中加入稀盐酸的质量比为2:3:2
D.足量的三种金属与等量的稀盐酸反应. 查看习题详情和答案>>
金属用途广泛,其结构和性质等是化学的重要研究内容。
(1)如图是铝的原子结构示意图。下列说法不正确的是_______。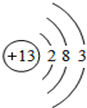
| A.铝原子中的质子数为13 |
| B.在化合物中铝通常显+3价 |
| C.铝是地壳中含量最多的元素 |
| D.铝可作导线是由于它具有良好的导电性 |

【提出问题】溶液A中的溶质可能有哪些?
【做出猜想】
① 只有Zn(NO3)2 ② Zn(NO3)2、AgNO3
③ Zn(NO3)2、Cu(NO3)2 ④ Zn(NO3)2、Cu(NO3)2、AgNO3
【交流讨论】不合理的猜想是_______(填标号),其理由是_______。
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请将下表填写完整。
| 实验步骤 | 现象 | 实验结论 |
| 取少量固体B,滴加_______ | 有气泡产生 | 固体B含有Cu 、Ag和_ |
(3)新型材料纳米级 Fe 粉具有广泛的用途,它比普通 Fe 粉更易与氧气反应,其制备工艺流程如图所示:
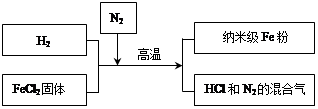
请回答下列问题:
①纳米级Fe粉在空气中易自燃。实验中通入N2的目的是_______。
②写出H2还原FeCl2,置换出铁的化学方程式_______。
③研究人员发现最后制得的纳米级 Fe 粉样品中混有少量的 FeCl2杂质。取样品20g,加入足量的盐酸,生成氢气 0.7 g。请计算该样品中单质 Fe 的质量分数(请写出计算过程)。_______ 查看习题详情和答案>>
金属在生产生活中应用广泛.
(1)铝可以制成铝箔,这是利用金属铝具有良好的 性.
(2)铁制品生锈的条件是 ,用稀盐酸除铁锈反应的化学方程式是 .
(3)我国是世界上最早采用湿法冶金提取铜的国家,铁与硫酸铜溶液反应的化学方程式是 .工业上冶炼铝,是将铝矿石(主要成分是Al2O3)在熔融条件下通电分解,其反应的化学方程式是 .
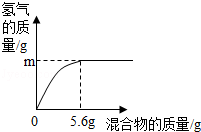
(4)现有两种金属单质组成的混合物.向100g某稀盐酸中加入该混合物,混合物的质量与生成氢气的质量关系如图所示.
下列说法正确的是 (填序号).
a.若混合物为Zn、Al,则m可能是0.2g
b.若混合物为Zn、Cu,则m一定大于0.2g
c.若混合物为Fe、Al,则稀盐酸中溶质质量分数一定大于7.3%
d.若混合物为Fe、Cu,m为0.1g,则该混合物中Fe的质量分数一定是50%