题目内容
金属在日常生活中随处可见,研究金属的性质可以更好地利用金属.
(1)铝、铁、铜是常见金属.下列生活用品中,主要利用金属导热性的是________(填序号).

(2)“淬火”是金属热处理常用的方法.宝剑淬火过程中,铁在高温下和水蒸气发生反应生成四氧化三铁和另一种气体单质,此反应的化学方程式为________,该反应属于基本反应类型中的________反应.
(3)将一定量铁粉加入到硫酸锌、硫酸铜的混合液中,充分反应后过滤.滤液中的溶质一定有________.
(4)取一定量镁、锌、铁三种金属,分别加入溶质质量分数相等的稀盐酸,充分反应后,生成氢气的质量相等.下列做法与此结果相符的是________(填序号).
A.相同质量的三种金属与足量的稀盐酸反应
B.2.4g镁、6.5g锌、5.6g铁与足量的稀盐酸反应
C.向足量的镁、锌、铁中加入稀盐酸的质量比为2:3:2
D.足量的三种金属与等量的稀盐酸反应.
解:用铜制成各种炊具,是利用它的良好的导热性;故答案为:②
(2)由题意知,反应物为铁和水蒸气、生成物为四氧化三铁和氢气、反应条件为高温,故可书写化学方程式为
3Fe+4H2O Fe3O4+4H2;此反应符合“单质+化合物=单质+化合物,即A+BC=B+AC”,即为置换反应;
Fe3O4+4H2;此反应符合“单质+化合物=单质+化合物,即A+BC=B+AC”,即为置换反应;
故答案为:3Fe+4H2O(气) Fe3O4+4H2 置换
Fe3O4+4H2 置换
(3)由于在金属活动性顺序中,铁在锌后铜前,因此发生的反应只有Fe+CuSO4=Cu+FeSO4 铁在和硫酸铜反应生成铜、氢气的同时也生成了硫酸亚铁,因此在滤液中一定有硫酸亚铁,还有没有参与反应的硫酸锌.
故答案为:FeSO4、ZnSO4
(4)①因为产生氢气的是盐酸中的氢离子,故参与反应的HCl的质量相等,产生的氢气的质量就相等.故D符合;
②假设Fe、Mg、Zn 三种金属分别跟稀盐酸充分反应,得到氢气的质量都是2g,
设参与反应的Fe的质量为x,Mg的质量为y,Zn的质量为z,
Fe+2HCl=FeCl2+H2↑,Mg+2HCl=MgCl2+H2↑,Zn+2HCl=2ZnCl2+H2↑,
56 2 24 2 65 2
x 2g y 2g z 2g
∴ =
= ,
,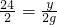 ,
,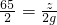
解之得:x=56g,y=24g,z=65g,
故Mg、Zn、Fe的质量比为:24g:65g:56g=24:65:56.
故B符合;C不符合;
故选BD.
分析:(1)物质的结构决定物质的性质,物质的性质决定物质的用途.
(2)由题意知,反应物为铁和水蒸气、生成物为四氧化三铁和氢气、反应条件为高温,故可书写化学方程式;由化学方程式判定反应类型;
(3)记住金属活动性顺序,金属和盐反应生成新的金属必须是前面的金属可以把排在后面的金属从盐溶液中置换出来.
(4)Fe、Mg、Zn三种金属分别跟稀盐酸反应的化学方程式为:Fe+2HCl=FeCl2+H2↑,Mg+2HCl=MgCl2+H2↑,Zn+2HCl=2ZnCl2+H2↑,由此可知,产生氢气的是盐酸中的氢离子,故要得到相同质量的氢气有两种情况:①参与反应的HCl的质量相等;②参与反应的Fe、Mg、Zn的质量符合得到相同质量的氢气的条件.
点评:四选项利用化学方程式和假设法解答问题较简单.在利用化学方程式解答问题时,运用假设法,对解题有很大作用.培养学生分析问题、解决问题的能力.
(2)由题意知,反应物为铁和水蒸气、生成物为四氧化三铁和氢气、反应条件为高温,故可书写化学方程式为
3Fe+4H2O
 Fe3O4+4H2;此反应符合“单质+化合物=单质+化合物,即A+BC=B+AC”,即为置换反应;
Fe3O4+4H2;此反应符合“单质+化合物=单质+化合物,即A+BC=B+AC”,即为置换反应; 故答案为:3Fe+4H2O(气)
 Fe3O4+4H2 置换
Fe3O4+4H2 置换(3)由于在金属活动性顺序中,铁在锌后铜前,因此发生的反应只有Fe+CuSO4=Cu+FeSO4 铁在和硫酸铜反应生成铜、氢气的同时也生成了硫酸亚铁,因此在滤液中一定有硫酸亚铁,还有没有参与反应的硫酸锌.
故答案为:FeSO4、ZnSO4
(4)①因为产生氢气的是盐酸中的氢离子,故参与反应的HCl的质量相等,产生的氢气的质量就相等.故D符合;
②假设Fe、Mg、Zn 三种金属分别跟稀盐酸充分反应,得到氢气的质量都是2g,
设参与反应的Fe的质量为x,Mg的质量为y,Zn的质量为z,
Fe+2HCl=FeCl2+H2↑,Mg+2HCl=MgCl2+H2↑,Zn+2HCl=2ZnCl2+H2↑,
56 2 24 2 65 2
x 2g y 2g z 2g
∴
 =
= ,
,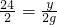 ,
,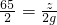
解之得:x=56g,y=24g,z=65g,
故Mg、Zn、Fe的质量比为:24g:65g:56g=24:65:56.
故B符合;C不符合;
故选BD.
分析:(1)物质的结构决定物质的性质,物质的性质决定物质的用途.
(2)由题意知,反应物为铁和水蒸气、生成物为四氧化三铁和氢气、反应条件为高温,故可书写化学方程式;由化学方程式判定反应类型;
(3)记住金属活动性顺序,金属和盐反应生成新的金属必须是前面的金属可以把排在后面的金属从盐溶液中置换出来.
(4)Fe、Mg、Zn三种金属分别跟稀盐酸反应的化学方程式为:Fe+2HCl=FeCl2+H2↑,Mg+2HCl=MgCl2+H2↑,Zn+2HCl=2ZnCl2+H2↑,由此可知,产生氢气的是盐酸中的氢离子,故要得到相同质量的氢气有两种情况:①参与反应的HCl的质量相等;②参与反应的Fe、Mg、Zn的质量符合得到相同质量的氢气的条件.
点评:四选项利用化学方程式和假设法解答问题较简单.在利用化学方程式解答问题时,运用假设法,对解题有很大作用.培养学生分析问题、解决问题的能力.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目







