摘要:13.铅蓄电池放电时.两极的反应分别是: 正极: 负极: 用铅蓄电池作电源电解AgNO3溶液时.当析出1.08g银时.铅蓄电池内消耗.H2SO4的物质的量为 A.0.01mol B.0.02mol C.0.04mol D.0.05mol
网址:http://m.1010jiajiao.com/timu3_id_1234254[举报]
铅蓄电池是最常见的二次电池,它由两组栅状极板交替排列而成,极板上分别覆盖有Pb和PbO2,电解质是H2SO4溶液。
(1)铅蓄电池放电时,其中一个电极的反应如下:PbO2 + 4H+ + SO42- +2e-==PbSO4 + 2H2O 该电极是
______(填“正极”或“负极”)。另一个电极的反应为_________。
(2)铅蓄电池充电时,总反应的化学方程式为_______________________。
(3)若使用铅蓄电池做电源,电解CuCl2溶液。已知CuCl2溶液足量,电解使用的电极为惰性电极。若在阳极上析出气体体积为44.8 L(标准状况下),则铅蓄电池中参加反应的H2SO4质量为___________。
查看习题详情和答案>>
(1)铅蓄电池放电时,其中一个电极的反应如下:PbO2 + 4H+ + SO42- +2e-==PbSO4 + 2H2O 该电极是
______(填“正极”或“负极”)。另一个电极的反应为_________。
(2)铅蓄电池充电时,总反应的化学方程式为_______________________。
(3)若使用铅蓄电池做电源,电解CuCl2溶液。已知CuCl2溶液足量,电解使用的电极为惰性电极。若在阳极上析出气体体积为44.8 L(标准状况下),则铅蓄电池中参加反应的H2SO4质量为___________。
构成铅蓄电池时,两种极板的铅、锑合金棚架上,均匀涂上膏状PbSO4,干燥后再分别安装,充电后即可使用。其发生的反应为:2PbSO4+2H2O PbO2+Pb+2H2SO4,下列对蓄电池的说法错误的是( )
PbO2+Pb+2H2SO4,下列对蓄电池的说法错误的是( )
A.需要定期补充硫酸
B.工作时铅为负极,PbO2为正极
C.充电时接电源正极的极板上发生的反应是:PbSO4+2H2O-2e-![]() PbO2+4H++
PbO2+4H++![]()
D.放电时电解液的密度减小
查看习题详情和答案>>
已知铅蓄电池总的化学方程式为Pb+PbO2+2H2SO4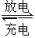 2H2O+2PbSO4,镍镉碱性充电电池在放电时,其正极反应为2NiO(OH)+2e-+2H2O===2Ni(OH)2+2OH-,负极反应为Cd+2OH--2e-===Cd(OH)2.铅蓄电池使用(放电)一段时间后,其内阻明显增大,电压却几乎不变,此时只有充电才能继续使用.镍镉碱性充电电池使用(放电)到后期,电压明显下降,其内阻却几乎不变,此时充电后也能继续使用.回答下列问题:
2H2O+2PbSO4,镍镉碱性充电电池在放电时,其正极反应为2NiO(OH)+2e-+2H2O===2Ni(OH)2+2OH-,负极反应为Cd+2OH--2e-===Cd(OH)2.铅蓄电池使用(放电)一段时间后,其内阻明显增大,电压却几乎不变,此时只有充电才能继续使用.镍镉碱性充电电池使用(放电)到后期,电压明显下降,其内阻却几乎不变,此时充电后也能继续使用.回答下列问题:
(1)铅蓄电池在放电时的负极反应为_________.
其在充电时的阳极反应为_________.
(2)镍镉碱性充电电池在充电时的总反应的化学方程式为_________.
(3)上述两种电池使用一段时间后,一个内阻明显增大,另一个内阻却几乎不变的主要原因可能是_________.
查看习题详情和答案>>
已知蓄电池在放电时起原电池的作用,在充电时起电解池的作用。汽车上用的铅蓄电池是以一组充满海绵状灰铅的铅板和另一组结构相似的充满二氧化铅的铅板组成。两个电极用硫酸溶液作电解质溶液。在放电时,两极发生的反应可分别表示为:
Pb+![]()
![]() PbSO4+2e-
PbSO4+2e-
PbO2+4H++![]() +2e-
+2e-![]() PbSO4+2H2O
PbSO4+2H2O
充电时,两极发生的反应分别表示为:
PbSO4+2e-![]() Pb+
Pb+![]()
PbSO4+2H2O-2e-![]() PbO2+4H++
PbO2+4H++![]()
根据上述材料,回答(1)—(3)题。
(1)在放电时,下列说法正确的是( )
A.铅板为电源正极 B.铅板为电源负极
C.铅板在放电时发生氧化反应 D.铅板在放电时发生还原反应
(2)在蓄电池放电时,溶液的pH将( )
A.不变 B.升高 C.降低 D.无法确定
(3)在蓄电池生产和使用时,下列说法正确的是( )
A.生产和使用铅蓄电池时,不会造成环境污染
B.生产和使用铅蓄电池时,可能引起铅中毒和环境污染
C.使用铅蓄电池时,若铅板上有1 mol铅反应就消耗2 mol H2SO4
D.在使用时,电池内溶液的密度会增大
查看习题详情和答案>>