网址:http://m.1010jiajiao.com/timu3_id_1231022[举报]
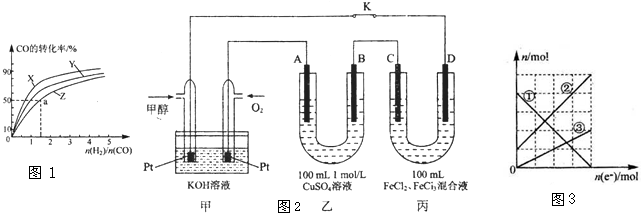
Ⅰ.工业上一般以CO和H2为原料在密闭容器中合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H=-90.8KJ/mol
(1)在容积为1L的恒容容器中,分别研究在230℃、250℃和270℃三种温度下合成甲醇的规律.如图1是上述三 种温度下不同的H2和CO的起始组成比(起始时CO的物质 的量均为1mol)与CO平衡转化率的关系,则曲线X对应的 温度是
(2)某温度下,将1mol CO和3mol H2充入1L的密闭容器中,充分反应后,达到平衡时 c(CO)=0.1mol/L.若保持温度和体积不变,将起始物质的物质的量改为a mol CO、b mol H2,c mol CH3OH,欲使开始时该反应向逆反应方向进行,c的取值范围是
Ⅱ.图2是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A,B两极上产生的气体体积相同.
(3)甲中负极的电极反应式为
(4)乙中A极析出的气体在标准状况下的体积为
(5)丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图3,则图中②线表示的是
甲醇是一种重要的化工原料。甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景。现有如下实验,在体积为1 L的密闭容器中,充入1mol CH3OH和1molH2O,一定条件下发生反应:CH3OH (g)+ H2O (g)  CO2(g) +3 H2 (g),测得CO2和CH3OH(g)的浓度随时间变化如下表所示。?
CO2(g) +3 H2 (g),测得CO2和CH3OH(g)的浓度随时间变化如下表所示。?
时间 物质 | 0 min | 10 min | 30 min | 60 min | 70 min |
CO2(mol/L) | 0 | 0.2 | 0.6 | 0.8 | 0.8 |
CH3OH(mol/L) | 1.0 | 0.8 | 0.4 | 0.2 | 0.2 |
①已知:CH3OH (g)+  O2 (g)
O2 (g)  CO2(g) + 2H2 (g)? ?H1= —192.9kJ/mol?
CO2(g) + 2H2 (g)? ?H1= —192.9kJ/mol?
H2(g)+  O2 (g)
O2 (g)  H2 O(g)? ?H2= —120.9kJ/mol?
H2 O(g)? ?H2= —120.9kJ/mol?
则甲醇与水蒸气催化重整反应的焓变△H3=_____??????????????????? 。?
②10~30 min内,氢气的平均反应速率v(H2)=___________mol/(L·min)。?
③该反应的平衡常数表达式为K=__________________。?
④下列措施中能使平衡时n(CH3OH)/n(CO2)减小的是(双选)___________。?
A.加入催化剂?????????????? B.恒容充入He(g),使体系压强增大?
C.将H2(g)从体系中分离??? D.再充入1molH2O?
(2)甲醇在催化剂条件下可以直接氧化成甲酸。?
①在常温下,用0.1000 mol/L NaOH溶液滴定20. 00 mL 0.1000 mol/L 甲酸溶液过程中,当混合液的pH=7时,所消耗的V(NaOH)___(填“<”或“>”或“=”) 20. 00 mL。?
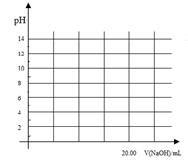
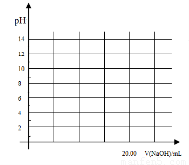
②在上述滴定操作中,若将甲酸换成盐酸,请在图中的相应位置画出相应的滴定曲线。(1滴溶液约0.04mL)?
查看习题详情和答案>>
甲醇是一种重要的化工原料。甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景。现有如下实验,在体积为1 L的密闭容器中,充入1mol CH3OH和1molH2O,一定条件下发生反应:CH3OH (g)+ H2O (g) CO2(g) +3 H2 (g),测得CO2和CH3OH(g)的浓度随时间变化如下表所示。
CO2(g) +3 H2 (g),测得CO2和CH3OH(g)的浓度随时间变化如下表所示。
| 时间 物质 | 0 min | 10 min | 30 min | 60 min | 70 min |
| CO2(mol/L) | 0 | 0.2 | 0.6 | 0.8 | 0.8 |
| CH3OH(mol/L) | 1.0 | 0.8 | 0.4 | 0.2 | 0.2 |
①已知:CH3OH (g)+
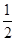 O2 (g)
O2 (g) CO2(g) + 2H2 (g) ?H1= —192.9kJ/mol
CO2(g) + 2H2 (g) ?H1= —192.9kJ/mol H2(g)+
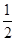 O2 (g)
O2 (g) H2 O(g) ?H2= —120.9kJ/mol
H2 O(g) ?H2= —120.9kJ/mol 则甲醇与水蒸气催化重整反应的焓变△H3=_____ 。
②10~30 min内,氢气的平均反应速率v(H2)=___________mol/(L·min)。
③该反应的平衡常数表达式为K=__________________。
④下列措施中能使平衡时n(CH3OH)/n(CO2)减小的是(双选)___________。
A.加入催化剂 B.恒容充入He(g),使体系压强增大
C.将H2(g)从体系中分离 D.再充入1molH2O
(2)甲醇在催化剂条件下可以直接氧化成甲酸。
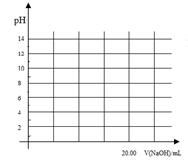
①在常温下,用0.1000 mol/L NaOH溶液滴定20. 00 mL 0.1000 mol/L 甲酸溶液过程中,当混合液的pH=7时,所消耗的V(NaOH)___(填“<”或“>”或“=”) 20. 00 mL。
②在上述滴定操作中,若将甲酸换成盐酸,请在图中的相应位置画出相应的滴定曲线。(1滴溶液约0.04mL)
 查看习题详情和答案>>
查看习题详情和答案>>
(1) 工业生产甲醇的常用方法是:CO(g)+ 2H2(g)  CH3OH(g) ;△H=-90.8 kJ·mol-1
CH3OH(g) ;△H=-90.8 kJ·mol-1
已知: 2H2(g)+ O2(g)  2H2O (l) ;△H=-571.6 kJ·mol-1
2H2O (l) ;△H=-571.6 kJ·mol-1
H2(g) + 1/2O2(g)  H2O (g) ;△H=-241.8 kJ·mol-1
H2O (g) ;△H=-241.8 kJ·mol-1
①H2的燃烧热为_________。
②CH3OH(g) + O2(g)  CO(g) + 2H2O(g) 的反应热△H=_________。
CO(g) + 2H2O(g) 的反应热△H=_________。
③若在恒温恒容的容器内进行反应CO(g)+ 2H2(g)  CH3OH(g),则可用来判断该反应达到平衡状态的标志有_________(填字母)
CH3OH(g),则可用来判断该反应达到平衡状态的标志有_________(填字母)
A.CO百分含量保持不变
B.容器中H2浓度与CO浓度相等
C.容器中混合气体的密度保持不变
D.CO的生成速率与CH3OH的生成速率相等
(2) 工业上利用甲醇制备氢气的常用方法有两种:
①甲醇蒸汽重整法。主要反应为CH3OH(g) CO(g) + 2H2(g)。设在容积为2.0 L的密闭容器中充入0.60 mol CH3OH(g),体系压强为P1,在一定条件下达到平衡时,体系压强为P2,且P1/P2 =2.2,计算该条件下CH3OH的平衡转化率。(要求写出计算过程)
CO(g) + 2H2(g)。设在容积为2.0 L的密闭容器中充入0.60 mol CH3OH(g),体系压强为P1,在一定条件下达到平衡时,体系压强为P2,且P1/P2 =2.2,计算该条件下CH3OH的平衡转化率。(要求写出计算过程)
②甲醇部分氯化法。在一定温度下以Ag/CeO2-ZnO为催化剂时原料气比例对反应的选择性(选择性越大,表示生成的该物质越多)影响关系如下图所示。 则当n(O2)/n(CH3OH)=0.25时。CH3OH与O2发生的主要反应方程式为:________。在制备H2时最好控制n(O2)/n(CH3OH) = ______。

 CO2(g) +3 H2 (g),测得CO2和CH3OH(g)的浓度随时间变化如下表所示。
CO2(g) +3 H2 (g),测得CO2和CH3OH(g)的浓度随时间变化如下表所示。 | 时间 物质 | 0 min | 10 min | 30 min | 60 min | 70 min |
| CO2(mol/L) | 0 | 0.2 | 0.6 | 0.8 | 0.8 |
| CH3OH(mol/L) | 1.0 | 0.8 | 0.4 | 0.2 | 0.2 |
①已知:CH3OH (g)+
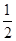 O2 (g)
O2 (g) CO2(g) + 2H2 (g) ?H1= —192.9kJ/mol
CO2(g) + 2H2 (g) ?H1= —192.9kJ/mol H2(g)+
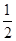 O2 (g)
O2 (g) H2 O(g) ?H2= —120.9kJ/mol
H2 O(g) ?H2= —120.9kJ/mol 则甲醇与水蒸气催化重整反应的焓变△H3=_____ 。
②10~30 min内,氢气的平均反应速率v(H2)=___________mol/(L·min)。
③该反应的平衡常数表达式为K=__________________。
④下列措施中能使平衡时n(CH3OH)/n(CO2)减小的是(双选)___________。
A.加入催化剂 B.恒容充入He(g),使体系压强增大
C.将H2(g)从体系中分离 D.再充入1molH2O
(2)甲醇在催化剂条件下可以直接氧化成甲酸。
①在常温下,用0.1000 mol/L NaOH溶液滴定20. 00 mL 0.1000 mol/L 甲酸溶液过程中,当混合液的pH=7时,所消耗的V(NaOH)___(填“<”或“>”或“=”) 20. 00 mL。
②在上述滴定操作中,若将甲酸换成盐酸,请在图中的相应位置画出相应的滴定曲线。(1滴溶液约0.04mL)