摘要:20.某同学为探究和是否能发生化学反应.设计出了如下图实验: (1)该同学想借助试管内气体压强变小而产生的现象来判定 能够发生反应.该同学设计的实验不是非常科学的.从 性质来分析其原因是 , (2)在原实验的基础上证明和确实发生了化学反应. 还需向反应后的溶液中加入的一种试剂是 ,反应的现象是 , (3) 和溶液反应的化学方程式为 .
网址:http://m.1010jiajiao.com/timu3_id_122919[举报]
某同学对“菠菜中富含可溶性草酸盐和碳酸盐,与豆腐同食会引起结石”的说法产生了兴趣.
探究一:菠菜里是否含有可溶性草酸盐和碳酸盐?
①可溶的草酸盐、碳酸盐能与CaCl2溶液反应生成难溶于水的草酸钙(CaC2O4)、碳酸钙.
②醋酸(化学式用HAc表示)不与草酸钙反应,但能与碳酸钙反应生成可溶性盐.
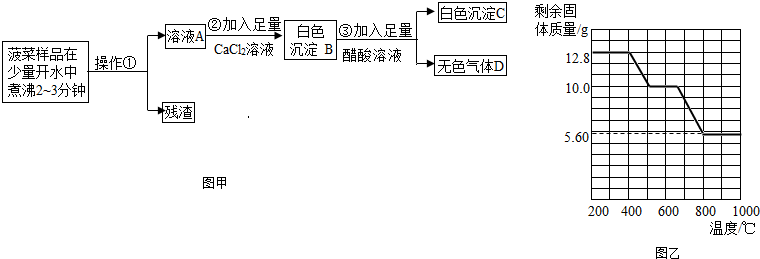
根据流程回答问题:
(1)操作①的名称是 .
(2)加入足量CaCl2溶液的目的是 .
(3)已知气体D能使澄清石灰水变浑浊,步骤③中发生反应的化学反应方程式为
【实验结论】菠菜里含有可溶性草酸盐和碳酸盐.
探究二:不同温度下,草酸钙分解的产物是否相同?
已知下列事实:
①草酸钙高温完全分解得到两种气态氧化物和一种固态氧化物.
②12.8g的草酸钙分解过程中温度与剩余固体的质量关系如乙图所示.根据上述事实,回答下列问题:
(4)草酸钙高温完全分解的化学方程式为 .
(5)通过上图数据分析,400℃--500℃发生反应的化学方程式是 ;
700℃时剩余固体的成分是 .
查看习题详情和答案>>
探究一:菠菜里是否含有可溶性草酸盐和碳酸盐?
①可溶的草酸盐、碳酸盐能与CaCl2溶液反应生成难溶于水的草酸钙(CaC2O4)、碳酸钙.
②醋酸(化学式用HAc表示)不与草酸钙反应,但能与碳酸钙反应生成可溶性盐.

根据流程回答问题:
(1)操作①的名称是
(2)加入足量CaCl2溶液的目的是
(3)已知气体D能使澄清石灰水变浑浊,步骤③中发生反应的化学反应方程式为
【实验结论】菠菜里含有可溶性草酸盐和碳酸盐.
探究二:不同温度下,草酸钙分解的产物是否相同?
已知下列事实:
①草酸钙高温完全分解得到两种气态氧化物和一种固态氧化物.
②12.8g的草酸钙分解过程中温度与剩余固体的质量关系如乙图所示.根据上述事实,回答下列问题:
(4)草酸钙高温完全分解的化学方程式为
(5)通过上图数据分析,400℃--500℃发生反应的化学方程式是
700℃时剩余固体的成分是
 某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请帮助完成下列实验报告.
某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请帮助完成下列实验报告.(一)实验目的:测定
测定粗锌的纯度
测定粗锌的纯度
.(二)实验用品:托盘天平、药水瓶、铜网、铜丝、饮料瓶.粗锌、稀盐酸、碱石灰(CaO和NaOH).
(三)实验步骤
| 实验内容和步骤 | 实验现象 | 结论(或化学方程式) |
| ①称量10.0g粗锌放在铜网中,按图示装置组装后,称得仪器和药品总质量为120.0g | ∕ | ∕ |
| ②将铜网插入足量稀盐酸中,充分反应 | 粗锌表面产生气泡 粗锌表面产生气泡 |
发生的化学方程式: Zn+2HCl═ZnCl2+H2↑ Zn+2HCl═ZnCl2+H2↑ |
| ③反应完全后,称得装置总质量为119.8g | ∕ | 产生H2的质量为 0.2 0.2 g.粗锌的纯度为 65% 65% . |
说明:不考虑空气中CO2、和H2O 对实验的影响.
(1)该实验中碱石灰的作用是
吸收氢气中的HCl和H2O
吸收氢气中的HCl和H2O
,若去掉碱石灰,则所测定的粗锌纯度偏大
偏大
(填“偏大”、“偏小”、“无影响”).(2)若只将粗锌换成石灰石,原实验方案能否用于石灰石样品纯度的测定
不能
不能
(填“能”或“不能”),理由是产生的CO2 将被碱石灰吸收,得不到生成的CO2质量
产生的CO2 将被碱石灰吸收,得不到生成的CO2质量
.(3)若将图中药水瓶改成直导管、粗锌换成纯锌,用原方案测定锌的相对原子质量,则结果
偏小
偏小
.(填“偏大”、“偏小”、“无影响”)某同学对“菠菜中富含可溶性草酸盐和碳酸盐,与豆腐同食会引起结石”的说法产生了兴趣.
探究一:菠菜里是否含有可溶性草酸盐和碳酸盐?
【查阅资料】
①可溶的草酸盐、碳酸盐能与CaCl2溶液反应生成难溶于水的草酸钙(CaC2O4)、碳酸钙.
②醋酸(化学式用HAc表示,)不与草酸钙反应,但能与碳酸钙反应生成可溶性醋酸钙[化学式为Ca(Ac)2].
【实验流程】

根据流程回答问题:
(1)操作①的名称是________; 沉淀C的名称是________
(2)加入足量CaCl2溶液的目的是_________.
(3)已知气体D能使澄清石灰水变浑浊,步骤③中发生反应的化学反应方程式为:________.
【实验结论】菠菜里含有________.
探究二:不同温度下,草酸钙分解的产物是否相同?
已知下列事实:
①草酸钙高温完全分解得到两种气态氧化物和一种固态氧化物.
②12.8g的草酸钙分解过程中温度与剩余固体的质量关系如右图所示.
根据上述事实,回答下列问题:
(4)草酸钙高温完全分解的化学方程式为________.
(5)通过上图数据分析,300℃时固体的成分是________.600℃时剩余固体的成分是________.800℃时剩余固体的成分是________.
查看习题详情和答案>>
某同学在做实验时发现盛放NaOH溶液的试剂瓶口与橡皮塞上常有白色粉末出现,为探究这一白色粉末的成分,他做了以下实验:
(1)取少量白色粉末于试管中,再滴加稀HCl,有气泡产生,由此可推出白色粉末中含有碳酸钠.碳酸钠形成的化学方程式是______.
(2)该同学为进一步探究白色粉末是否含有NaOH,设计了如下实验方案: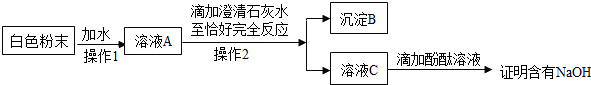
①沉淀B的物质名称为______.
②“操作1”的名称是______;进行“操作1”的目的是______;
现有铁架台、烧杯和玻璃棒,进行“操作2”时,还需补充的玻璃仪器是______.
③有同学认为该方案中滴加澄清石灰水不能确定粉末是否含有NaOH,其理由是______; 你的改进建议是______.
(3)为测定固体混合物中碳酸钠的质量分数,可采用下面图1所示装置进行实验.铁夹夹持的仪器是理想无摩擦注射器,通过反应后注射器内所收集到CO2气体的体积计算出Na2CO3的质量分数.
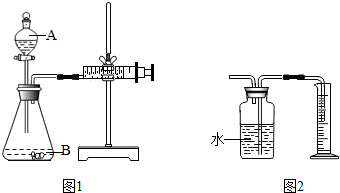
有同学提出以图2代替图1中的收集装置,则所测CO2气体的体积______(填“偏大”、“偏小”、“不变”),理由是______,你的改进方案______;广口瓶内原有的空气对实验结果______(填“有”或“没有”)影响.
查看习题详情和答案>>
某同学在家中发现有两瓶消毒药,瓶外贴的信息如下:
| 化学名:高锰酸钾 别名:灰锰氧,过锰酸钾,PP粉 化学式:KMnO4 相对分子质量:158.03 性质:是一种常见的强氧化剂,常温下为紫黑色片状晶体,见光易分解 用途:在工业上用作消毒剂、漂白剂等;医学上,用0.01%-0.02%的高锰酸钾溶液消毒、洗胃. | 化学名:过氧化氢 俗名:双氧水 化学式:H2O2 相对分子质量:34 性质:无色有刺激性气味的液体,不稳定 用途:医疗上常用3%的双氧水进行伤口或中耳炎消毒. |
他联系所学的化学知识,做了以下探究,请你跟他共同完成.

(1)实验室制取氧气的知识回顾
| 药 品 | KMnO4 | H2O2溶液(MnO2) |
| 反应原理(写方程式) | ______ | ______ |
| 发生和收集装置(选填如图) | ______ | ______ |
该同学想既然两种都是消毒药,能否混合使用呢?于是他进行了如下探究:
混合后观察现象:有使带火星的木条复燃的气体产生,混合液由紫红色变为无色,能使酚酞试液变红,有黑色固体产生.
1根据反应现象,该同学尝试书写了将KMnO4加入到H2O2中的化学反应方程式,
请帮他补充完整:2KMnO4+3H2O2=2MnO2↓+3O2↑+2H2O+______;
②该同学觉得制氧气的药品已经齐备,他又收集了家中的以下物品:
a.蜡烛,b.口服液玻璃瓶,c.吸管,d.注射器,e.小塑料瓶.
通过查阅资料得到以下信息:蜡烛火焰温度最高可达540°C左右;高锰酸钾受热分解温度为240°C左右;口服液玻璃瓶耐高温(800°C).
若选用KMnO4做反应物制氧气,则发生装置应选用上述物品中的______(选填字母);
若选用H2O2和MnO2制氧气,则发生装置应选用上述物品中______(选填字母). 查看习题详情和答案>>