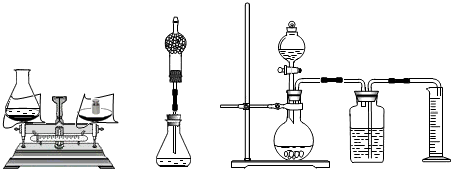
摘要:27.小海.小林.小明三同学一起测定双氧水溶液中溶质的质量分数. 查阅资料:2H2O2 2H2O+ O2↑,常温下氧气密度为1.42g/L. 设计原理:将一定质量的双氧水样品与二氧化锰混合.测定反应产生的氧气的质量.计算出H2O2的质量.继而得双氧水溶液中溶质的质量分数. 过程方法: (1)小海首先设计:向装有样品溶液中投入0.5g二氧化锰.待双氧水反应完毕后测得锥形瓶和反应后混合物的总质量为95.1 g.则产生氧气的质量是 g.双氧水溶液中溶质的质量分数为 . (2)小林对小海的设计提出质疑后.设计如中图的方案(只在上述方案中的锥形瓶上加一干燥管).请你说明小林质疑的理由是 . (3)小明通过思考后.觉得他们的方案误差都较大.于是小明设计如右图的方案.请你说明小明认为他们误差较大的原因: .如果要满足小明的要求.该实验需用 mL的量筒.
网址:http://m.1010jiajiao.com/timu3_id_12159[举报]
小海、小林、小明三同学一起测定双氧水溶液中溶质的质量分数.
查阅资料:2H2O2
2H2O+O2↑;常温下氧气密度为1.42g/L.
设计原理:将一定质量的双氧水样品与二氧化锰混合,测定反应产生的氧气的质量,计算出H2O2的质量,继而得双氧水溶液中溶质的质量分数.过程方法:
(1)小海首先设计(如图):向装有样品溶液(20g)的锥形瓶(75g)中投入0.5g二氧化锰,待双氧水反应完毕后测得锥形瓶和反应后混合物的总质量为95.1g,则产生氧气的质量是 g,双氧水溶液中溶质的质量分数为 .
(2)小林对小海的设计提出质疑后,设计如中图的方案(只在上述方案中的锥形瓶上加一干燥管),请你说明小林质疑的理由是 .
(3)小明通过思考后,觉得他们的方案误差都较大,于是小明设计如右图的方案(试剂用量不变).请你说明小明认为他们误差较大的原因: .如果要满足小明的要求,该实验需用 的量筒.
查看习题详情和答案>>
查阅资料:2H2O2
| ||
设计原理:将一定质量的双氧水样品与二氧化锰混合,测定反应产生的氧气的质量,计算出H2O2的质量,继而得双氧水溶液中溶质的质量分数.过程方法:
(1)小海首先设计(如图):向装有样品溶液(20g)的锥形瓶(75g)中投入0.5g二氧化锰,待双氧水反应完毕后测得锥形瓶和反应后混合物的总质量为95.1g,则产生氧气的质量是

(2)小林对小海的设计提出质疑后,设计如中图的方案(只在上述方案中的锥形瓶上加一干燥管),请你说明小林质疑的理由是
(3)小明通过思考后,觉得他们的方案误差都较大,于是小明设计如右图的方案(试剂用量不变).请你说明小明认为他们误差较大的原因:
小海、小林、小明三同学一起测定双氧水溶液中溶质的质量分数.
查阅资料:2H2O2
2H2O+O2↑;常温下氧气密度为1.42g/L.
设计原理:将一定质量的双氧水样品与二氧化锰混合,测定反应产生的氧气的质量,计算出H2O2的质量,继而得双氧水溶液中溶质的质量分数.
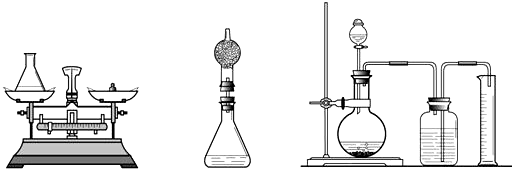
过程方法:(1)小海首先设计(如图):向装有样品溶液(20 g)的锥形瓶(75 g)中投入0.5g二氧化锰,待双氧水反应完毕后测得锥形瓶和反应后混合物的总质量为95.1 g,则产生氧气的质量是 ,双氧水溶液中溶质的质量分数为 .

(2)小林对小海的设计提出质疑后,设计如中图的方案(只在上述方案中的锥形瓶上加一干燥管),请你说明小林质疑的理由是 .
(3)小明通过思考后,觉得他们的方案误差都较大,于是小明设计如右图的方案(试剂用量不变).请你说明小明认为他们误差较大的原因: .如果要满足小明的要求,该实验需用 mL的量筒.
查看习题详情和答案>>
查阅资料:2H2O2
| ||
设计原理:将一定质量的双氧水样品与二氧化锰混合,测定反应产生的氧气的质量,计算出H2O2的质量,继而得双氧水溶液中溶质的质量分数.
过程方法:(1)小海首先设计(如图):向装有样品溶液(20 g)的锥形瓶(75 g)中投入0.5g二氧化锰,待双氧水反应完毕后测得锥形瓶和反应后混合物的总质量为95.1 g,则产生氧气的质量是

(2)小林对小海的设计提出质疑后,设计如中图的方案(只在上述方案中的锥形瓶上加一干燥管),请你说明小林质疑的理由是
(3)小明通过思考后,觉得他们的方案误差都较大,于是小明设计如右图的方案(试剂用量不变).请你说明小明认为他们误差较大的原因:
小海、小林、小明三同学一起测定双氧水溶液中过氧化氢的质量.
查阅资料:
常温下氧气密度为1.42g,L;
碱石灰干燥剂是氧化钙和固体氢氧化钠的混合物,极易吸收水蒸汽和二氧化碳.
设计原理:将一定质量的双氧水样品与二氧化锰混合,测定反应产生的氧气的质量,计算出其中过氧化氢的质量.
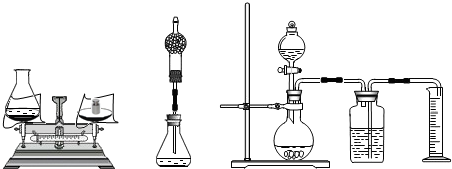
过程方法:
(1)小海首先设计(如图):向装有样品溶液(20g)的锥形瓶(75g)中投入0.5g二氧化锰,待双氧水反应完毕后测得锥形瓶和反应后混合物的总质量为95.1g,则产生氧气的质量是 g,双氧水溶液中过氧化氢的质量分数为 .
(2)小林对小海的设计提出质疑后,设计如中图的方案(只在上述方案中的锥形瓶上加一碱石灰干燥管),请你说明小林质疑的理由是 .
(3)小明通过思考后,觉得他们的方案误差都较大,于是小明设计如右图的方案(试剂用量不变).请你说明小明认为他们误差较大的原因: .
(4)小明实验前对该装置进行了气密性检查:打开装置中的活塞,发现分液漏斗中的水
没有流下,于是得出气密性良好的结论.你认为甲同学的检验方法是否可行? (填“是”或“否”).如果要满足小明要求,该实验需用 mL的量筒.
查看习题详情和答案>>
查阅资料:
常温下氧气密度为1.42g,L;
碱石灰干燥剂是氧化钙和固体氢氧化钠的混合物,极易吸收水蒸汽和二氧化碳.
设计原理:将一定质量的双氧水样品与二氧化锰混合,测定反应产生的氧气的质量,计算出其中过氧化氢的质量.

过程方法:
(1)小海首先设计(如图):向装有样品溶液(20g)的锥形瓶(75g)中投入0.5g二氧化锰,待双氧水反应完毕后测得锥形瓶和反应后混合物的总质量为95.1g,则产生氧气的质量是
(2)小林对小海的设计提出质疑后,设计如中图的方案(只在上述方案中的锥形瓶上加一碱石灰干燥管),请你说明小林质疑的理由是
(3)小明通过思考后,觉得他们的方案误差都较大,于是小明设计如右图的方案(试剂用量不变).请你说明小明认为他们误差较大的原因:
(4)小明实验前对该装置进行了气密性检查:打开装置中的活塞,发现分液漏斗中的水
没有流下,于是得出气密性良好的结论.你认为甲同学的检验方法是否可行?
 2H2O+O2↑;常温下氧气密度为1.42g/L.
2H2O+O2↑;常温下氧气密度为1.42g/L.