摘要: D 解析:石器是磨制的.没有生成新的物质是物理变化.而铁器和青铜器需要矿石进行冶炼制锝.而塑料制品也需要经过化学变化才能制取.
网址:http://m.1010jiajiao.com/timu3_id_120186[举报]
我国化工专家侯德榜曾为世界制碱工业作出了突出贡献.“侯氏制碱法”是以食盐、氨气、二氧化碳等为原料先制得N.HCq,进而生产出纯碱.其生产过程用化学方程式可简要表示为:
①NH3+H2O+CO2=NH4HCO3;②NH4HCO3+NaCl=NaHCO3↓+NH4Cl;③2NaHCO3
Na2CO3+H2O+CO2↑.
(1)“侯氏制碱法”生产过程中涉及到的基本反应类型是 .
A.置换反应;B.化合反应;C.分解反应;D.复分解反应
(2)第②步中加入的是磨细的食盐粉,食盐磨细的目的是 .
若第②步中得到的NaHCO3中含有少量的NH4HCO3,但不会影响产品Na2CO3的纯度,原因是 .
(3)若纯碱中含有NaHCO3杂质,为测定试样中纯碱的质量分数,用右图中的装置进行实验.主要实验步骤如下: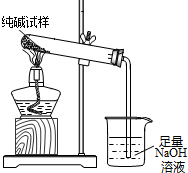
用天平准确称量出干燥试管的质量为20.2克,然后称取4.0克已研碎的纯碱样品并放入干燥的试管中.用酒精灯加热,待充分反应并冷却后,在天平上称出试管和碳酸钠的质量23.5克.
①停止加热前,要进行的操作是 .
②该试样中纯碱的质量分数为 .
查看习题详情和答案>>
①NH3+H2O+CO2=NH4HCO3;②NH4HCO3+NaCl=NaHCO3↓+NH4Cl;③2NaHCO3
| ||
(1)“侯氏制碱法”生产过程中涉及到的基本反应类型是
A.置换反应;B.化合反应;C.分解反应;D.复分解反应
(2)第②步中加入的是磨细的食盐粉,食盐磨细的目的是
若第②步中得到的NaHCO3中含有少量的NH4HCO3,但不会影响产品Na2CO3的纯度,原因是
(3)若纯碱中含有NaHCO3杂质,为测定试样中纯碱的质量分数,用右图中的装置进行实验.主要实验步骤如下:

用天平准确称量出干燥试管的质量为20.2克,然后称取4.0克已研碎的纯碱样品并放入干燥的试管中.用酒精灯加热,待充分反应并冷却后,在天平上称出试管和碳酸钠的质量23.5克.
①停止加热前,要进行的操作是
②该试样中纯碱的质量分数为
我国科学家侯德榜创造了一种著名的纯碱生产方法--“联合制碱法”.
(1)“联合制碱法”生产过程用化学方程式可简要表示为:
①NH3+CO2+H2O=NH4HCO3②NH4HCO3+NaCl=NaHCO3↓+NH4Cl ③2NaHCO3
Na2CO3+H2O+CO2↑.
该过程中没有涉及到的基本反应类型是( )
A.化合反应B.分解反应C.置换反应D.复分解反应
(2)第②步中加入的是磨细的食盐粉.食盐磨细的目的是: .
查看习题详情和答案>>
(1)“联合制碱法”生产过程用化学方程式可简要表示为:
①NH3+CO2+H2O=NH4HCO3②NH4HCO3+NaCl=NaHCO3↓+NH4Cl ③2NaHCO3
| ||
该过程中没有涉及到的基本反应类型是(
A.化合反应B.分解反应C.置换反应D.复分解反应
(2)第②步中加入的是磨细的食盐粉.食盐磨细的目的是:
(2007?湖州)我国化工专家侯德榜曾为世界制碱工业作出了突出贡献.“侯氏制碱法”是以食盐、氨气、二氧化碳等为原料先制得N.HCq,进而生产出纯碱.其生产过程用化学方程式可简要表示为:
①NH3+H2O+CO2=NH4HCO3;②NH4HCO3+NaCl=NaHCO3↓+NH4Cl;③2NaHCO3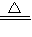 Na2CO3+H2O+CO2↑.
Na2CO3+H2O+CO2↑.
(1)“侯氏制碱法”生产过程中涉及到的基本反应类型是______.
A.置换反应;B.化合反应;C.分解反应;D.复分解反应
(2)第②步中加入的是磨细的食盐粉,食盐磨细的目的是______.
若第②步中得到的NaHCO3中含有少量的NH4HCO3,但不会影响产品Na2CO3的纯度,原因是______ NH3↑+H2O+CO2↑ 查看习题详情和答案>>
①NH3+H2O+CO2=NH4HCO3;②NH4HCO3+NaCl=NaHCO3↓+NH4Cl;③2NaHCO3
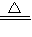 Na2CO3+H2O+CO2↑.
Na2CO3+H2O+CO2↑.(1)“侯氏制碱法”生产过程中涉及到的基本反应类型是______.
A.置换反应;B.化合反应;C.分解反应;D.复分解反应
(2)第②步中加入的是磨细的食盐粉,食盐磨细的目的是______.
若第②步中得到的NaHCO3中含有少量的NH4HCO3,但不会影响产品Na2CO3的纯度,原因是______ NH3↑+H2O+CO2↑ 查看习题详情和答案>>