摘要:21.右图是一种“化学氧自救器 (又称“自生氧防毒面具 ).其使用的生氧剂(主要成分是KO2)的作用原理为:4KO2+2CO2=2K2CO3+3O2 某研究小组取100g生氧剂.放人装置A中.加入足量水与生氧剂充分反应(化学方程式为:4KO2+2H2O=4KOH+3O2↑).测定反应前后装置A的总质量.他们进行了三次实验.测定结果如下: 测定序号 第1次 第2次 第3次 平均值 反应前装置A总质量(g) 400.1 400.2 399.7 400.O 反应后装置A总质量(g) 368.1 368.1 367.8 368.O 请根据上述实验结果计算:(假设杂质不与水反应产生气体) (1)100g生氧剂与足量水反应生成的氧气质量, (2)生氧剂中KO2的质量分数, (3)若成人每分钟正常需氧量为0.32g.则能维持成人正常呼吸20分钟的“化学氧自救器 .至少要装入这种生氧剂多少克?
网址:http://m.1010jiajiao.com/timu3_id_10065[举报]
(2011?遵义)下列图示中,A图是一种“化学氧自救器”,主要用于煤矿进下应急和机体缺氧病人的自救,它利用人呼出的二氧化碳与自救药罐中的生氧剂(超氧化钾KO2)接触产生的氧气,该反应的化学方程式为:4KO2+2CO2=2X+3O2

(1)上述化学方程式中,X的化学式为
(2)若要在实验室用高锰酸钾制取并收集一瓶氧气,你应选择图中的
(3)如采用双氧水和二氧化锰在实验室制取氧气,在选择发生装置时,小桐认为应选C,小晨认为应选D,你认为谁的选择更好?理由是
查看习题详情和答案>>

(1)上述化学方程式中,X的化学式为
K2C03
K2C03
.(2)若要在实验室用高锰酸钾制取并收集一瓶氧气,你应选择图中的
B
B
(填字母序号)作为发生装置,其相应的化学方程式为:2KMn04
K2Mn04+Mn02+02↑
| ||
2KMn04
K2Mn04+Mn02+02↑
,收集装置应选
| ||
E或G
E或G
(填字母序号).(3)如采用双氧水和二氧化锰在实验室制取氧气,在选择发生装置时,小桐认为应选C,小晨认为应选D,你认为谁的选择更好?理由是
小晨,控制反应速率(或节约药品,能够使反应随时发生,随时停止)
小晨,控制反应速率(或节约药品,能够使反应随时发生,随时停止)
,该反应的尔化学方程式为2H202
2H20+02↑
| ||
2H202
2H20+02↑
.
| ||
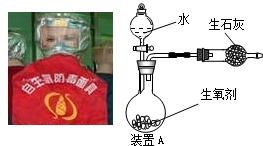 图是一种“化学氧自救器”(又称“自生氧防毒面具”),其使用的生氧剂(主要成分是KO2)的作用原理为:4KO2+2CO2=2K2CO3+3O2.某研究小组取100g生氧剂,放入装置A中,加入足量水与生氧剂充分反应(化学方程式为:4KO2+2H2O=4KOH+3O2↑),测定反应前后装置A的总质量(装置中的生石灰可防止因反应放热汽化的水蒸气从装置中逸出),他们进行了三次实验.测定结果如下
图是一种“化学氧自救器”(又称“自生氧防毒面具”),其使用的生氧剂(主要成分是KO2)的作用原理为:4KO2+2CO2=2K2CO3+3O2.某研究小组取100g生氧剂,放入装置A中,加入足量水与生氧剂充分反应(化学方程式为:4KO2+2H2O=4KOH+3O2↑),测定反应前后装置A的总质量(装置中的生石灰可防止因反应放热汽化的水蒸气从装置中逸出),他们进行了三次实验.测定结果如下
| 测定序号 | 第1次 | 第2次 | 第3次 | 平均值 |
| 反应前装置A总质量(g) | 400.1 | 400.2 | 399.7 | 400.O |
| 反应后装置A总质量(g) | 368.1 | 368.1 | 367.8 | 368.O |
(1)100g生氧剂与足量水反应生成的氧气质量;
(2)生氧剂中KO2的质量分数;(保留到0.1%) 查看习题详情和答案>>
下列图示中,A图是一种“化学氧自救器”,主要用于煤矿进下应急和机体缺
氧病人的自救,它利用人呼出的二氧化碳与自救药罐中的生氧剂(超氧化钾KO2)接触产
生的氧气,该反应的化学方程式为:4KO2+2CO2=2X+3CO2
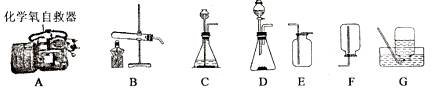
(1)上述化学方程式中,X的化学式为____ __。
(2)若要在实验室用高锰酸钾制取并收集一瓶氧气,你应选择图中的__ ___(填字母序号)作为发生装置,其相应的化学方程式为:_ _____,收集装置应选___ _(填字母序号)。
(3)如采用双氧水和二氧化锰在实验室制取氧气,在选择发生装置时,小桐认为应选C,小晨认为应选D,你认为谁的选择更好?理由是__ ___,该反应的尔化学方程式为____ ______。
查看习题详情和答案>>
下列图示中,A图是一种“化学氧自救器”,主要用于煤矿进下应急和机体缺氧病人的自救,它利用人呼出的二氧化碳与自救药罐中的生氧剂(超氧化钾KO2)接触产生的氧气,该反应的化学方程式为:4KO2+2CO2=2X+3O2

(1)上述化学方程式中,X的化学式为________.
(2)若要在实验室用高锰酸钾制取并收集一瓶氧气,你应选择图中的________(填字母序号)作为发生装置,其相应的化学方程式为:________,收集装置应选________(填字母序号).
(3)如采用双氧水和二氧化锰在实验室制取氧气,在选择发生装置时,小桐认为应选C,小晨认为应选D,你认为谁的选择更好?理由是________,该反应的尔化学方程式为________.
查看习题详情和答案>>
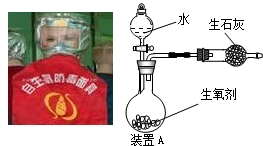 图是一种“化学氧自救器”(又称“自生氧防毒面具”),其使用的生氧剂(主要成分是KO2)的作用原理为:4KO2+2CO2=2K2CO3+3O2.某研究小组取100g生氧剂,放入装置A中,加入足量水与生氧剂充分反应(化学方程式为:4KO2+2H2O=4KOH+3O2↑),测定反应前后装置A的总质量(装置中的生石灰可防止因反应放热汽化的水蒸气从装置中逸出),他们进行了三次实验.测定结果如下
图是一种“化学氧自救器”(又称“自生氧防毒面具”),其使用的生氧剂(主要成分是KO2)的作用原理为:4KO2+2CO2=2K2CO3+3O2.某研究小组取100g生氧剂,放入装置A中,加入足量水与生氧剂充分反应(化学方程式为:4KO2+2H2O=4KOH+3O2↑),测定反应前后装置A的总质量(装置中的生石灰可防止因反应放热汽化的水蒸气从装置中逸出),他们进行了三次实验.测定结果如下
| 测定序号 | 第1次 | 第2次 | 第3次 | 平均值 |
| 反应前装置A总质量(g) | 400.1 | 400.2 | 399.7 | 400.O |
| 反应后装置A总质量(g) | 368.1 | 368.1 | 367.8 | 368.O |
(1)100g生氧剂与足量水反应生成的氧气质量;
(2)生氧剂中KO2的质量分数;(保留到0.1%) 查看习题详情和答案>>