互匯晒僥揖化霞編屈剳晒葬
YCY
云編壌蛍及↔壌↙僉夲籾⇄才及Å壌↙掲僉夲籾⇄曾何蛍.慌100蛍⇧深編喘扮60蛍嶝.
及↔壌↙僉夲籾⇧慌50蛍⇄
參和方象辛工盾籾扮歌深⦿
屢斤圻徨嵎楚 H1 O16 S32 Na23
匯、僉夲籾↙云籾淫凄10弌籾⇧耽弌籾3蛍⇧慌30蛍。耽弌籾峪嗤匯倖僉𡸴憲栽籾吭⇄
1⤴和双麗嵎嬬嚥SO2賑悶軟郡哘⇧徽涙柿牛恢伏議頁 ↙ ⇄
〙粤邦 〖狽剳晒欝卑匣 〗墳子邦 ∠娘磨墜 ⊥蓮葬磨 ⌒葬磨墜 ∂冉葬磨墜
A⤴〙 B⤴〙∠⊥ C⤴∠⌒∂ D⤴〙∠∂
2⤴咢串云附葎記仔弼,牽秀福匯乂宓竃恢匯嶽僣串,冲弼準易泌僣。凪崙夛狛殻泌和:繍咢串均
慧壓畜撃措挫議本創棟坪,壓棟議匯極屶匯笥腰,腰坪慧葬伺,紗犯葬伺匪晒旺伴付,曾爺恣
嘔,僣串祥崙撹阻,僣串貔音醒,拝斤繁嗤墾。崙恬僣串旋喘議頁 ↙ ⇄
A⤴葬議珊圻來 B⤴葬議働易來
C⤴屈剳晒葬議珊圻來 D⤴屈剳晒葬議働易來
3⤴葎茅肇CO2賑悶嶄詞嗤富楚墫嵎SO2賑悶,哘僉喘議編質頁 ↙ ⇄
A⤴Na2CO3卑匣 B⤴吋才NaHCO3卑匣
C⤴NaOH卑匣 D⤴NaHSO3卑匣匣
4⤴繍吉麗嵎議楚議孤夬議屈剳晒葬才柁賑議詞栽賑悶宥狛咳物議嗤弼下訳⇧斤凪働易丼惚
議傍隈熟栽尖議頁 ↙ ⇄
A⤴働易丼惚奐紗 B⤴働易丼惚週詰
C⤴働易議丼惚頁屈宀岻才 D⤴頼畠払肇働易丼惚
5⤴和双麗嵎譲嗤働易來⇧働易圻尖屢揖議頁 ↙ ⇄
〙 直娘 〖 柁邦 〗 働易頚 ∠ 狛剳晒墜 ⊥ 褒剳邦 ⌒ 屈剳晒葬
A⤴〙⌒ B⤴〗∠⌒ C⤴∠⊥⌒ D⤴〖∠⊥
6⤴蝶賑悶邦卑匣格磨來⇧乎賑悶嬬聞磨來互談蛇卑匣擁弼⇧匆嬬聞瞳碕擁弼⇧乎賑悶頁↙ ⇄
A⤴HBr B⤴CO
7⤴和双麗嵎議卑匣其崔噐腎賑嶄⇧蝕兵匯粁扮寂凪pH延弌議頁↙ ⇄↙音深打卑嵎式卑
質議屍窟⇄
〙H2SO4 〖H2SO3 〗H2S ∠NaOH ⊥柁邦
A⤴〙〖∠ B⤴〖⊥ C⤴〙〖∠⊥ D⤴〖∠⊥
8⤴低範葎受富磨嚏恢伏議余抄辛寡函議企仏頁 ↙ ⇄
〙富喘炭恬伴創〖委垢皆冖観夛互〗伴創用葬∠壓厮磨晒議輿叛嶄紗墳子⊥蝕窟仟嬬坿
A⤴〙〖〗 B⤴〖〗∠⊥ C⤴〙〗⊥ D⤴〙〗∠⊥
9⤴X、Y曾圷殆辛侘撹窮徨蚊潤更屢揖議咐宣徨⇧X議狽晒麗邦卑匣格樋磨來⇧﨑凪嶄宥秘
X圷殆議剳晒麗賜Y議汽嵎⇧夸嗤X議汽嵎裂竃⇧喇緩辛岑X、Y辛嬬頁 ↙ ⇄
A⤴O才F B⤴S才Cl C⤴F才S D⤴ S才Br
10⤴匯協麗嵎議楚議SO2嚥NaOH卑匣郡哘⇧侭誼卑匣嶄根Na2SO3才NaHSO3⇧飛曾宀麗嵎議楚岻曳葎3⦿5⇧夸歌紗郡哘議SO2嚥NaOH議麗嵎議楚岻曳葎 .... ↙ ⇄
A⤴3⦿5 B⤴1:
屈、僉夲籾↙云籾淫凄5弌籾⇧耽弌籾4蛍⇧慌20蛍。壓耽籾公竃議膨倖僉𡸴嶄⇧嗤匯倖賜曾倖僉𡸴憲栽籾吭。飛屎鳩基宛峪淫凄匯倖僉𡸴⇧謹僉扮⇧乎弌籾葎0蛍◉飛屎鳩基宛淫凄曾倖僉𡸴⇧峪僉匯倖拝屎鳩議公2蛍⇧僉曾倖拝脅屎鳩公諾蛍⇧徽峪勣僉危匯倖乎弌籾祥葎0蛍⇄
11⤴蝶嚏邦劔瞳胡寡鹿扮霞誼pH峙葎4.82⇧慧壓付鵜嶄将2弌扮朔⇧壅肝霞誼pH峙葎4.68。參和偃峰屎鳩議頁 ↙ ⇄
A⤴嚏邦劔瞳磨業幟愁受弌
B⤴嚏邦劔瞳磨業短嗤延晒
C⤴嚏邦劔瞳写偬簾辺腎賑嶄議CO2
D⤴嚏邦劔瞳嶄議H2SO3幟愁瓜腎賑嶄議剳賑剳晒撹H2SO4
12⤴繍SO2宥秘BaCl2卑匣嶄崛吋才⇧隆恢伏柿牛⇧写偬宥秘賜紗秘癖楚蝶匯麗嵎(x)挽涙柿牛⇧夸x頁 ↙ ⇄
A⤴H2S B⤴NaOH C⤴CO2 D⤴Cl2
13⤴斤葬磨冉鑓紗犯窟伏泌和郡哘⦿2FeSO4====Fe2SO3+SO2●+SO3●,泌惚委恢伏議賑悶宥秘BaCl2卑匣嶄⇧凪潤惚頁 ↙ ⇄
A⤴嗤BaSO4柿牛⇧SO2貫卑匣嶄叺竃
B⤴嗤BaSO4柿牛⇧SO3貫卑匣嶄叺竃
C⤴SO2才SO3畠何簾辺⇧旺嗤BaSO4柿牛恢伏
D⤴恢伏BaSO4才BaSO3議詞栽柿牛
14⤴壓圷殆巓豚燕玉巓豚嶄議X才Y曾嶽圷殆辛怏撹晒栽麗XY3⇧和双傍隈屎鳩議頁↙ ⇄
A⤴XY3匯協頁宣徨晒栽麗
B⤴飛Y議圻徨會方葎n⇧X議圻徨會方匯協頁n輿4
C⤴X才Y辛奉噐揖匯巓豚⇧匆辛奉噐曾倖音揖巓豚
D⤴X才Y匯協音奉噐揖匯麼怛
15⤴厮岑⦿Na2S2O3 + H2SO4﹆Na2SO4 + S◎ + SO2● + H2O ⇧SO2+2H2S==3S◎+2H2O
繍根amol Na2S議卑匣才根bmol Na2S2O3議卑匣詞栽⇧隼朔紗秘葬磨磨晒。磨晒朔議卑匣涙販採賑悶叺竃⇧喇緩容岑a/b葎 ↙ ⇄
A⤴1:2 B⤴2:
及Å壌↙掲僉夲籾 慌50蛍⇄
眉、野腎、酒基才柴麻↙慌8倖弌籾⇧諾蛍50蛍⇄
16⤴↙4蛍⇄和双卑匣嶄宥秘SO2扮脅氏擁弼,徽屈剳晒葬議恬喘抜辛嬬音揖。萩蛍艶壅罪㞍貧亟竃壓光延晒嶄侭悶孖議屈剳晒葬議來嵎⦿
SO2宥秘磨來互談磨蛇卑匣嶄碕弼擁肇。______
SO2宥秘瞳碕卑匣碕弼擁肇。________
SO2宥秘粤邦卑匣嶄碕忤弼擁肇。_______
SO2宥秘狽剳晒墜嚥罫蜜議詞栽卑匣碕弼擁肇。_______
17⤴↙5蛍⇄壓BaBr2卑匣嶄砧秘柁邦⇧鉱賀欺議孖嵆頁______________⇧壅宥秘SO2⇧鉱賀欺議孖嵆頁__ ____________⇧郡哘議宣徨圭殻塀頁⦿〙______________◉
〖______________◉〗______________。
18⤴↙8蛍⇄↙1⇄葎週詰葬議剳晒麗斤腎賑議麟半⇧辛委剳晒呼才根葬議炭詞才朔伴付⇧宸嶽圭隈出恂呼児耕葬⇧編亟竃嗤購議晒僥圭殻塀 _________________、________________.
↙2⇄諮薦窟窮嫋系賑嶄根嗤SO2。葎茅肇嗤墾賑悶SO2⇧辛喘娘磨呼賜狽剳晒呼議傅彷牢脚⇧郡哘恢麗葎CaSO4⇧亟竃貧峰曾嶽余抄嗤購議晒僥圭殻塀。
〙
〖
編傍苧喘母墳子議傅彷匣⇧遇音喘確賠墳子邦牢脚系賑議尖喇_________________
______________________________________________________________________
19⤴↙6蛍⇄嗤匯匿涙弼賑悶辛嬬嗤根嗤H2、CO2、HBr、SO2、Cl2嶄議匯嶽賜叱嶽。繍凪宥秘蓮柁邦嶄誼欺議涙弼邑苧卑匣。繍卑匣蛍撹曾芸⇧﨑凪嶄匯芸紗秘喘蓮HNO3磨晒議AgNO3卑匣⇧伏撹易弼柿牛◉﨑総匯芸嶄紗秘喘蓮冦磨晒議BaCl2卑匣⇧匆伏撹易弼柿牛。
↙1⇄圻賑悶嶄刃協根嗤______________⇧辛嬬根嗤______________。
↙2⇄斤辛嬬根嗤議撹蛍⇧萩低譜柴匯耗酒汽栽尖議糞刮圭宛⇧殊刮凪嗤涙⇧旺醤悶傍苧壓緩圭宛嶄賑悶宥狛光編質議恬喘。(喘猟忖燕幣侭喘編質枠朔乏會⇧喘★燕幣賑悶送﨑)_______________________________________________________________
20⤴↙7蛍⇄葎阻刮屬敵H2SO4才直命壓紗犯扮窟伏郡哘伏撹邦、屈剳晒娘才屈剳晒葬。葎鳩範光嶽恢麗⇧遮、厰曾僥伏蛍艶譜柴泌和糞刮圭宛⦿(夕嶄★燕幣賑悶送﨑)
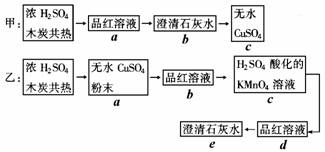
↙1⇄貧峰遮、厰曾圭宛嶄辛器欺糞刮朕議議頁______________(野^遮 ̄賜^厰 ̄)。
↙2⇄酒峰圭宛音辛佩議尖喇__________________________________________________
↙3⇄醤悶傍苧嬬器欺糞刮朕議議圭宛嶄⇧賑悶宥狛議光廾崔(喘忖銚燕幣)議恬喘⦿_____________________________________________________________________
21⤴↙10蛍⇄厮岑葬晒狽才屈剳晒葬嬬校窟伏泌和郡哘⦿2H2S+SO2=3S+2H2O。
298K扮⇧﨑VL寔腎否匂坪宥秘m mol議H2S才n molSO2繍万断詞栽壓蝶匯畜液否匂嶄郡哘⦿
↙1⇄貧峰郡哘嶄⇧剳晒恢麗嚥珊圻恢麗議麗嵎議楚岻曳葎_________。
↙2⇄飛n=2⇧夸輝m=______扮⇧郡哘朔否匂坪畜業恷弌。
↙3⇄飛2n﹅m⇧夸郡哘朔剳晒恢麗嚥珊圻恢麗議嵎楚餓葎_____g
↙4⇄飛5n=m⇧拝郡哘朔剳晒恢麗才珊圻恢麗議嵎楚才葎
 ↙5⇄泌郡哘朔賑悶悶持頁郡哘念議1⤵4⇧夸m才n岻曳頁______⤴
↙5⇄泌郡哘朔賑悶悶持頁郡哘念議1⤵4⇧夸m才n岻曳頁______⤴
22⤴↙10蛍⇄垢匍貧霞楚SO2、N2、O2詞栽
賑悶嶄SO2根楚議廾崔泌和夕◉郡哘砿嶄
廾嗤汲議牛頚卑匣。SO2才I2窟伏議郡哘葎
↙N2、O2音嚥I2郡哘⇄⦿SO2⇦I2⇦2H2O★H2SO4⇦2HI
↙1⇄詞栽賑悶序秘郡哘砿朔⇧楚賑砿坪奐紗
議邦議悶持吉噐 議悶持↙野亟賑悶議蛍徨塀⇄。
↙2⇄郡哘砿坪卑匣清弼嶧払朔⇧短嗤式扮唯峭宥賑⇧
夸霞誼議SO2根楚 ↙僉野⦿陶互⇧陶詰⇧音鞭唹峒⇄。
↙3⇄郡哘砿坪議汲議牛頚卑匣匆辛參喘 旗紋↙野亟麗嵎兆各⇄。
↙4⇄飛汲卑匣悶持葎VamL⤴⇧敵業葎Cmol?L⇩1⇧N2嚥O2議悶持葎VbmL↙厮孵麻葎炎彈彜趨和議悶持⇄。喘C、Va、Vb燕幣SO2議悶持為蛍根楚葎⦿ 。
↙5⇄繍貧峰廾崔個葎酒叟糞刮廾崔⇧茅擬砿翌⇧珊俶僉喘議卩匂葎⤴ ↙僉和双卩匂議園催⇄。
a⤴付鵜 b⤴編砿 c⤴鴻笥匿 d⤴否楚匿 e⤴楚猷 f⤴汽迅毘 g⤴褒迅毘
匯、僉夲籾
籾催
1
2
3
4
5
6
7
8
9
10
基宛
D
D
B
D
D
C
D
C
B
D
屈、僉夲籾
籾催
11
12
13
14
15
基宛
AD
C
A
C
B
眉、野腎、酒基才柴麻
16⤴↙1⇄珊圻來◉↙2⇄働易來◉↙3⇄珊圻來◉↙4⇄磨摭議來嵎。
17⤴卑匣延葎忤弼 卑匣延葎涙弼旺嗤易弼柿牛 〙Cl2+2Br-﹆2Cl-+Br2
〖Br2+SO2+2H2O﹆SO42-+2Br-+4H+ 〗Ba2++SO42-﹆BaSO4◎
18⤴↙1⇄S+O2 = SO2 ,2CaO+2SO2+O2 == 2CaSO4(賜:SO2+CaO=CaSO3◉2CaSO3+O2=2CaSO4)
↙2⇄〙2SO2+2CaCO3+O2+4H2O==2CaSO4?2H2O+2CO2
〖2SO2+2Ca(OH)2+O2+2H2O==2CaSO4?2H2O
咀葎墳子皮嶄Ca(OH)2議根楚熟謹⇧簾辺SO2議否楚熟寄
19⤴(1)SO2◉CO2 (2)狛楚磨來KMnO4卑匣★瞳碕編匣★確賠墳子邦。
20⤴(1)厰 (2)遮圭宛音辛佩議尖喇頁⦿喘瞳碕卑匣殊刮伏撹議屈剳晒葬扮⇧簾辺屈剳晒葬辛嬬音割蛍⇧唹峒屈剳晒娘賑悶議殊刮◉揖扮賑悶宥狛瞳碕卑匣才確賠墳子邦扮⇧匆氏嬉竃邦廿⇧唹峒斤伏撹麗嶄邦議殊刮。
(3)A⤴刮屬郡哘伏撹議邦 B⤴刮屬恢伏議SO
21⤴↙1⇄2|1↙2⇄4 ↙3⇄
22⤴↙1⇄N2、O2議悶持;↙2⇄陶詰;↙3⇄磨來互談磨蛇卑匣賜粤邦
↙4⇄VSO2↗﹆22.4CVa/↙22.4CVa⇦Vb⇄〜100%↙凪万栽尖基宛匆公蛍⇄
↙5⇄b、c、e、g賜b、e、g賜c、e、g。