江苏省南京市初中毕业、升学统一考试化学试题
第Ⅰ卷(选择题)
一、选择题(本题包括34小题,共34分,每小题只有一个选项符合题意)
1.下列自然现象,属于化学变化的是[ ]
A.海水蒸发
B.冰雪融化
C.动植物腐败
D.山体滑坡
2.北约轰炸南联盟的炼油厂,引起周边地区普降酸雨,这是因为空气中含有较多的[ ]
A.氧气
B.二氧化硫
C.氮气
D.一氧化碳
3.生活中的下列物质属于纯净物的是[ ]
A.蒸馏水
B.食醋
C.煤
D.大理石
4.能保持氧气化学性质的微粒是[ ]
A.氧元素
B.氧离子
C.氧原子
D.氧分子
5.国际上推广使用中国铁锅,这是因为铁锅[ ]
A.是单质
B.含碳,属于混合物
C.化学性质活泼
D.易使食物中含人体所需的铁元素
6.决定元素种类的是原子中的[ ]
A.电子数
B.质子数
C.中子数
D.最外层电子数
7.常用作消毒剂的高锰酸钾(KMnO4)中锰元素的化合价是[ ]
A.+7价
B.+6价
C.+5价
D.+4价
8.田径比赛发令枪打响后,产生的白烟主要是[ ]
A.SO2
B.CO2
C.P2O5
D.Fe3O4
9.冬天用煤火取暖,易造成中毒事件的气体是[ ]
A.氮气
B.水蒸气
C.二氧化碳
D.一氧化碳
10.一些食物的近似pH如下:葡萄3.5―4.5;苹果2.9―3.3;牛奶6.3―6.6;鸡蛋清7.6―8.0。其中显碱性的一种食物是[ ]
A.鸡蛋清
B.牛奶
C.苹果
D.葡萄
11.下列说法正确的是[ ]
A.原子不能再分
B.原子核都由质子、中子构成
C.式量的单位为一
D.水中含两个氢和一个氧
12.将鸡蛋壳浸入稀盐酸中,有气泡产生,这是因为鸡蛋壳中含有[ ]
A.硫酸根
B.碳酸根
C.氢氧根
D.硝酸根
13.下列常见物质,不属于有机物的是[ ]
A.CO2
B.CH4
C.C2H5OH
D.CH3COOH
14.3克碳在空气中充分燃烧,可向大气中排放温室气体(CO2)的质量是(原子量:C为12,O为16)[ ]
A.14克
B.11克
C.7克
D.6克
15.下列说法与事实不符的是[ ]
A.地壳中含量最多的元素是氧
B.空气中含量最多的元素是氮
C.金属活动顺序表中,活动性最强的是钾
D.氧化物中一定含金属元素
16.下列关于物质用途的叙述,易造成重大伤亡事故的是[ ]
A.活性炭可做冰箱除臭剂
B.熟石灰可用来粉墙
C.庆典活动可使用大量氢气球
D.钛合金可做轮船外壳
17.下列情况下,常常使铁制品锈迹斑斑的是[ ]
A.表面涂油
B.任其风吹雨淋
C.表面镀锌
D.保持表面干燥
18.下列仪器中,不能作为反应容器的是[ ]
A.试管
B.集气瓶
D.量筒
D.烧杯
19.下列四项基本操作中,正确的是[ ]
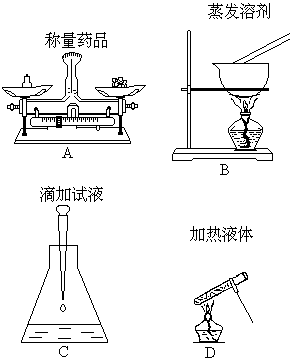
20.下列有关实验操作先后顺序,正确的是[ ]
A.制O2结束时,先熄灭酒精灯,再将导管移出水面
B.稀释浓H2SO4时,先将浓H2SO4倒入烧杯中,再慢慢注入水
C.H2还原CuO,应先通H2后加热
D.让铁丝先在盛O2的集气瓶中燃烧,再在瓶底放少量水
21.下列电离方程式书写正确的是[ ]
A.Ca(OH)2=Ca +2 +OH -
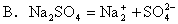
C.H2SO4=2H + +S 6+ +4O 2-
D.BaCl2=Ba 2+ +2Cl -
22.新买的铝锅、铝壶用来烧开水时,凡是水浸到的地方都会变黑,说明水中溶有[ ]
A.钾盐
B.纳盐
C.钙盐
D.铁盐
23.区别CO和H2,可用的方法是分别[ ]
A.点燃后观察火焰的颜色
B.通到水中
C.将燃烧产物通入澄清石灰水
D.与灼热的氧化铜反应
24.下列叙述中错误的是[ ]
A.可燃物遇到氧气就燃烧
B.档案材料着火,可用于冰扑灭
C.点燃氢气前一定要验纯
D.严禁携带易燃、易爆物品上车船
25.下列关于溶液的说法,正确的是[ ]
A.饱和石灰水一定是浓溶液
B.无色的液体一定是溶液
C.溶液一定是均一、稳定的
D.溶液一定是固体溶于水形成的
26.下列物质一般不参与复分解反应的是[ ]
A.CuSO4
B.KNO3
C.Fe2O3
D.H2SO4
27.可以作为复合肥料使用的是[ ]
A.KH2PO4
B.(NH4)2SO4
C.KCl
D.CO(NH2)2
28.据今年6月5日“世界环境日”的现场报道:甘甜清澈的长江源头水流至入海口,水下能见度变为不足10厘米。其主要原因是沿途大量流入①工业废水;②生活污水;③泥沙;④雨水。下列回答正确的是[ ]
A.①②
B.③④
C.①②③
D.①②③④
29.以下对科学事实的归纳和总结,你认为正确的是[ ]
A.置换反应不一定要在溶液中发生
B.碱能跟一切非金属氧化物起反应
C.酸能跟所有盐起反应
D.酸跟活泼金属反应一定生成盐和氢气
30.已知碳酸钙和另一物质组成的混合物含碳量大于12%,则另一物质可能是(原子量:Ca为40,C为12,O为16,Na为23,K为39,H为1,Mg为24)[ ]
A.Na2CO3
B.KHCO3
C.MgCO3
D.K2CO3
31.下列物质的特征:①液体是无色、无气味的;②液体具有酒香气味;③液体具有鲜艳的颜色;④盐呈白色粉末状。其中不能作为食用依据的是[ ]
A.①②
B.②③
C.②③④
D.①②③④
32.在化合、分解、置换、复分解四类反应中,可能生成水的反应有[ ]
A.1类
B.2类
C.3类
D.4类
33.某电镀厂排出的酸性污水中,含有有毒的Cu 2+ ,欲除去Cu 2+ ,并降低其酸性,加入适量下列物质不能达到目的的是[ ]
A.碳酸钠
B.生石灰
C.氯化铁
D.铁粉
34.某课外兴趣小组的同学,通过实验测定浓硫酸吸水性的有关数据,绘制成如图的函数图象,其中横坐标表示时间,纵坐标可以表示:①溶质的质量分数;②溶液的质量;③溶液的体积;④溶液中所含水的质量。其中正确的是[ ]
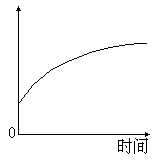
A.①②
B.②③
C.②③④
D.①②③④
二、选择题(本题包括3小题,共6分,每小题有一个或二个选项符合题意,错选、多选不给分,少选且选对了给1分)
35.下面报道中,你认为科学的是[ ]
A.一窨井冒出大火,烧伤行人,估计是窨井产生可燃性气体和氮气遇明火引起的
B.识别街头贩卖的假银元,可用硫酸铜溶液浸泡,观察颜色有无变化
C.利用气球内的于冰释放出一氧化碳的原理,使气球始终处于充足了气的状态
D.不是企业消灭污染,就是污染消灭企业
36.下列各组溶液,不加其它试剂就能鉴别的是[ ]
A.Na2CO3、H2SO4、HCl、NaNO3
B.NaOH、NaCl、HCl、FeCl3
C.HCl、AgNO3、HNO3、MgCl2
D.K2SO4、Na2CO3、BaCl2、HNO3
37.对下列实验过程的评价,正确的是[ ]
A.某固体中加入稀盐酸,产生了无色气体,证明该
B.某溶液中滴加BaCl2溶液,生成不溶于稀HNO3
C.某无色溶液滴入酚酞试液显红色,该溶液不一定是碱溶液
D.验证烧碱溶液中是否含Cl - ,先加稀盐酸除去OH - ,再加AgNO3溶液,有白色沉淀出现,证明含Cl -
第Ⅱ卷(非选择题)
三、填空题(本题共38分)
38.研究发现,我国某些地区居民喜食的腌制食品,能产生二甲基亚硝胺(CH3)2NNO,它与导致癌病高发有关。它由____种元素组成,每个分子中共有____个原子。
39.用化学式填写:在氧气、碳、盐酸、氢氧化钠中,能使带火星的木条复燃的是________;能作为实验室制取氢气或二氧化碳的原料是____________;其固体可以作为氧气或一氧化碳的干燥剂的是___________;可用来还原氧化铜的是__________。试在括号内用符号或化学式表示下文中加横线的物质:在饱和碳酸钠溶液降温时,按2个钠离子( )、1个碳酸根离子( )和10个水分子( )的个数比相结合,可以形成碳酸钠晶体( )。
40.根据下图所示实验装置进行回答:
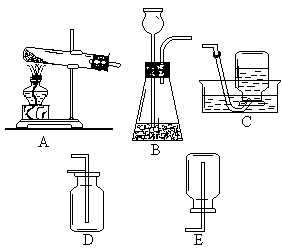
(1)用固体与液体在常温下反应产生气体应选(填序号,下同)____;用固体受热反应产生气体应选____;收集难溶性气体应选____;收集常温下密度比空气大的气体应选____。
(2)A的试管口略向下倾斜,是为了防止受热后试管____;B中的长颈漏斗末端应伸至液面以下,可以防止产生的气体____。伸进D、E中的导管均应接近集气瓶底部,是为了将瓶中的空气____。
41.某固体粉末与氯酸钾混合共热,发现氯酸钾分解速率明显增大。由此得出粉末在该反应中(填“一定是”、“可能是”、“不是”)____。催化剂。
42.写出下列反应的化学方程式,并注明反应类型(指化合、分解、置换、复分解)。
(1)我国宋代用铁和硫酸铜溶液反应制铜________属于( )反应
(2)用氢气做燃料的“零污染汽车”,其燃烧反应________属于( )反应
(3)在石灰窑中,煅烧石灰石制生石灰__________属于( )反应
(4)用盐酸洗去试管壁上的氧化铜____________属于( )反应
43.根据下图回答问题(计算结果保留三位有效数字):
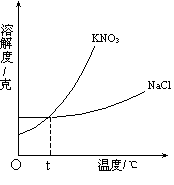
(1)已知t℃时,KNO3的溶解度为36克。则该温度______下50克水中最多溶解______克NaCl,此时NaCl溶液中的NaCl的质量分数为______。
(2)将混合物中的KNO3和NaCl进行分离,可以用热的饱和溶液______结晶的方法。
44.现有白纸、溶质质量分数分别为:(A)10%的NaOH溶液,(B)5%的H2SO4溶液,(C)5%的紫色石蕊溶液。试设计《“雨”落叶出红花开》的趣味实验:先在白纸上用玻璃棒蘸(填序号,下同)______画上花,再蘸______画上叶,将白纸挂上墙,用______向纸上喷洒即可。实验的化学原理是______。
实验证明,少数活泼金属能在二氧化碳中燃烧,由此推断二氧化碳不能用来灭火①。例如用坩埚钳夹镁带点燃,随即放在盛二氧化碳的集气瓶上方②,发生的燃烧反应为:2Mg+CO2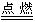 2MgO+C,该反应中,Mg是还原剂,发生还原反应③,CO2是氧化剂,发生氧反应④。反应前后,还原剂中元素化合价降低⑤,氧化剂中有元素化合价升高⑥。
2MgO+C,该反应中,Mg是还原剂,发生还原反应③,CO2是氧化剂,发生氧反应④。反应前后,还原剂中元素化合价降低⑤,氧化剂中有元素化合价升高⑥。
①___________________________
②___________________________
③___________________________
④___________________________
⑤___________________________
⑥___________________________
46.根据物质的组成或结构不同,具体填写(1)―(6)组物质性质不同的原因。并以此为例,再写另外两组实例。
(1)金刚石、石墨:碳原子__________不同。
(2)钠原子和氯原子:原子的________不同。
(3)CO与CO2:分子的____________不同。
(4)酸溶液、碱溶液:所含的________不同。
(5)生铁和钢:________________不同。
(6)浓硫酸和稀硫酸:__________不同。
(7)___________________________。
(8)___________________________。
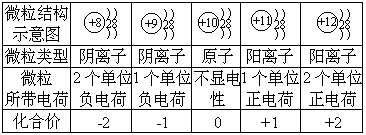
47.已知几种离子或原子的结构、带电情况及其化合价如下表所示。通过此表可总结出:“带负荷的原子属于阴离子”。还能总结出:
(1)_______________________________
(2)_______________________________
(3)_______________________________
(4)_______________________________
48.药品标签上应注明名称、化学式和质量标准,有的还指明有剧毒性、腐蚀性、挥发性。由此联想到,农民购买、贮存、使用农药时,应注意的事项及理由,请填入下表。

四、简答题(本题共4分)
49.为提高南京的空气质量,可以采取的措施有哪些?
(1)__________________________________
(2)__________________________________
(3)__________________________________
(4)__________________________________
50.面对湖水被严重污染,有人建议:①建立拦污闸,对入湖污水预先进行治理。②将长江水引入冲洗,使死水变活。③恢复湖中荷藕、菱、水葫芦的种植,利用植物的净水作用,并将植物叶茎回收,经沼气池发酵产生沼气。从长远观点看,你同意(填序号)__________方案。不同意有关方案的理由是__________。
五、实验推断题(本题共9分)
51.某市三名学生误入废弃的防空洞,虽经抢救,仍造成学生及抢救人员重大伤亡。该事件提醒我们:
(1)进人洞穴前,需要进行____实验,当证明洞内缺氧时,应携带____进入洞穴。
(2)需要检验洞内气体成分。例如可组合下列装置检验它是否含H2O、CO、CO2。
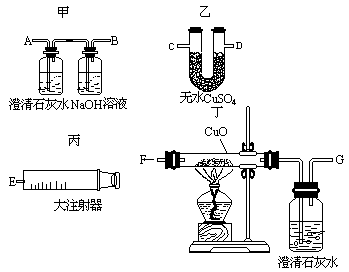
①先用____从洞穴中抽取气体样品,然后将装置按如下顺序连接(填A、B…):____接____,____接____,____接____。③通入气体实验后,观察到____中出现____时,证明含H2O;观察到____中出现____时,证明含CO2;观察到____中出现____时,证明含CO。最终尾气应作____处理。
52.某同学可用下图装置粗略地测定空气中氧气的体积分数。图中烧杯上方玻璃管(预先固定好)中部有一可左右滑动的活塞,活塞左端管内密封有空气,活塞右端的玻璃管口跟空气连通,实验开始前活塞处在刻度5厘米处。
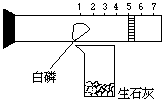
(1)向烧杯内加入适量水,与生石灰反应的目的是_____________________________________。
(2)可观察到玻璃管内开始发生的现象:①白磷(足量)____________;②活塞向(填左、右)__________移动。
(3)实验结束,恢复至常温后,活塞应停在约________厘米处,据此可得出的结论是______________。
53.溶有A、B、C、D四种物质的溶液,它们各是Na2SO4、HCl、Ba(OH)2、Na2CO3中的一种。现确知它们与反应产物的关系是:A+C→E↓+F;B+C→G↓+F;B+D→H+J+K↑。试写出化学式:A________;B________;C________;D________。
六、计算题(本题共9分)
(原子量:H―1,C―12,O―16,S―32,Fe―56,Zn―65。提示:计算过程注意数字间约分,以简化计算)
54.某钢铁厂日产含4%杂质的生铁2240吨。问:
(1)需要含Fe2O3质量分数为80%的赤铁矿石多少吨?
(2)若现在只有上述的赤铁矿石2160吨,为了确保生铁的周产量不变,还需要含Fe3O4质量分数为56%的磁铁矿石________吨。
55.某同学根据所做实验进行下列计算:
(1)配制184克质量分数为19.6%的稀硫酸,需要98%浓硫酸(密度为1.84克/厘米3)____毫升。
(2)取一定量上述配制好的稀硫酸倒入烧杯中,向烧杯中投入一块足量的锌片,待硫酸作用完成后,锌片质量减轻6.5克;再将烧杯内溶液蒸发掉6克水后,并降温至10℃,恰好成为饱和溶液,求10℃时硫酸锌的溶解度(保留三位有效数字)。
一、(每小题1分,本题共34分)
1.C;2.B;3.A;4.D;5.D;6.B;7.A;8.C;9.D;10.A;11.C;12.B
13.A;14.B;15.D;16.C;17.B;18.C;19.B;20.C;21.D;22.D;23.C;24.A
25.C;26.B;27.A;28.C;29.A;30.C;31.D;32.D;33.C;34.C;;
二、(每小题2分,本题共6分)
35.B、D 36.B、D 37.C
三、(共38分)
38.四;11(每空0.5分,共1分)
39.O2;HCl;NaOH;C

(每空0.5分,共4分)
40.(1)B;A;C;D; (2)炸裂;从长颈漏斗口逸出;排净(每空0.5分,共3.5分)
41.可能是(1分)
42.(1)Fe+CuSO4 FeSO4+Cu;置换;
FeSO4+Cu;置换;
(2)2H2+O2 2H2O;化合;
2H2O;化合;
(3)CaCO3 CaO+CO2↑;分解;
CaO+CO2↑;分解;
(4)CuO+2HCl CuCl2+H2O;复分解(每个方程式1.5分,类型0.5分,共8分)
CuCl2+H2O;复分解(每个方程式1.5分,类型0.5分,共8分)
43.(1)18.0(0.5分);26.5%(1分) (2)冷却(0.5分)
44.B;A;C;紫色石蕊试液遇酸变红,遇碱变蓝。
(前面三空每空0.5分,最后一空1分,共25分)
45.①不能灭活泼金属的着火;②里;③镁是还原剂,发生氧化反应;④CO2是氧化剂,发生还原反应;⑤升高;⑥降低(每空0.5分,共3分)
46.(1)排列;(2)最外层电子数;(3)构成;(4)离子;(5)含碳量(或含铁量);
(6)含硫酸质量分数;(7)氯原子和氯离子:最外层电子数不同;(8)盐酸和稀硫酸:所含酸根离子不同。
(前面六空,每空0.5分,后面两空每空1分,共5分,其中(7)、(8)其它合理答案也给分)
47、(1)核外电子总数大于质子总数,为阴离子;
(2)核外电子排布相同而核电荷数不同,可分属于不同元素;
(3)原子失电子数等于其正价数;
(4)核外电子排布相同,但核电荷数不同,可分别是阳离子、阴离子、原子。
(每空1分,共4分,其它合理答案给分)
48.

(每空0.5分,共4分;其它合理答案也给分)
四、(共4分)
49.(1)减少建筑工地粉尘;(2)限制使用含铅汽油;(3)尽量用燃气代替燃煤;(4)工业废气经处理后才能排放。
(每空0.分,共2分,其它合理答案也给分)
50.①③;污水冲入长江后会造成二次污染(每空1分,共2分)
五、(共9分)
51.(1)灯火(0.5分);供氧设备(0.5分)
(2)①丙(0.5分)E接C(或D),D(或C)接A,B接F(1分,错一空不给分)②乙,蓝色(0.5分);甲,浑浊(0.5分);丁,黑色CuO变红(或澄清石灰水变浑浊);(0.5分)燃烧(0.5分)(本题共4.5分)
52.(1)供热 (2)①燃烧,产生白烟 ②右 (3)4,氧气约占空气体积的l/5。(每空0.5分,共2.5分)
53.A.Na2SO4;B.Na2CO3;C.Ba(OH)2;D.HCl。(每空0.5分,共2分)
六、(共9分)
54.解:(1)设需要赤铁矿石的质量为x。
Fe2O3+3CO 2Fe+3CO2 (0.5分)
2Fe+3CO2 (0.5分)
106 112
x×80%2 240吨×(1-4%)(0.5分)

x=3840吨 (0.5分)
答:需80%的赤铁矿石3840吨。 (0.5分)
(2)2320吨 (1分)
55.(1)20 (1分)
(2)解:设消耗19.6%稀硫酸溶液的质量为x,生成硫酸锌质量为y。
H2SO4+Zn ZnSO4+H2↑ (0.5分)
ZnSO4+H2↑ (0.5分)
98 65 161
x×19.6% 6.5克 y (0.5分)

x=50克(0.5分) y=16.1克 (0.5分)
烧杯中取用的稀硫酸含水的质量为
50克×(1-19.6%)=40.2克 (0.5分)
10℃时硫酸锌的溶解度为:

答:10℃时硫酸锌的溶解度为47.1克 (0.5分