2009届汕尾市高三化学毕业测试题
可能用到的相对原子质量: H
一.选择题(本题包括9小题,每小题3分,共27分。每小题只有一个选项符合题意)
1.2008年夏季奥运会将在我国举行,这次奥运会要突出“绿色奥运、科技奥运、人文奥运”的理念,其中“绿色奥运”是
A.把环境保护作为奥运设施规划和建设的首要条件
B.严禁使用兴奋剂,使运动员公平竞争
C.所有奥运用品全是绿色的
D.奥运场馆建设均使用天然材料,不使用合成材料
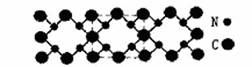 2.氮化碳结构如右图,其中β-氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料。下列有关氮化碳的说法不正确的是
2.氮化碳结构如右图,其中β-氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料。下列有关氮化碳的说法不正确的是
A.氮化碳属于原子晶体
B.氮化碳中碳显-4价,氮显+3价
C.氮化碳的化学式为:C3N4
 D.每个碳原子与四个氮原子相连,每个氮原子与三个碳原子相连
D.每个碳原子与四个氮原子相连,每个氮原子与三个碳原子相连
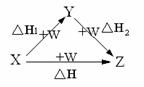
3. X、Y、Z、W有如右图所示的转化关系,已知焓变:
△H=△H1+△H2,则X、Y只可能是
①C , CO ②AlCl3 , Al(OH)3
③Fe , Fe(NO3)2 ④FeBr2 , FeBr3
A.①②③④ B.①②
C.③④ D.①②③
4.下列除去杂质的实验方法不正确的是
A.除去CO2中少量HCl气体:通过饱和NaHCO3溶液后再干燥气体
B.除去Na2CO3固体中少量NaHCO3:置于坩埚中加热
C.除去苯中溶有的少量苯酚: 加入适量浓溴水反应后过滤
D.除去FeCl3酸性溶液中少量的FeCl2:通入稍过量的Cl2
5.下列叙述正确的是
A.0.1mol?L-1氨水中,c(OH-)=c(NH4+)
B.在常温下,10 mL 0.02mol?L-1HCl溶液与10 mL 0.02mol?L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12
C.在0.1mol?L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)
D.0.1mol?L-1某二元弱酸强碱盐NaHA溶液中,c(Na+)=
6.一定温度下的难溶电解质AmBn在水溶液中达到沉淀溶解平衡时,其平衡常数
Ksp=cm(An+)×cn(Bm-),称为难溶电解质的离子积。在
物质
AgCl
AgI
Ag2S
颜色
白
黄
黑
KSP(
1.8×10-10
1.5×10-16
1.8×10-50
下列叙述不正确的是
A.溶度积小的沉淀可以转化为溶度积更小的沉淀
B.若先加入Na2S溶液,再加入KI溶液,则无黄色沉淀产生
C.
D.
7.充分利用能源、提高原子利用率、减少向环境排放废弃物等都是绿色化学基本要求。
① 在有机实验中,用溴的四氯化碳溶液代替溴的水溶液;
②用水浴加热代替直接用酒精灯加热;
③接触法制硫酸中采用“热交换器”,利用余热预热冷原料气和烧水;
④工业合成氨中分离产物得到氢气和氮气再循环使用;
⑤电解法冶炼钠和镁,选择电解氯化钠和氯化镁,不电解对应的金属氧化物。
上述主要不是从绿色化学角度考虑的是
A.①② B.③④ C.④⑤ D.③⑤
8.实验是解决化学问题的基本途径,下列有关实验的叙述不正确的是
A.用苯萃取碘水中的碘时,萃取后的油层不能从分液漏斗下端放出
B.不慎将NaOH溶液溅到皮肤上,应立即用较多的水冲洗
C.用pH计测定中和滴定时溶液中的pH变化,临近滴定终点,每加一滴测一次
D.向FeCl3稀溶液中滴加NaOH溶液,并加热至沸腾,制备Fe(OH)3胶体
9.阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是
A.2.24LCl2中含有的原子数一定为0.2 ×6.02×1023
B.
C.0.88gC3H8中含有的共价键总数目为0.2 ×6.02×1023
D.
二、选择题(本题包括9小题,每小题4分,共36分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给4分,但只要选错一个,该小题就为0分。)
10.下列离子方程式中正确的是
A.过量的NaHSO4与Ba(OH)2溶液反应:
Ba2++2OH-+2H++SO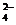 == BaSO4↓+2H2O
== BaSO4↓+2H2O
B.NH4HCO3溶液与过量NaOH溶液反应:NH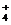 + OH-== NH3↑+
H2O
+ OH-== NH3↑+
H2O
C.苯酚钠溶液中通入少量二氧化碳:
 -O-+CO2+H2O ―→
-O-+CO2+H2O ―→  -OH+HCO
-OH+HCO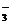
D.FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2 == 2Fe3++Br2+4Cl-
11.下列各组离子中,在所给条件下能够大量共存的是
A.无色溶液中:Na+、MnO4-、SO42-、K+
B.pH=0的溶液中:Fe3+、Mg2+、Cl-、SO42-
C.加入(NH4)2Fe(SO4)2?6H2O晶体的溶液中:Na+、H+、Cl-、NO3-
D.c(H+)=1×10-10 mol/L溶液中:K+、CO32-、Na+、S2-
12.A、B、C和D都是周期表中前20号元素,已知A的阳离子和C的阴离子具有相同的核外电子排布,且能形成组成为AC的化合物;C和D属同族元素,其中C中核外电子数是D中核内质子数的2倍。B和D是同周期元素且A和B能形成AB2型化合物。下列说法中正确的是
A.D元素处于元素周期表中第2周期第Ⅵ族
B.AB2中可能既有离子键又有共价键
C.四种元素的原子半径A>C>D>B
D.BC2分子一定是非极性分子
13.如下图所示两个装置,溶液体积均为200 mL,开始电解质溶液的浓度均为0.1 mol?L-1,工作一段时间后,测得导线上通过0.02 mol电子,若不考虑盐水解和溶液体积的变化,则下列叙述正确的是
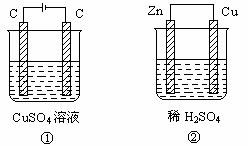
A.产生气体的体积:①>②?
B.电极上析出固体的质量:①>②?
C.溶液的pH变化:①增大,②减小?
D.装置②的电极反应式为:?
①阳极:4OH―-4e-=2H2O+O2↑ ②阴极:2H++2e-=H2↑
14.某有机物含C 52.2%,含H13.0%;该有机物
A.C2H6O
B.C2H4O
15.把6molA气体和5molB气体混合放入
A.x = 2 B.B的转化率为20%
C.平衡时A的浓度为0.8mol/L D.恒温达平衡时容器内压强为开始时的85%
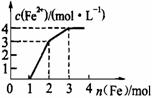 16. 现有含Fe(NO3)3、Cu(NO3)2、HNO3 的某稀溶液, 若向其中逐
16. 现有含Fe(NO3)3、Cu(NO3)2、HNO3 的某稀溶液, 若向其中逐
步加入铁粉,溶液中Fe2+ 浓度与加入铁粉的物质的量之间的关系
如图所示,则该溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度
之比为
A.1∶1∶1 B.1∶3∶1
C.3∶3∶8 D.1∶1∶4
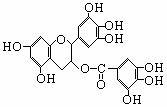 17.美国美国梅奥诊所的研究人员最近发现,绿茶中含有EGCG(表没食子儿茶素没食子酸酯)物质具有抗癌作用,能使血癌(白血病)中癌细胞自杀性死亡,已知EGCG的结构如右图:
17.美国美国梅奥诊所的研究人员最近发现,绿茶中含有EGCG(表没食子儿茶素没食子酸酯)物质具有抗癌作用,能使血癌(白血病)中癌细胞自杀性死亡,已知EGCG的结构如右图:
有关EGCG的说法正确的是
A.EGCG能与碳酸钠溶液反应放出二氧化碳
B.EGCG遇FeCl3溶液能发生显色反应
C.1molEGCG最多可与含10mol氢氧化钠的溶液完全作用
D.EGCG在空气中易氧化
|
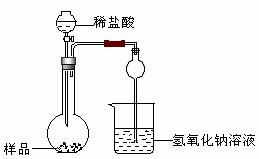
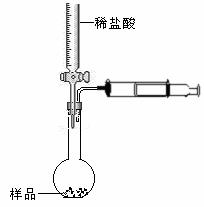
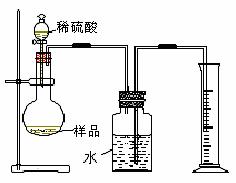
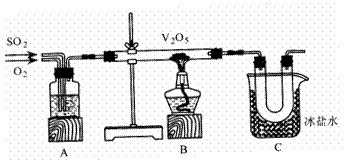
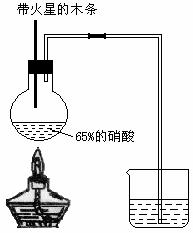
 ⑸老师说该实验装置设计不完整,请你协助该研究小组设计出所缺装置并在右边方框中画出。
⑸老师说该实验装置设计不完整,请你协助该研究小组设计出所缺装置并在右边方框中画出。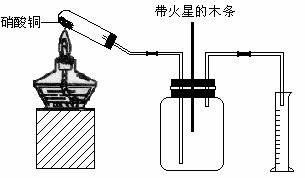
 H2O,一种白色粉末)和生石膏(CaSO4?2H2O,一种坚硬的固体)两种,医生使用的石膏是 (填分子式或名称)。石膏定型时发生的化学反应方程式
。
H2O,一种白色粉末)和生石膏(CaSO4?2H2O,一种坚硬的固体)两种,医生使用的石膏是 (填分子式或名称)。石膏定型时发生的化学反应方程式
。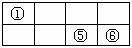 ⑴若①、⑤、⑥三种元素在周期表中相对位置如右图。①与⑤、①与⑥形成的液体化合物是常见的重要溶剂,则这三种元素最高价含氧酸酸性由强到弱的顺序是 。
⑴若①、⑤、⑥三种元素在周期表中相对位置如右图。①与⑤、①与⑥形成的液体化合物是常见的重要溶剂,则这三种元素最高价含氧酸酸性由强到弱的顺序是 。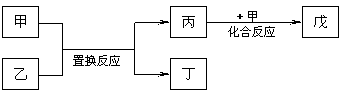
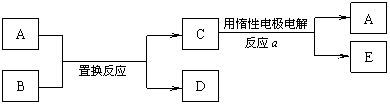 若下图中A是常见的金属单质,B、C、D、E分别是上述9种元素中的某些元素组成的单质或其中两种元素组成的化合物。
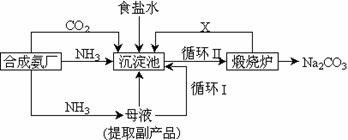
若下图中A是常见的金属单质,B、C、D、E分别是上述9种元素中的某些元素组成的单质或其中两种元素组成的化合物。 24.(13分)工业上合成氨是在一定条件下进行如下反应:N2(g)+3H2(g)
24.(13分)工业上合成氨是在一定条件下进行如下反应:N2(g)+3H2(g)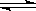 2NH3(g),其部分工艺流程如下:
2NH3(g),其部分工艺流程如下: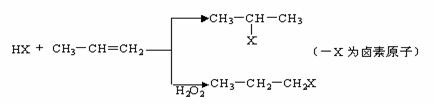
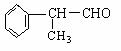 苯的同系物与卤素单质混合,在光照条件下,侧链上的氢原子被卤素原子取代;在催化剂的作用下,苯环上的氢原子被卤素原子取代。
苯的同系物与卤素单质混合,在光照条件下,侧链上的氢原子被卤素原子取代;在催化剂的作用下,苯环上的氢原子被卤素原子取代。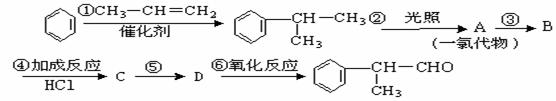
 26.(10分)TBC是优良的增塑剂,具有很好的相容性,且挥发性小、耐寒、耐光及耐水等,广泛用于医学卫生用品,它的结构式如右图,合成时柠檬酸与正丁醇合成数据如下:
26.(10分)TBC是优良的增塑剂,具有很好的相容性,且挥发性小、耐寒、耐光及耐水等,广泛用于医学卫生用品,它的结构式如右图,合成时柠檬酸与正丁醇合成数据如下: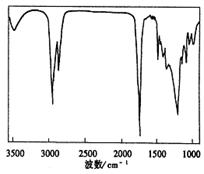 试回答下列问题
试回答下列问题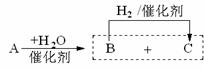 ⑷柠檬酸的一种同分异构体A,能发生如右图转化:
⑷柠檬酸的一种同分异构体A,能发生如右图转化: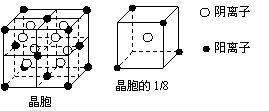 ⑴A和E所形成的化合物的电子式是
。
⑴A和E所形成的化合物的电子式是
。

 O2(g)
O2(g) 

 21.(共11分)
21.(共11分) ⑵正确,(1分)2Cu(NO3)2分解产生的混合气体中O2的体积分数与空气中O2的体积分数相当空气中带火星的木条不复燃,而在NO2和O2混合气体中木条复燃,所以NO2能支持燃烧。(2分)
⑵正确,(1分)2Cu(NO3)2分解产生的混合气体中O2的体积分数与空气中O2的体积分数相当空气中带火星的木条不复燃,而在NO2和O2混合气体中木条复燃,所以NO2能支持燃烧。(2分) H2O+3H2O===2CaSO4?2H2O(2分)
H2O+3H2O===2CaSO4?2H2O(2分) 





 (1分) (2)由于HF分子间存在氢键(2分)
(1分) (2)由于HF分子间存在氢键(2分) =
=