第四单元《物质构成的奥秘》测试
考试时间100分钟 共100分
可能用到的相对原子质量: N:14 H:1 O:
一、选择题(每空2分)
1.为了预防缺铁性贫血,人体必须保证摄入足够的铁,这里的“铁”是指( )
A.铁单质 B.铁元素 C.铁原子 D.氧化铁
2.下列试剂瓶标签上的化学式书写错误的是 ( )




3.下列粒子在人体中起着重要的作用,其中属于阴离子的是 ( )
A.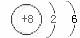 B.
B.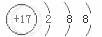
C.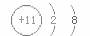 D.
D.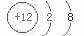
4.“王水”溶解黄金后得到一种物质:HAuCl4(四氯合金酸),其中金元素的化合价为:( )
A.+1 B.+
5.某些花岗岩石材中含有放射性元素氡。一种氡原子的质子数为86,中子数为136,这种氡原子核外电子数为( )
A.50 B.
6.下列符号中既表示一个原子,又表示一种元素,还表示一种物质的是( )
A.C60 B.2H C.2H2 D.Hg
7.下列物质中,含有氧分子的是( )
A.KMnO4 B.H2O
8.下图是表示物质分子的示意图,图中“●”和“○”分别表示两种含有不同质子数的原子,则图中表示单质的是( )
A.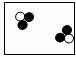 B.
B.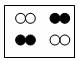 C.
C. D.
D.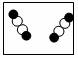
9.化学式H2O所表示的意义中,错误的是( )
A.表示水这种物质
B.表示一个水分子
C.表示水由氢氧元素组成
D.表示一个水分子由2个氢元素和一个氧元素组成
10.1996年发现C60后,C70也已制得。下列有关C70说法正确的是( )
A.它是一种化合物 B.它是一种混合物
C.它是一种单质 D.它的相对分子质量是
二、选择题 (本题5小题,每小题只有一个正确答案,每小题2分,共10分)
11.据报道,国家有关部门对家庭装饰材料进行抽样,发现有毒气污染材料,甲醛就是其中一种,它的化学式CH2O,下面关于甲醛的叙述正确的是( )
A.甲醛由三种原子构成
B.甲醛由碳、氢、氧三种元素组成
C.甲醛中碳、氢、氧三种元素的质量比为1:2:1
D.甲醛中氢元素的质量分数约为53.3%
12.纽约大学的科学家最近研制出有“双腿”,能在盘子里“散步”的分子机器人,它是由26个氨基酸(含C、H、N等元素) 结合而成的多肽分子,下列说法正确的是( )
A.这种分子机器人是一种新型分子
B.我们已可以用肉眼直接看到这种分子“散步”
C.分子本身是不会运动的,其“散步”一定是在人的推动下进行的
D.这种分子组成的物质是一种单质
13.下列五种物质中均含有碘元素,它们按碘的化合价的顺序排列:① KI ② I2 ③ HIO ④ X ⑤NaIO4,则根据这种排列规律,X不可能的是( )
A.I2O5 B.KIO
14.不纯的硝酸铵(NH4NO3)中氮的质量分数为此36%,则此硝酸铵(NH4NO3)中混入杂质可能是( )
A.NH4HCO3 B.(NH4)2SO
15.雷雨后的空气十分新鲜 ,这是因为空气中有极少量的氧气(O2)转化成臭氧(O3)的缘故,下列说法中错误的是( )
A.该变化是化学变化 B.O2和O3均为氧的单质
C.O2和O3是同种物质 D.O2和O3是不同种物质
16.下列说法错误的是( )
A.氧化物中一定含有氧元素 B.“2Fe2+”表示2个铁离子
C.质子数相同的微粒属于同种元素 D.相对原子质量的国际单位制单位为1
17.下列物质中铁元素的质量分数由高到低排列顺序正确的( )
A.FeO>Fe2O3 >Fe3O4>FeS B.Fe2O3>FeO>Fe3O4 >FeS
C.Fe3O4 >Fe2O3 >FeO>FeS D.FeO>Fe3O4>Fe2O3 >FeS
18.现代医学证明,人类牙齿有一层为碱式磷酸钙的坚硬物质保护着,碱式磷酸钙分子中除钙离子外,还有一个氢氧根离子和三个磷酸根离子(PO43-),则碱式磷酸钙的化学式是( )
A.Ca2(OH)(PO4)3 B.Ca3(OH)(PO4)3
C.Ca4(OH)(PO4)3 D.Ca5(OH)(PO4)3
19.由以下粒子结构示意图得出的结论中,错误的是( )
(1) (2)
(2)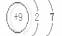 (3)
(3)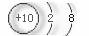
(4)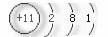 (5)
(5)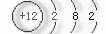
A.①和②分别与④或⑤反应,均能形成与③电子层结构相同的粒子
B.上述粒子间能形成AB型,AB2型、A2B型化合物
C.上述粒子形成化合物前后,质子总数,电子总数均发生变化,而质量不变
D.上述粒子形成化合物后,在化合物中均能显示可变化合价
20.有两种粒子,它们的质子数相等,核外电子数也相等,下列关于这两种粒子的说法错误的是( )
A.可能是一种分子和一种原子 B.可能是两种不同的离子
C.可能是一种分子和一种离子 D.可能是两种不同的分子
三、填空题: (除第21题每空1分外,其余每空2分 ,共 20 分):
21.用化学用语(符号)表示:
石灰水中的溶质是_________;人体内含量最多的元素是_________;3个氮原子_________;2个钙离子_________;2个硫酸根离子_________;
下列化学用语均有错误,请将正确的化学用语写在相应的横线上:
氯元素Cl_________;2个氧分子2O_________;铁离子Fe2+_________;
22.下图表示的是地壳里所含各种元素的含量。请根据下图回答下列问题:
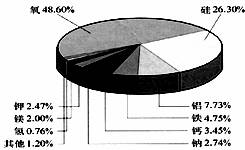
⑴图中表示出的金属元素有 种;
⑵地壳中含量最多的非金属元素是______(填元素符号),它与含量占第一位的金属元素之间所形成化合物的化学式是 。
23.下图形象地表示了在高温催化剂条件下,某化学反应前后反应物与生成物分子及其数目的变化,其中 表示硫原子
表示硫原子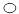 表示氧原子则该反应的化学符号表达式为:
。你还可以由此得到哪些信息: 。(至少写两条)
表示氧原子则该反应的化学符号表达式为:
。你还可以由此得到哪些信息: 。(至少写两条)
24.(4分)手机中使用的锂电池电板是新型的高能电池,以质量轻、电容量大而受到普遍重视。目前已制成多种功能的锂电池,某种锂电池的总反应可表示为Li+MnO2=LiMnO2在上述反应中锂元素的化合价从0价转变为_________价,锰元素的化合价从+4价转变为_________价。
四、简答题(6分)
25.用分子、原子的观点解释下列问题:
(1)用铝壶烧水时,水开了会将壶盖顶开。
(2)一杯水敞口放在空气中,一周后,杯子里的水不见了。若将这杯水烧开,一会儿整杯子的水就消失了。
(3)加油站里的汽油贮存在油罐里,但在离油罐一定距离内仍要“严禁烟火”
五、我会分析 (每空2分共 22分):
26.下列是生物细胞中的元素含量分布表:
元素
质量分数%
元素
质量分数%
元素
质量分数%
元素
质量分数%
氧
65
氮
3
钾
0.35
镁
0.05
碳
18
钙
1.5
硫
0.25
铜、锌、硒、钼、氟、氯、碘、钴、锰、铁
0.70
氢
10
磷
1.0
钠
0.15
其他
微量
生活中人们喜爱吃精细的食物,饮用纯净水。可有人提出了应提倡多食粗食,饮用白开水,我认为___________________________原因是 ________________。
27.上海已建成我国第一条磁悬浮技术,是利用超导体的反磁性,高温超导物质(Y2Ba4Cu6O13)是以YmOn、BaCO3和CuO为原料,经研磨烧结合成(此过程中所有 元素的化合价均不变)。
(1)高温超导物质(Y2Ba4CuO13)是由_________种元素组成,其中Y是_________价,YmOn的化学式是_________。
(2)在合成该高温超导物质的同时,还生成另一种物质,该物质是_________。
28.已知碘元素符号为I,它的原子结构示意图为:
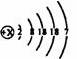
请结合所学知识,填写下列空白:
(1)X的值为________;
(2)碘元素的化学性质与下列哪种元素的化学性质最相似?________(填序号)。
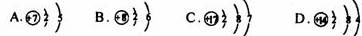
29.1911年,卢瑟夫用一束平行高速运动的α粒子(α粒子带正电荷)轰击金箔时,发现三种实验现象,请回答:
按照示例方式,提出解释实验现象的原因。
实验现象
产生现象的原因
(1)一小部分α粒子改变原来的运动路径。
α粒子途经金原子核时,受到斥力而改变原来的运动方向。
(2)大多数α粒子不改变原来的运动方向。
(3)极少数α粒子被弹回来。
由此可推出关于原子内部结构的一些假设:( )
A.原子核体积较大 B.原子内部有很大的空间
C.原子是一个实心球体 D.原子核与α粒子带有相同的电荷
六、科学探究:(6分)
30.为了防治“非典”,常用过氧乙酸做消毒剂,过氧乙酸的化学式为CH3COOOH,从过氧乙酸的化学式中,你可以知道哪些信息?
31.为了履行国际社会的<<关于消耗臭氧层物质的蒙特利尔议定书>>,我国政府决定自2003年6月1日 起在全国范围内禁止使用“CTC”作为清洗剂。“CTC”又称四氯化碳,是常用的服装干洗剂,也是修正液(又称涂改液)中的一种溶剂,还是一种优良的灭火剂。根据以上信息回答:
(1)“CTC”的化学式为____________,其中碳元素的化合价为______。
(2)推测“CTC”的物理性质和化学性质各一种。
物理性质:________________________。
化学性质:________________________。
七、我会计算 :(6分)
钙≥0.11g
脂肪≥3.3g
蛋白质≥2.9g
(1)包装标签上脂肪3.3g,是指100ml牛奶中含脂肪的质量至少为3.3克,那么一盒牛奶含钙至少为多少克(保留到0.01克)?
(2)求羟基磷酸钙中钙元素的质量分数(保留到0.1%)?
(3)若人体每天至少需要0.6克钙,且这些钙有90%来自牛奶,则一个人每天至少要喝多少盒牛奶?