2009年四川省资阳市高中阶段学校招生统一考试
化学试卷
(满分l50分,考试时间l20分钟)
可能用到的相对原子质量:H一1
He一4
Li一7
Be一9
B一
第Ⅰ卷(选择题 共51分)
一、选择题
3.下列关于水的说法不正确的是 ( )
A.水是由氢、氧两种元素组成的
B.地球表面的水不少,但可供人类生存所需的淡水却不多
C.欲从食盐水中把水分离出来,最好采用蒸馏方法
D.软水一定是纯水
4.下列关于人体健康的叙述不正确的是 ( )
A.蛋白质、维生素等是维持生命的重要营养物质,因此不要偏食,以保持营养平衡
B.钙、铁、锌、碘都是人体必需的元素,食用含这些元素的药品越多越好
C.吸烟有害健康,因烟气中的尼古丁和CO等是有毒物质
D.食用无污染的绿色食品,有利身体健康
5.下列关于生活中常见物质的认识不正确的是 ( )
A.化学中的盐不只是食盐
B.生石灰和熟石灰是同一种物质
C.纯碱不属于化学中的碱
D.食醋不是纯净物
6.现有X、Y、Z三种金属单质,根据下列叙述作出判断,这三种金属依次可能是( )
①将X放入盐酸中,无任何现象
②Z在潮湿的空气中易锈蚀
③将Y和Z分别放入XSO4溶液中,均有X析出,且Y的反应更快
A.Cu、Zn、Fe B.Al、Fe、Cu C.Ag,Cu,Fe D.Zn、Fe、Cu
7.2008年震惊中华大地的三鹿毒奶粉事件,是造假者在牛奶中掺入了廉价的三聚氰胺(分子结构如图)。下列关于三聚氰胺的说法不正确的是 ( )
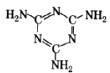
A.其化学式为C3H6N6
B.其中C、H、N元素质量比为6:1:14
C.其N元素的质量分数为93.3%
D.该分子中共有15个原子核
8.将下列各物质(或溶液)中的少量杂质(括号内为杂质)除去的操作不正确的是( )
A.食盐(泥沙)――溶解于水、过滤、蒸发
B.硝酸溶液(硫酸)――加入适量Ba(NO3)2溶液,过滤
C.氧气(水蒸气)――将气体通过浓硫酸
D.NaOH溶液(Na2CO3)――加入适量盐酸
9.在溶液中发生AB+CD―AD↓+CB类型的反应,下列说法不正确的是( )
A.该反应类型属于复分解反应
B.A在反应前后的化合价无变化
C.D一定是原子团
D.若AB是AgNO3,则CD可能是NaCl
25.(4分)根据元素周期表中原子序数为1~18的元素,选择相应的元素填写符合题目要求的化学式:
(1)通常情况下,单质密度最小的物质:_____________;
(2)一种具有强腐蚀性的、由3种元素组成的、其水溶液pH小于7的物质:____________;
(3)化学实验室常用的固体药品之一,俗称火碱的物质:______________;
(4)一种叫铵盐的化学肥料:___________。
26.(3分)最近在我省达州发现一大型海相整装气田,是我国继新疆塔里木、内蒙古鄂尔多斯之后的三大气田之一,现已探明天然气储量6 600亿立方米,远景储量达3.8万亿立方米。
(1)天然气属于_________能源,其主要成分是(填化学式)_______________;
(2)我省由于天然气储量丰富,许多城镇居民都以天然气作为生活能源,因而用气安全尤为重要。若夜晚回家,闻到有天然气味(实际为天然气中加入的硫醇气味,便于查漏),说明有天然气泄漏,这时你要做的第一件事是(选填序号)____________。
①用打火机照亮,查看情况 ②打开电灯,查找泄漏点
③打开门窗通气 ④用手机打电话,通知专业人员处理
27.(4分)下图为A、B两物质的溶解度曲线,据此作答:
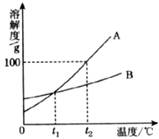
(1)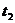 ℃时,A、B两物质溶解度大小比较,A______B(填“<”“>”或“=”);
℃时,A、B两物质溶解度大小比较,A______B(填“<”“>”或“=”);
(2)等质量A和B的饱和溶液由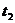 ℃降低温度到
℃降低温度到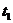 ℃时,析出溶质较多的是________;
℃时,析出溶质较多的是________;
(3)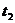 ℃时,
℃时,
28.(4分)氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于大规模集成电路生产、陶瓷工业等领域。
(1)铝的原子结构示意图为: ,铝原子核内中子数比质子数多1,则铝原子的中子数为_________;
,铝原子核内中子数比质子数多1,则铝原子的中子数为_________;
(2)氮化铝陶瓷属于(选填序号)_________;
①有机合成材料 ②金属材料 ③无机非金属材料
(3)工业上制氮化铝,是从铝土矿中获得氧化物X;通过净化、液化空气,控温蒸发得到N2;X与N2和碳在一定条件下反应制得AlN和CO。氧化物X的化学式为_________,制AlN的化学方程为_____________。
29.(2分)漂白粉具有消毒杀菌作用,其有效成分为Ca(ClO)2,工业制漂白粉是用氯气与石灰乳反应,化学方程式表示为:2Cl2+2Ca(OH)2==Ca(ClO)2+X+2H2O。
(1)物质X的化学式为______________________________________________;
(2)石灰乳在空气中长期存放易变质发硬,写出石灰乳在空气中变质的化学方程式:________________________________________________________________。
30.(7分)初中化学中的常见四种物质:A、B、C、D,它们有如图所示转化关系。A、D是单质,A为固体,B、C、D常温下都是无色气体。
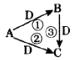
(1)自然界有多种A,其中一种可导电的A名称为___________;
(2)①、②、③反应属于化学反应基本类型中的__________反应;
(3)C溶于水,部分与水发生反应。证明C与水发生了反应的方法是: _________
___________________________________________________________________________。
(4)按下列要求写出得到C物质的化学方程式(反应物可自定):
分解反应的方法得到C:_________________________________________________;
复分解反应的方法得到C:_______________________________________________;
由B还原氧化铜得到C:__________________________________________________。
三、探究与实验题
34.(4分)下图是实验室制取气体时常用的仪器(选择仪器时,填仪器代号)。
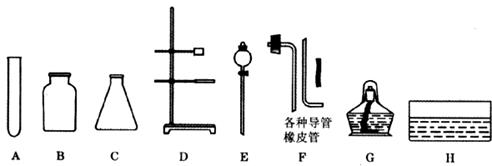
(1)若用排水法收集较多氧气时,最好选用的仪器有:___________________________;
(2)若用C、E、F组合成制气装置,你可以用它制得的气体有(知道的都写)__________;
(3)实验室用双氧水制O2的化学方程式是:____________________________________;若反应装置对反应是可控制的,则双氧水应装入仪器________中。
35.(6分)空气中氧气含量的实验探究,是利用可燃物燃烧消耗氧气来粗略测定其体积分数的。课本中是用燃烧红磷的方法来进行的实验探究(如图甲)。
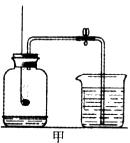
【提出问题】能用燃烧硫磺(单质硫)来测定空气中氧气的体积分数吗?
【猜想与假设1】甲同学认为不能。假设用硫燃烧,燃烧后的产物为_________,是气态物质,不适宜用该实验方法测定。
【猜想与假设】乙同学认为能。假设用硫燃烧,根据现有化学知识,只要消耗硫燃烧后的产物就同样能粗略测定空气中氧气的体积分数。
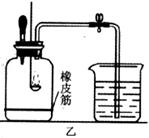
【设计与实验】将原装置改为如图乙的实验装置,烧杯和滴管中的液体为__________。 当硫磺燃烧至火焰熄灭并冷却后,打开止水夹,挤压滴管,滴入几滴液体,此时可观察到烧杯中的液体吸入集气瓶中,流入液体的体积大约在集气瓶的橡皮筋处。液体流入集气瓶中后发生反应的化学方程式为:_________________________________________________;
【结论】_________________________________________________________________。
【评价与反思】①燃烧红磷与②燃烧硫磺两种测定空气中氧气含量的方法,最好选用(选填方法代号)_________的方法;原因是_____________________________________________
___________________________________________________________________________。
四、论证与计算题(本大题包括3小题,共19分)
38.(5分)准确量取密度为
(1)稀释后硫酸溶液的质量分数是多少?
(2)滴加NaOH溶液中和稀释后的硫酸溶液,当混合溶液pH等于7时,发生反应的NaOH的质量是多少?