2009年江苏名校高中单独招生考试(二)
化学试题
说明:本试题满分70分,考试时间60分钟。
一、选择题(本题包括12小题,每小题有1个或2个选项符合题意。若有两个答案的错1个不得分。漏选1个扣2分。每小题3分,共36分)
1.下列做法或说法合理的是
A.正常雨水的pH约为5.6的原因:
B.用甲醛浸泡水产品
C.用含小苏打的发酵粉焙制糕点
D.水沸腾时可掀起壶盖,说明分子大小随温度升高而增大
2.下列各组物质反应后,溶液的总质量减少的是
A.氨气通入稀硝酸中 B.二氧化碳通入过量石灰水中
C.铁粉加入到稀硫酸中 D.锌粒加入到硫酸铜溶液中
3.小玲同学对所学部分化学知识进行了如下归纳,其中有错误的一组是
A.物质的性质和用途
B.安全常识
N2性质稳定――填充食品袋防腐
乙醇具有可燃性――可用作燃料
CO具有还原性――可冶炼金属
居室装修――常开窗通风,防甲醛中毒
电器着火――用泡沫灭火器
煤气泄漏――关闭气阀、严禁烟火
C.元素与人体健康
D.日常生活经验
缺铁――易引起贫血
缺钙――易得佝偻病或骨质疏松
缺碘――易得甲状腺肿大
区别硬水与软水――常用肥皂水检验
区分羊毛纤维与合成纤维――灼烧后闻气味
点石成金――指石灰石能变成黄金
4.下列四个图像反映的变化趋势,分别对应四种操作过程,其中正确的是

A.某温度下,向一定量接近饱和的硝酸钾溶液中不断加入硝酸钾晶体
B.向氯化铁和盐酸的混合溶液中加入过量的氢氧化钠溶液
C.用相等质量的双氧水来制取氧气
D.氢氧化钠溶液中加足量的水稀释
5.下图为某固体溶解度随温度变化的曲线。该固体从溶液中析出时不带结晶水。M、N两点分别表示该固体形成的两份溶液在不同温度时的浓度。当条件改变时,溶液新的状态在图中对应的点的位置可能也随之变化,其中判断不正确的是
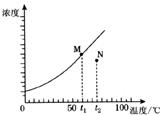
A.都升温
B.加水稀释(假设温度都不变)时,M、N点均不动
C.都降温
D.蒸发溶剂(假设温度都不变)时,先是M点不动,N点向上移至曲线;继续蒸发溶剂,M、N点都不动
6.密闭容器内有M、N、P、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表,下列说法正确的是
物 质
M
N
P
Q
反应前质量/g
19.7
8.7
31.6
0.4
反应后质量/g
待测
17.4
19.7
3.6
A.反应后密闭容器中M的质量为
B.该反应一定是化合反应
C.物质P一定是化合物
D.反应生成的N与Q的质量之比为87┱18
7.下表是元素周期表中部分元素的相关信息,根据有关信息判断不正确的是

A.同一族的元素对应的原子从上往下电子层数在逐渐增加
B.同一周期的元素对应的原子的电子层数相同
C.第ⅠA的元素不一定都是金属元素
D.同一周期的元素的金属性逐渐增强
8.把铁粉和氧化铜的混合物加入到一定量的盐酸中,充分反应后,过滤。在滤液中加入少量铁粉,无现象。则下列判断正确的是
A.滤渣中一定含铜 B.滤液中可能含FeCl2和HCl
C.滤渣可能是铜和铁的混合物 D.滤液中一定含FeCl2和CuCl2
9.
A.只含碳、氢两种元素
B.含有碳、氢、氧三种元素
C.含有碳、氢两种元素,可能含氧元素
D.含有碳、氢两种元素,不含氧元素
10.下列各物质,无论以何种比例混合,其氯元素的质量分数不变的是
A.HClO4、KClO3 B.NaClO、KCl
C.KClO、KCl D.NaCl、KCl
11.下列图像能正确反映所对应叙述关系的是

A.图A表示一定量的木炭还原氧化铜,剩余固体质量与反应时间的关系
B.图B表示 ℃时,向饱和硝酸钾溶液中加入硝酸钾晶体,溶质质量分数与加入量的关系
℃时,向饱和硝酸钾溶液中加入硝酸钾晶体,溶质质量分数与加入量的关系
C.图C表示一定量的稀硫酸与锌粒反应,溶液的质量与反应时间的关系
D.图D表示向硫酸和硫酸铜混合溶液中加入氢氧化钠,沉淀质量与加入量的关系
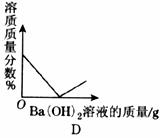
12.向装有 溶液至过量。有关量的变化情况见下图(横坐标表示氢氧化钡溶液的质量,纵坐标表示小烧杯中量的变化)。其中肯定不正确的是
溶液至过量。有关量的变化情况见下图(横坐标表示氢氧化钡溶液的质量,纵坐标表示小烧杯中量的变化)。其中肯定不正确的是



二、填空题(本题包括3个题,共24分)
13.(8分)在“食盐、葡萄糖、硝酸钾、纯碱”中选择适当物质的化学式填空:
(1)人体重要的能量来源___________;
(2)可用作调味品和防腐剂___________;
(3)农业上可作复合肥料使用___________;
(4)其水溶液pH大于7___________。
14.(10分)铁是自然界分布最广的金属元素之一,在地壳中的质量约占5%左右。铁矿石的种类很多,重要的有磁铁矿石(主要成分Fe3O4)、赤铁矿石(主要成分Fe2O3)等。
(1)高炉中用赤铁矿炼铁的主要化学方程式为_____________________________,其中氧化铁中的氧被夺去,发生___________反应。分析该反应中各元素的化合价可知;物质发生氧化反应的元素,其化合价会___________(填“升高”“降低”或“不变”)。
(2)在常温下,铁跟水不起反应。但是,在水和空气里的氧气等共同作用下,铁容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。刷油漆是重要的防腐蚀措施之一,油漆防腐蚀的主要原理是______________________。
(3)铁元素是人体的重要营养元素,举一例说明铁元素在人体中的重要作用:______ __________________________________________________________。
15.(6分)某化学兴趣小组设计了下列三组实验装置,试图通过观察实验现象说明CO2与NaOH溶液可能发生了反应。
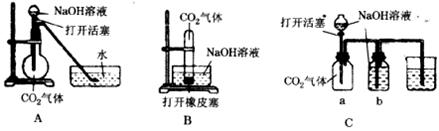
(1)请写出CO2与过量的NaOH发生反应的化学方程式______________________。
(2)选择任意一组装置,简述预计出现的实验现象,解释产生该现象的原因:_______________________________________________________。
三、综合运用(10分)
16.(10分)食盐是日常生活的必需品,也是重要的化工原料。一同学用某种粗盐进行提纯实验,步骤如下图所示。
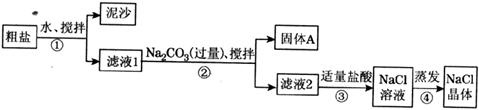
请回答:
(1)步骤①和②的操作名称是______________________________。
(2)步骤④加热蒸发时要用到玻璃棒不断搅拌,这是为了防止__________________。
(3)猜想和验证:
猜想
验证方法
实验现象
结论
猜想Ⅰ:固体A中含CaCO3
取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口
__________
猜想Ⅰ成立
猜想Ⅱ:固体A中含BaCO3
取少量固体A于试管中,先滴入__________,再滴入Na2SO4溶液
有气泡放出,无白色沉淀
__________
猜想Ⅲ:最后制得的NaCl晶体中还含有Na2SO4
取少量NaCl晶体于试管中,加适量蒸馏水溶解,再__________
__________
猜想Ⅲ成立
(4)我省生产的某种钙盐的配料表如下:氯化钠、食用碳酸钙、碘酸钾。为了测定此盐中的钙元素含量,取