2009年泰安市高中阶段学校招生考试
化学试卷
注意事项:
1.答卷前将密封线内的项目填写清楚。
2.本试题共6页,满分50分。物理、化学合场,考试时间120分钟。
相对原子质量:H l C 12 N 14 O 16 Na
一、选择题(本题包括10小题,1~5题每小题1分,6~10题每小题2分,共15分。每小题只有一个选项符合题意,请将符合题意的选项序号填入下面相应的空格内)
1.小军同学在做家庭小实验时.向热的大米粥中加入碘酒,发现未变蓝色。面对“异常”现象,他不应该采取的做法是
A.向老师请教 B.查找相关资料,探究原因
C.反复实验。并观察是否有相同现象D.认为自己做错了,继续做其它实验
2.物质的性质决定它的用途,还决定其保存方法。固体KOH具有以下性质:①白色固体
②有腐蚀性③易吸收水分④能与空气中的二氧化碳反应。实验室中必须将它密封保存的主要原因是
A.①② B.③④ C.①③ D.②④
3.图表资料可以为我们提供很多信息。下列从图表中获取的信息及应用不正确的是
A.根据金属的熔点数据表.可判断金属的导电性强弱
B.根据金属活动性顺序表,可判断金属是否容易被盐酸腐蚀
C.根据元素周期表,可查找元素的原子序数、元素符号、相对原子质量等信息
D.根据空气质量报告,可知道空气质级别和首要污染物
4.正确的化学实验操作对实验结果、人身安全非常重要。下图中的实验操作正确的是
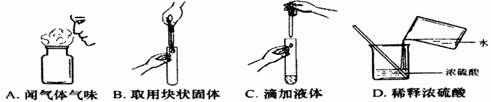
5.“关爱生命,拥抱健康”是永恒的主题。下列做法不利于人体健康的是
A.多食水果和蔬菜,给人体补充维生素 B.向易变质食品的包装袋中充入氯气
C.胃酸过多的人应少喝汽水 D.用甲醛溶液浸泡海产品,以防其变质
6.下图是甲、乙两种固体物质的溶解度曲线。
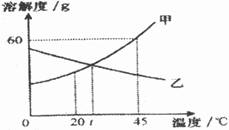
下列说法正确的是
A.甲物质的溶解度为
B.t℃时,甲、乙两物质的溶解度相等
C.升高温度可使不饱和的甲溶液变为饱和
D.乙物质的溶解度随温度的升高而增大
7.化学时刻影响着我们的生活。它在工农业生产和日常生活中起到了非常重要的作用。下列说法中正确的是
A.发现燃气(天然气、煤气或液化石油气等)泄漏,点火检查出泄漏处
B.棉花、羊毛、塑料和天然橡胶等均属于天然有机高分子材料
C.熟石灰可以改良酸性土壤,但不能和硫酸铵混合使用
D.木炭燃烧的剧烈程度由它的着火点决定,而与氧气的浓度无关
8.下图表示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含与不包含关系,若整个大圆圈代表纯净物,则在下列选项中,能正确指出①、②、③、④所属物质类别的是
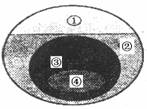
A.②化合物、④氧化物 B.①单质、③氧化物
C.①单质、③化合物 D.②含氧化合物、④氧化物
9.下列对相应现象或事实的解释不正确的是
选项
现象或事实
解释
A
金刚石和石墨的性质差异较大
两者的原子排列方式不同
B
酒香不怕巷子深
分子不断的运动
C
温度计中的水银(汞)热胀冷缩
原子的大小发生改变
D
用于冰进行人工降雨;用铜制作导线
都是利用物质的物理性质
10.用氯化钠固体配制
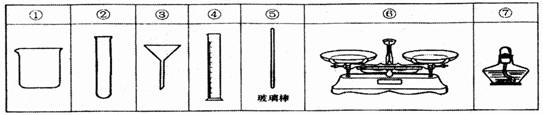
A.②④⑥⑦ B.①④⑤⑥ C.①③⑤⑦ D.①②④⑦
二、(本题包括5小题,共18分)
11.(3分)化学用语是化学学科的专用语言.是我们学习化学的重要工具。请你从给定化
+1 0 -2 +5 +1
合价的K、Cu、 O、N、H五种元素中,选择适当的元素,按要求写出相应物质的化学式(每空只填一种物质):
单质 ;金属氧化物 ;可作为复合肥料的盐 。
12.(3分)化学和我们的日常生活息息相关,化学科学的发展促进了人类社会文明的进步,提高了人们的生活质量。
通过化学学习,我们已经认识了很多化学反应,请你用化学方程式解释下列问题:
(1)不用铁桶盛放波尔多液的原因
(2)用石灰乳粉刷墙壁能形成坚硬的墙面
(3)用盐酸除去铁制品表面的铁锈
13.(2分)锂元素(元素符号为Li)及其所形成的化合物。在通讯和航空航天领域中具有极其重要的用途。它的化合物氢氧化锂(LiOH)是一种易溶于水的白色固体,有辣味,具有强碱性和腐蚀性。
(1)写出氢氧化锂的一条物理性质 ;
(2)下表是部分物质的溶解性表.运用此溶解性表并结合你对复分解反应发生条件的理解,
 阴离子
阴离子
阳离子
CO32-
SO42-
NO3-
Ba2+
溶
不
不
溶
Cu2+
不
不
溶
溶
Li+
溶
微溶
溶
溶
从表中选出一种盐,该盐能和LiOH发生复分解反应,请你写出该盐的化学式 。
14.(4分)泰安的豆腐闻名遐迩。豆腐制作是中国古代的一项重要发明,现在豆腐在全球已成为颇受欢迎的食品,其制作的主要工艺流程通常如下:
【资料】下表是豆腐中主要成分的平均质量分数:
成分
水
蛋白质
油脂
糖类
钙
磷
铁
维生素B1
维生素B2
质量分数/%
89.3
4.7
1.3
2.8
0.24
0.064
1.4
0.00006
0.00003
请回答下列问题:
(1)上述工艺流程中,磨浆属于 (填“物理”或“化学”)变化,由豆腐花制豆腐的过程就是将豆腐与水分离,该过程利用的操作名称是 。
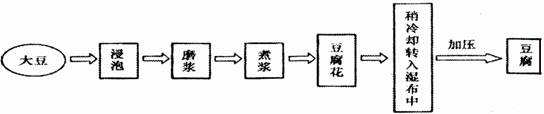
(2)除水、无机盐和维生素外,豆腐中还含的营养素有 ,含人体所需的微量元素是 。
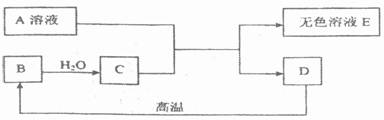
15.(6分)A、B、C、D为中学化学中常见的物质,其中A为含三种元素的钠盐,其水溶液pH大于7.B可用作固体干燥剂。D是相对分子质量为100的白色不溶物。它们的相互关系如下图所示:
请填写下列空白:
(1)A B D (填写化学式);
(2)D转化为B的反应类型为 (填基本反应类型);
(3)E中一定含有的溶质是 ,理由是 (用化学方程式表示)
三、(本题包括2小题,共10分)
16.(5分)为了制取少量的氧气,化学兴趣小组的同学把工作分为以下三个阶段。
I 查阅资料,获得信息:过氧化氢、氯酸钾、高锰酸钾等含有氧元素的物质在一定条件下分解都可以产生氧气,其中过氧化氢价格最低,在常温下就能够分解放出氧气,该过程无副产物;氯酸钾价格较高。分解较困难.且常伴有副产物;高锰酸钾价格较高,加热即可快速分解。二氧化锰能加速上述三种物质的分解。
根据上述信息,确定制取氧气的实验方案。
Ⅱ组装仪器,进行实验。可供选择的实验装置如下:
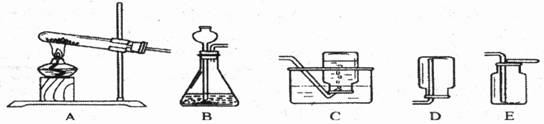
Ⅲ 实验完毕,洗刷仪器,整理用品,总结实验,完成实验报告。
(1)要制取一瓶氧气,你认为应选择的最佳实验装置是 (填写字母代号),
组装好实验装置后首先应 。
(2)有气体产生的化学反应在有限的空间里发生时,如果反应速度过快,容易引起爆炸。
在用过氧化氢和二氧化锰制氧气的实验中,为预防爆炸应采取的措施是(列举两条);
(3)回顾整个工作过程,你认为在准备工作阶段除应考虑药品的价格、制氧气反应的难易、制氧气过程的安全性等因素外。还应考虑的因素是(一条即可)。
17.(5分)如图所示,某同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液滴加稀盐酸一会儿后,发现忘记了滴加指示剂。为了确定盐酸与氢氧化钠是否恰好完全反应,她从烧杯中取了少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液.振荡.观察到酚酞试液不变色。于是她得出“两种物质已恰好完全中和”的结论。
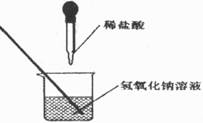
(I)你认为她得出的结论是 的(填“正确”或“错误”),理由是
(2)请你设计一个实验.探究上述烧杯中的溶液是否恰好完全中和。 请填写下表:
实验方法
可能观察到的现象
结 论
四、(本题包括2小题。共7分)
18.(3分)制作“叶脉书签”需要l
请问:
(I)配制时需要氢氧化钠固体的质量是 g.水的质量是 g;
(2)若用20%的氢氧化钠溶液和水配制,需要20%的氢氧化钠溶液质量是 g。
19.(4分)甲醇(CH3OH)有毒,误饮可使眼睛失明,甚至死亡。最新研究证明用氨气(NH3)处 理含有甲醇的工业废水,能使其转变成无毒的物质。
有关反应的化学方程式为:5CH3OH+12O2+6NH3 3B+5CO2+19H2O
3B+5CO2+19H2O
(1)上述反应中B物质的化学式为 ,甲醇中氧元素的质量分数为 。
(2)若处理含有0.32%甲醇的工业废水500t.理论上需要氨气多少吨?
(计算结果精确到0.01)