2008-2009学年度潍坊市高密第一学期九年级期中考试
化学试卷
(时间:60分钟 满分:100分)
可能用到的相对原子质量:H―1,C―12,O―16,Cl―35.5,Fe―56
一、选择题(四选一,请把正确答案的序号填在下表内,每小题2分,共40分)
1.下列物质,各取少量分别放到水中,充分搅拌,不能得到溶液的是( )
A.醋酸 B.酒精 C.大豆油 D.蔗糖
2.下列关于溶液的说法中,正确的是( )
A.饱和溶液一定是浓溶液 B.溶液一定是无色透明的
C.溶液一定是均一稳定的 D.溶液中的溶剂只能为水
3.常温下,在
A.15% B.20% C.25% D.33.3%
4.下列是一些物质的PH值范围,酸碱性最接近中性的是( )
A.苹果汁(2.9-3.3) B.番茄汁(4.0-4.4)
C.玉米粥(6.8-8.0) D.肥皂水(9.8-10.2)
5.如下图所示的实验中,小烧杯①盛的是紫色石蕊试液,②盛的是浓盐酸。片刻后,可以观察到烧杯①中液体的颜色是( )
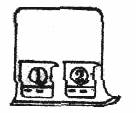
A.紫色 B.红色 C.无色 D.蓝色
6.下列物质不能导电的是( )
A.澄清石灰水 B.氢氧化钠溶液 C.稀硫酸 D.乙醇
7.按酸、碱、盐、氧化物的顺序排列的一组物质是( )
A.H2SO4、Na2CO3、NaCl、CuO B.H2O、Ca(OH)2、HCl、Na2SO4
C.H2SO4、NaOH、Na2CO3、Fe2O3 D.NaOH、H2CO3、NaCl、CO2
8.下列方法能够将石灰水和氢氧化钠溶液区别开的是( )
A.分别滴加紫色石蕊试液 B.分别通入CO2
C.分别滴加氯化钠溶液 D.分别滴加稀盐酸
9.下列物质露置在空气中质量会变大且变质的是( )
A.浓盐酸 B.浓硫酸 C.氢氧化钠 D.食盐
10.下列清洗方法中,利用乳化作用的是( )
A.用自来水洗手 B.用汽油清洗油污
C.用洗涤剂清洗油腻的餐具 D.用盐酸清除铁锈
11.现有一杯
A.加入一定量的硝酸钾 B.恒温蒸发部分水
C.升温到
12.SO2是形成酸雨的主要物质,能有效吸收SO2的溶液是( )
A.NaOH B.Na2SO
13.山茶花、杜鹃花、栀子花等适宜在酸性土壤中生长,而仙人球适宜在中性或偏碱性土壤中生长。现测得某土壤的PH约为7-8,该土壤适宜种植的花卉是( )
A.仙人球 B.杜鹃花 C.栀子花 D.山茶花
14.下列物质的顺序依一定规律排列:HCl、Cl2、NaClO、M、Cl2O5、HClO4,根据这种排列规律,M是( )
A.Cl2O7 B.KClO3 C.NaClO2 D.MgCl2
15.下列反应属于复分解反应的是( )
A.H2CO3==H2O+CO2↑ B.CaO+H2O===Ca(OH)2
C.Fe+CuSO4===FeSO4+Cu D.2NaOH+H2SO4===Na2SO4+2H2O
16.已知KNO3的溶解度随温度的升高而增大。下图是某KNO3饱和溶液的浓度随温度升高而变化的图像(不考虑溶剂的质量变化),其中正确的是( )
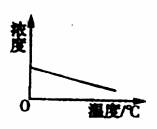
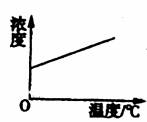
A B
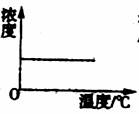
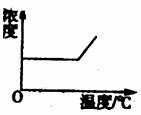
C D
17.用氧氧化钠固体配制一定质量分数的溶液时,造成所配制溶液中氢氧化钠的质量分数偏高的因素可能是(各选项不考虑其他因素的影响)( )
A.所用氢氧化钠固体已经潮解 B.氯氧化钠已经部分变质
C.用量筒量取水时,加水未到所需刻度 D,有少量的氢氧化钠溶液残留在烧杯中
18.某一无色溶液具有如下性质:①使无色酚酞试液变红;②与硫酸铜溶液反应可产生蓝色沉淀。据以上推断,此溶液是( )
A.氢氧化钠溶液 B.氯化钠溶液 C.氯化钙溶液 D.盐酸
19.下图是M、N两种物质的溶解度曲线,由溶解度曲线得出以下几条信息,你认为正确的是( )
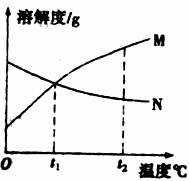
A.t1℃时,M、N两物质溶液溶质质量分数相等
B.由t1℃升温到t2℃时,N物质溶液溶质质量分数不变
C.M物质的溶解度大于N物质的溶解度
D.N物质的溶解度随温度的升高而降低
20.在一个密闭容器中,有甲、乙、丙、丁四种物质在一定条件下充分反应,测得反应前后各物质质量如下表:
物质
甲
乙
丙
丁
反应前质量/g
5
2
20
22
反应后质量/g
待测
11
28
5
下列说法错误的是( )
A.该反应是分解反应 B.甲可能是该反应的催化剂
C.乙、丙变化的质量比为9:8 D.反应后甲的质量为0 g
二、填空题(本题包括8小题,共41分)
21.(4分)在锌与稀硫酸恰好完全反应后得到的溶液中,溶质是______________,溶剂是____________;在医用消毒酒精中,溶质是_______________,溶剂是____________(均填化学式)。
22.(6分)生石灰起干燥作用时发生反应的化学方程式为_____________。取少量生石灰于水中,搅拌后取上层清液,向其中滴加无色酚酞试液,试液变红,说明该溶液呈____________________(填“酸性”、“中性”或“碱性”),测定该溶液酸碱度的最简单方法是使用______________________________。该溶液敞口放置于空气中会变质,发生反应的化学方程式为________________________________________.
23.(4分)现有60℃时100g的NaCl饱和溶液,与该溶液有关的量有:①水的质量;②溶液中NaCl的质量;③NaCl的质量分数;④60℃时NaCl的溶解度;⑤溶液的质量。
用序号填空:
(1)60℃时,用水稀释该饱和溶液,稀释前后不变的量有____________________;
(2)将该饱和溶液降温至40℃,降温前后不变的量有________________________.
24.(4分)目前市面上有一种新型饭盒――“即热饭盒”,其原理是在饭盒底部有两层,一层存放水,另一层存放镁和铁的混合物。使用时打开隔离层,即发生以下反应:Mg+2H2O==X+ H2↑。请根据以上信息回答下列问题:
(1)该饭盒底部“即热”的原理是将化学能转化为___________________。
(2)已知X是一种碱。则X的化学式是_____________________________,你推断X的化学式的依据是_____________________________.
(3)上述化学反应属于______________________(填写基本反应类型)。
25.(4分)下图中有两组实验,请根据实验中的问题写化学方程式。
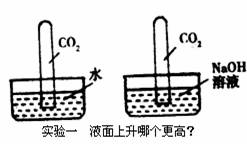
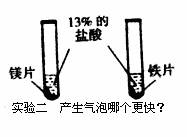
写出实验中“更高”的化学方程式:____________________________________________;
写出实验中“更快”的化学方程式:____________________________________________.
26.(7分)下图是A、B、C、D四种物质的溶解度曲线图,根据此图回答:
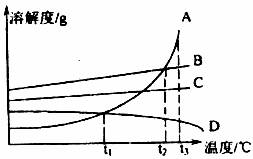
(1)在t3℃时,四种物质的溶解度大小顺序是_______________________________.
(2)在t3℃时,将四种物质分别溶于等量的水中,制成饱和溶液,然后使它们的温度都降低到t1℃时,其中,析出溶质最多的是___________;最少的是___________;没有晶体析出的物质是___________。
(3)A、B两物质的溶解度相等时的温度是___________。
(4)若要把混在A中的C除去,应采用______________________方法;若使C从饱和溶液中结晶出来,最好采用______________________方法。
27.(6分)将20g硝酸钾溶于80g水里,所得溶液均匀分为两等份:
(1)每一份溶液中硝酸钾的质量分数为______________________;
(2)若将第一份溶液变为10%溶液,可向里加入___________g水;
(3)若将第二份溶液变为40%溶液,可加热蒸发掉___________g水(无晶体析出)。
28.(6分)用三种不同的方法鉴别氢氧化钙溶液和稀硫酸。
试验编号
试验方法
现象及结论
(一)
(二)
(三)
三、实验探究题(本题包括2小题,共13分)
29.(4分)下图是小明配制100g溶质质量分数为12%的NaCl溶液的实验操作示意图:
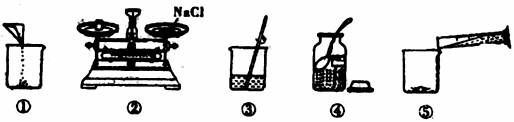
(1)上图中的玻璃仪器分别是广口瓶、量筒、烧杯和___________.
(2)指出图中的一处错误操作_________________________________。
(3)配制时应选择___________mL(10mL或50mL或100mL)的量筒量取所需要的水。
(4)用上述图示的序号表示配制溶液的操作顺序___________________。
30.(9分)氧化铜是一种黑色固体,可溶于稀硫酸。某同学想知道是稀硫酸中的哪种粒子(H2O、H+、SO42-)能使氧化铜溶解。请你和他一起通过下图所示I、II、III三个实验完成这次探究活动。
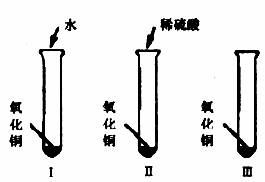
(1)你提出的假设是____________________________________;
(2)通过实验I可以证明________________________________________________;
(3)要证明另外两种粒子能否溶解氧化铜,还需要进行实验II和Ⅲ,在Ⅲ中应该加入________________________。
(4)探究结果为____________________________________。你认为除实验II和Ⅲ所用试剂外,还能够溶解氧化铜的一种常见物质是_______________________。
四、计算题(本题包括1小题,共6分)
31.(6分)某校同学探究附近赤铁矿中Fe2O3的纯度。他们采集了20g样品,加入稀盐酸,恰好完全反应,共用去稀盐酸309g,过滤得到滤渣4g(假设杂质既不溶于水,也不溶于酸;不考虑实验中的损耗)。计算:
(1)Fe2O3在赤铁矿样品中的质量分数为多少?
(2)反应后所得溶液中溶质的质量分数是多少?