初中化学第一学期期末检测?A?
一、选择题(每小题有1~2个选项符合题意,每小题4分,共48分)
1.日常生活中的下列物质,可以看成纯净物的是 ( )
A.矿泉水 B.酸牛奶 C.冰水 D.食醋
2.要从空气中获取
A.
3.我国是四大文明古国之一,商代就制造出许多精美的青铜器,这些青铜器不少至今仍完好的保存着。我国商代的青铜器能完好的保存至今,从化学的角度看主要是因为( )
A.铜的化学性质不活泼 B.铜是一种金属
C.铜的硬度比较大 D.铜的耐磨性能特别强
4.“农夫山泉”矿泉水瓶的标签上印有如下字样:Ca≥4.0 mg/L,Mg≥0.5 mg/L,K≥ 0.35 mg/L,Na≥0.8 mg/L等,这里的Ca、Mg、K、Na是指 ( )
A.元素 B.分子 C.原子 D.离子
5.用分子、原子的观点对下列现象进行解释,其中正确的是 ( )
A.蔗糖放到水中逐渐消失,是由于蔗糖分子变成了其他分子
B.气体比固体容易压缩是由于气体中的分子比固体中的分子运动的快
C.水变成水蒸气体积变大是由于水分子间的间隙变大了
D.水银温度计能指示温度高低是由于汞原子受热时体积膨胀遇冷时体积收缩
6.下列物质在氧气中燃烧,生成物均为白色固体的是 ( )
A.硫和铜 B.镁和磷 C.磷和木炭 D.木炭和铁丝
7.人类生活需要能量,下列现象中,没有直接利用化学反应所产生的能量的是 ( )
A.人用食物维持体能 B.家庭用煤气做饭
C.办公室用空调取暖 D.工人用炸药拆除危旧建筑
8.化学方程式不能提供的信息是 ( )
A.化学反应速率的快慢 B.哪些物质参加反应
C.生成的各种粒子的相对分子质量 D.在什么条件下发生反应
9.在反应
A.34 B.
10.小张为探究燃烧的条件,做了如图所示的实验。结果发现铜片上的白磷燃烧起来,而铜片上的A物质和水中的白磷没有燃烧。从实验中,该同学得出了下列结论,其中不正确的是 ( )
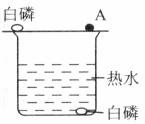
A.可燃物燃烧,必须达到着火点和与空气接触
B.物质A一定不具有可燃性
C.向热水中的白磷通入空气,在水下也能燃烧
D.任何物质只要和空气接触并达到着火点就能燃烧
11.2004年,美国科学家通过“勇气号”太空车检测出火星大气中含有一种称为硫化羰(化学式为COS)的物质,已知硫化羰与二氧化碳的结构相似,但能在氧气中完全燃烧,下列有关硫化羰的说法正确的是 ( )
A.硫化羰可作灭火剂
B.硫化羰在氧气中完全燃烧后生成物是CO2和SO2
C.硫化羰的相对分子质量是44
D.硫化羰和二氧化碳都是氧化物
12.证明生石灰中含有石灰石,应选用的试剂或方法是 ( )
A.高温煅烧 澄清的石灰水 B.用水溶解
C.稀盐酸 澄清的石灰水 D.观察颜色和状态
二、填空题(本大题共6小题,共29分)
13.(5分)写出符号的意义或用化学符号表示:
2个氮原子__________;1个干冰分子__________;3Fe2十__________;
氧离子的结构示意图_____________;在氧化铝中铝元素的化合价为+3价__________。
14.(3分)臭氧层衰竭、酸雨和温室效应是当今世界三大环境问题。
(1)人为的大气污染物,使地球外层空间的臭氧层受到不同程度破坏,减弱了臭氧层吸收__________的作用;
(2)形成酸雨的原因是空气受到硫的氧化物和氮的氧化物的污染,请举一例说明酸雨可导致人类生存环境的恶化______________________________;
(3)形成温室效应的原因之一是____________________;你对防止温室效应的一点建议是______________________________。
15.(4分)与金属跟盐的置换反应规律相似,非金属跟盐反应也有这种规律,Br2、I2、Cl2及其化合物间有如下的反应关系:Br2+2NaI==2NaBr+I2,Cl2+2NaI==2NaCl +I2,Cl2+2NaBr==2NaCl+Br2,试确定三种非金属单质的化学活动性由强到弱的顺序:______________________________。
16.(6分)有人在研究FeSO4受热分解时,作了如下假设:
(1)假设它按KClO3受热分解的方式来分解,反应的化学方程式为________________;
(2)假设它按CaCO3受热分解的方式来分解,反应的化学方程式为________________;
(3)事实上由于FeO易被氧化,FeSO4的分解产物(分解温度约
17.(5分)氧化铜是一种黑色固体,可溶于稀硫酸。某同学想知道是稀硫酸中的哪种粒子(H2O、H+、SO42―)能使氧化铜溶解。请你和她一起通过下图所示的Ⅰ、Ⅱ、Ⅲ三个实验完成这次探究活动。
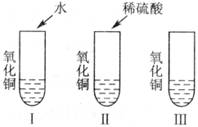
(1)你提出的假设是__________________;
(2)通过实验Ⅰ可以证明__________________。
(3)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅲ中应该加入__________________;
(4)探究结果为_____________________________。你认为除实验Ⅱ和Ⅲ所用试剂外,还能够溶解氧化铜的一种常见物质是_________。
18.(6分)对知识的归纳和整理是学习化学的一种重要方法。现有三个化学反应如下:
①S+O2 SO2;②2CO+O2
SO2;②2CO+O2 2CO2;③3Fe+2O2
2CO2;③3Fe+2O2 Fe3O4
Fe3O4
(1)通过比较发现:它们有许多相似之处:其一______________;其二______________。我能另写一个符合这两点的化学方程式:______________。它们之间存在相异之处,其中一个反应与众不同,这个反应和它的不同之处是______________。
(2)课外学习Cu2(OH)2CO3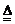 2CuO+H2O+CO2↑后,我又发现它也和上述三个反应相似,其相似之处是______________ 。
2CuO+H2O+CO2↑后,我又发现它也和上述三个反应相似,其相似之处是______________ 。
三、简答题(本大题共2小题,共11分)
19.(3分)如图,取一团光亮无锈的铁丝绒,放入一支洁净的试管的底部,将试管倒放在一个盛有水的烧杯里。数天后,能观察到的现象是:__________________________。
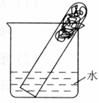
20.(8分)雪碧(可乐、啤酒等)是生活中常见的饮料,其中含有二氧化碳、水等物质。
(1)二氧化碳是利用什么原理装进饮料瓶中的?喝了雪碧为何常常会打嗝?
(2)请你设计两种实验方法检验雪碧(可乐、啤酒等)中的二氧化碳(写出必要的实验步骤和实验现象)。
四、计算题(本大题共l小题,共l2分)
21.实验室现需
收集
充分加热后试管内残余固体的质量
(1)反应过程中产生氧气的总质量是多少?(实际操作中氧气的损耗忽略不计)
(2)该同学最多能回收到多少g二氧化锰?