2008年无锡市高级中等学校招生考试
化学试卷
相对原子质量:H―1 O―
一、单项选择题(本题包括20小题,每小题只有1个选项符合题意,每小题1分,共20分)
1、物质的下列性质中,属于化学性质的是 ( )
A.颜色、状态 B.密谋、硬度 C.溶点、沸点 D.还原性、可燃性
2、下列食物中富含淀粉的是 ( )
A.黄瓜 B.鸡蛋 C.米饭 D.瘦肉
3、佝偻病患者体内缺少的元素是 ( )
A.钙 B.铁 C.锌 D.硒
4、化学反应提供的能量已不能满足人类的需求,需要开发新的能源。下列属于新能源的是( )
A.煤 B.天然气 C.石油 D.太阳能
5、下列变化不属于缓慢氧化的是 ( )
A.甲烷燃烧 B.酒的酿造 C.食物腐烂 D.动植物呼吸
6、下列物质混合,充分搅拌后能形成无色溶液的是 ( )
A.植物油与水 B.碘与酒精 C.面粉与水 D.食盐与水
7、结构示意图 所表示的粒子是 ( )
所表示的粒子是 ( )
A.分子 B.原子 C.阳离子 D.阴离子
8、下列图示实验操作错误的是 ( )




除去CO中的CO2 检查装置气密性 过滤 浓硫酸稀释
A. B. C. D.
9、用分子的观点解释下列现象,不合理的是 ( )
A.酒精燃烧――分子发生了变化 B.汽油挥发――分子大小发生了变化
C.干冰升华――分子间的间隔改变了 D.花香四溢――分子在不断运动
10、下列物质名称、俗名、化学式一致的是 ( )
A. 冰、干冰、H2O B.银、水银、Hg
C.乙醇、酒精、C2H5OH D.氢氧化钠、纯碱、NaOH
11、下列区别物质的方法错误的是( )
A.用肥皂水区别软水和硬水 B.用水区别氧化钠和硝酸铵固体
C.用燃烧的方法区别羊毛和涤纶 D.用观察颜色的方法区别O2和CO2
12、下列五之间的转化,不能通过一步反应实现的是( )
A.Fe2O3→Fe B.NaNO3→NaCl C.Al→Al2O3 D.CO2→CaCO3
13、下列各组中的环境问题与治理措施无关的是 ( )
A
B
C
D
环境问题
温室效应
土地沙漠化
酸雨
蓝藻爆发
治理措施
减少使用化石燃料
植树造林
回收废旧电池
污水处理后排放
14、下列做法不会引起食品安全事故的是 ( )
A.用霉变大米煮饭食用 B.用铁强化酱油作调味品
C.用甲醛溶液浸泡水产品并食用 D.用含亚硝酸钠的工业用盐腌制食品
15、下列实验现象描述错误的是 ( )
A.硫在氧气中燃烧发出蓝紫色火焰
B.将二氧化碳通入紫色石蕊溶液中,溶液变红色
C.打盛有浓盐酸的试剂瓶的瓶盖,瓶口出现白烟
D.氢氧化钠溶液中加入硫酸铜溶液,产生蓝色沉淀
16、手电筒中使用的锌?锰干电池,在工作时反应的化学方程式为:
Zn+2NH4Cl+2MnO2===ZnCl2+2NH3+X+H2O,则X的化学式为 ( )
A.
MnO B.
Mn2O
17、今年6月1日起执行的“限塑令”规定,超市、商场、集贸市场等零售场所实行塑料袋有偿使用制度。下面4位同学对“限塑令”的看法,不合理的是 ( )


A. B. C. D.
18、下列家庭小实验能成功的是 ( )
A.用淬火处理后的缝衣钢针制钓鱼钩 B.用食盐水除去热水瓶中的水垢
C.用加热的方法修补电木插座 D.用电池“锌皮”与食醋反应制氢气
19、硝酸铵(俗称硝铵)是一种常见的氮肥,易溶于水,易潮解而结块,受热易分解,遇碱放出氨气,在高温或受猛烈撞击时易爆炸。贮存或使用硝铵时正确的是 ( )
A.露天敞口贮存 B.在阴凉处密封贮存
C.结块进用铁锤砸碎 D.与熟石灰混合施用
20、某工厂常用1体积的浓硫酸(密度为
A.10% B.15% C.20% D.25%
二、不定项选择题(本题包括5小题,每小题有1~2个选项符合题意,每小题2分,共10分。按题意选对给2分;错选、多选不给分;少选且选对给1分)
21、下列实验操作正确的是 ( )
A.将pH试纸浸入溶液中测溶液的pH
B.用酒精灯的内焰给试管中的液体加热
C.实验结束后,将剩余药品倒入指定的容器中
D.为了节约火柴,用燃着的酒精灯点燃另一盏酒精灯
22、下列叙述正确的是 ( )
A.不锈钢的含碳量比生铁中的含碳量高
B.可用燃着的木条检验液化石油气罐是否漏气
C.二氧化锰、硫酸铜溶液都能作为过氧化氢分解的催化剂
D.粗盐提纯实验中蒸发滤液,待蒸发皿内出现较多固体时应停止加热
23、下列有关溶液的叙述正确的是 ( )
A.洗涤剂能除去油污,是因为它具有乳化作用
B.8gCaO溶于
C.喝下汽水后,常会打嗝,说明气体的溶解度随温度的升高而减小
D.配制
24、在一定量的稀盐酸中逐滴加入下列物质至过量,其对应的曲线变化(V为加入溶液的体积,AgCl难溶于水)正确的是 ( )
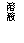





25、铁和铜都能与氯化铁溶液反应,反应的化学方程式为:
Fe+2FeCl3===3FeCl2, Cu+2FeCl3===CuCl2 + 2FeCl2
若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后烧杯中有金属剩余。下列分析正确的是 ( )
A.剩余金属只有Fe B.剩余金属一定有Cu
C.反应后的溶液中可能有FeCl3 D. 反应后的溶液中一定有FeCl2
三、(本题包括5小题,共26分)
26、天然水中含有的部分杂质如下表所示:
溶 解 物 质
悬浮物质
主要气体
主要离子
生物生成物
细菌、藻类及原生物、泥沙、黏土等
氧气
二氧化碳
硫化氢等
钙离子、氯离子、
硫酸根离子
镁离子
NH4+、NO2-、
HPO42-、Fe3+、
H2PO4-等
请根据上表内容回答:
⑴写出“主要气体”中两种气体的化学式__________、__________;
⑵写出“主要离子”中一种阳离子和一种阴离子的符号_________、_________;
⑶写出由“生物生成物”中的离子组成的硫酸二氢铵的化学式______________。
27、在“浓硫酸、氯化钠、大理石、稀有气体、钛合金”中选用适当的物质填空。
⑴可用来消除公路积雪的是___________;⑵可用作保护气的是__________________;
⑶可用来制造人造骨的是_____________;⑷可用作某些气体干燥剂的是__________;
⑸可用作建筑材料的是_______________。
28、现有H、S、O、Na四种元素,请选用其中的元素写出符合下列要求的化学式各一个:
⑴相对分子质量最小的氧化物_________;⑵用于金属表面除锈的酸____________;
⑶厨房清洁剂中含有的碱_____________;⑷由三种元素组成的一种盐__________。
29、写出下列反应的化学方程式,并在括号内注明反应的基本类型:
⑴红磷在空气中燃烧________________________________________,( )反应;
⑵高温下碳与氧化铜反应____________________________________,( )反应;
⑶加热高锰酸钾制氧气______________________________________________________;
⑷氢氧化亚铁在氧气和水的作用下生成氢氧化铁________________________________。
30、根据图甲、乙两种固体物质的溶解度曲线,回答下列问题:
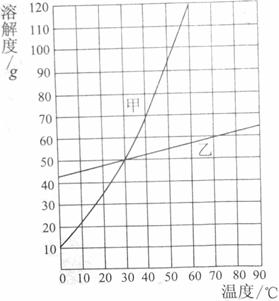
⑴温度的变化对溶解度影响相对较小的物质是__________。
⑵在______℃时,甲、乙两种物质的溶解度相等;
⑶
四、(本题包括3小题,共14分)
31、A、B、C三种元素,A元素的单质是最清洁的燃料;B元素的单质能在C元素的单质中剧烈燃烧,火星四射,生成黑色固体;B元素的单质是目前世界上年产量最高的金属。写出A、B、C三种元素的名称或符号:A___________、B___________、C___________;写出B、C二种元素组成的一种化合物的化学式:____________。
32、人类的生活和工农业生产都离不开水。下图是自来水厂净水过程示意图。
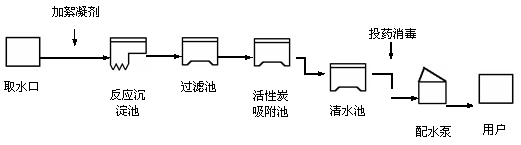

请根据图示回答下列问题:
⑴自来水厂生产自来水时,使用的净水方法有___________________;
A.沉淀 B.过滤 C.煮沸 D.蒸馏 E.吸附
⑵取水后加入絮凝剂(明矾)的作用是________________________________________;
⑶自来水厂常用二氧化氯进行投药消毒,二氧化氯的化学式为_________;漂白粉(有效成分为次氯酸钙)也可用为饮水消毒剂,次氯酸钙[Ca(ClO)2]中氯元素的化合价为____。
33、物质A-J有下图转化关系,反应条件均略去。A、B物质的组成元素相同,C、D、G是初中化学中常见的单质,I是金属。H的相对分子质量为100,组成元素的原子个数比为3:2,其中一种元素的质量分数为28%。


试回答:
⑴上述转化中属于分解反应的是 (填序号);
⑵A、J、H的化学式为A 、J 、H ;
⑶反应②的化学方程式为 ;
反应⑤的化学方程式为 。
五、(本题包括3小题,共22分)
34、请回答下列问题:(在下列⑴⑵两小题中任选一题回答,若两小题都回答,则以第⑴小题的答案评定分数。)
⑴酸碱中和反应在生活、生产中有广泛的应用,请举两例说明。
⑵燃料充分燃烧可节约资源,使燃料充分燃烧通常需要考虑的两点是什么?
35、利用下列仪器进行气体的制取和性质实验。请完成下列问题。


⑴仪器B、I的名称分别是 、 ;
⑵实验室用氯酸钾和二氧化锰制取氧气,仪器的装置组合是 (填字母),反应的化学方程式为 ;
⑶实验室制取二氧化碳,所用的药品是 ,从上述仪器中组合3套发生装置为 、 、 (填字母),检验二氧化碳收集满的方法是_______________________________________________________。
⑷在B中收集满二氧化碳,倒扣于盛有水的H中,一段时间后,B中液面__________(填“上升”或“不变”);若B中充满下列________气体,也会发生类似现象。
A.H2
B.NO
(提示:①3NO2+H2O===2HNO3+NO,NO气体难溶于水;
②同温同压下,任何气体体积之比等于分子数之比。)
36、某化学兴趣小组的同学对溶液的鉴别进行探究,请你分析并填空。
【实验目的】Na2CO3溶液、NaOH溶液、Ca(OH)2溶液、稀盐酸四种溶液的鉴别。
【实验药品】未贴标签的四瓶溶液[Na2CO3溶液、NaOH溶液、Ca(OH)2溶液、稀盐酸]和紫色石蕊试液。
【实验仪器】试管、胶头滴管等。
【设计并实验】
甲组同学利用紫色石蕊试液鉴别四种溶液:
实验操作和步骤
实验现象与结论
⑴用4支试管,各取少量四种溶液,分别滴加紫色石蕊试液。
一支试管中溶液由无色变红色,则原溶液是_____________溶液。
⑵另用3支试管,各取少量未确定的三种溶液,分别滴加步骤⑴检验出的溶液。
一支试管溶液中有气泡放出,则原溶液是____________溶液。
⑶另用2支试管,_________________
_____________________,__________
_________________________________。
一支试管溶液中有白色沉淀析出,则原溶液是_________溶液,反应的化学方各式为_________________________,另一支试管溶液中无现象,则原溶液是________溶液。
乙组同学经过讨论认为,不用紫色石蕊试液也能鉴别出四种溶液。各自分别做了如下实验:
同学
实验操作
实验现象
结 论
小峰
用3支试管,各取少量三种溶液,分别滴加另一种溶液。
一支试管溶液中有气泡放出,其余二支试管溶液中无现象。
所滴加的溶液是稀盐酸。
小伟
一支试管溶液中有白色沉淀析出,其余二支试管溶液中无现象。
所滴加的溶液是Na2CO3溶液。
小明
三支试管溶液中都无现象。
所滴加的溶液是NaOH溶液。
乙组三位同学经过交流后发现__________同学的结论是错误的,所滴加的溶液应是____________溶液,由此鉴别出了四种溶液。
【反思与体会】①物质的鉴别有多种方法;②鉴别物质的关键是利用物质的特征性质; ……
六、(本题包括2小题,共8分)
37、蛋白质是重要的营养物质,它由多种氨基酸(如丙氨酸、甘氨酸等)构成,甘氨酸的化学式为H2N?CH2?COOH。请回答下列问题:
⑴甘氨酸中碳、氢、氮、氧元素的质量比为____________________;
⑵甘氨酸中碳元素的质量分数为___________________;
⑶每克蛋白质完全氧化约放出18kJ的能量,成人每天摄取60-
的蛋白质完全氧化,则放出的能量约为_________________ kJ。
38、某石灰厂有一批石灰石原料,为了测定该石灰石的纯度,厂化验室技术员称取
操作次序
第一次
第二次
第三次
第四次
剩余固体质量
试计算:
⑴完全反应后生成二氧化碳_____________g;
⑵石灰石样品中碳酸钙的质量分数;
⑶充分煅烧20t这种石灰石,可制得含杂质的生石灰的质量。