2008 年潍坊市初中学业水平考试
化 学 试 题
注意事项:
1.本试睡分为第1卷(选择题)和第Ⅱ卷(非选择题)两部分。全卷满分100分,考试时间为90分钟。
2.答第Ⅰ卷前务必将自己的姓名、准考证号、考试科目和试卷类型涂写在答题卡上。第Ⅰ卷每题选出答案后,用2B铅笔把答题卡上对应题目的答案标号(A、B、C、D)涂黑。如需改动,必须先用橡皮擦干净,再改涂其它答案。
可能用到的相对原子质量:H
Cl 35.5 Ca 40 Fe 56 Cu 64
第Ⅰ卷(选择题 共40分)
一、选择题(本题包括20小题,每小题2分,共40分,每小题只有一个选项符合题意)
1.石油是―种重要能源,人类正面临着石油短缺、油价上涨的困惑。以下解决能源问题的方法不当的是( )
A.砍伐树木作燃料 B.利用太阳能 C.利用风能 D.开发核能
2.生活中的下列物质属于纯净物的是( )

3.下表是小明制定的食谱单,为使营养均衡,在“你的补充”栏可以选填的食物是( )
主食
米饭、馒头
菜肴
烧鸡块、红烧鱼、花生米
乳品
牛奶
你的补充
A.煎豆腐 B.炸大虾 C.凉拌黄瓜 D.蛋糕
4.下列说法中,正确的是( )
A.过氧化氢的化学式为H2O B.钠原子的结构示意图为
C.硫酸根离子的符号为SO4 D.氯离子中质子数=电子数=17
5.家庭常用洗涤剂的pH如下图所示,其中最接近中性的是( )
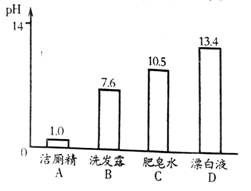
6.铁是应用最广泛的金属之一。下列物质中不能与氧化铁反应生成铁的是( )
A.木炭 B.氢气 C.一氧化碳 D.氧气
7.乙醇汽油(汽油中加入一定比例的乙醇)的使用可以缓解石油危机。从甜菜或甘蔗中提取的蔗糖可以通过发酵产生乙醇。下列过程中没有发生化学变化的是( )
A.甜菜的生长 B.汽油中加入乙醇 C.乙醇的燃烧 D.蔗糖的发酵
8.航天员专用的小分子团水具有饮用量少、在人体内储留时间长、排放量少等特点。航天员一次饮用125mL小分子团水,可维持人体6h正常需水量。下列关于小分子团水的说法中正确的是( )
A.水分子的化学性质被改变了 B.小分子团水中水分子间没有间隙
C.小分子团水中水分子停止了运动 D.小分子团水的部分物理性质与普通水有所不同
9.“生命可贵,安全第一”。下列采取的安全措施中不正确的是( )
A.厨房天然气管道漏气,立即关闭阀门并轻轻开窗通风
B.震后灾区饮用水应消毒处理后才能饮用
C.为避免了尘土进入,豪华装修完的房屋立即入住后必须关闭门窗
D.进入久未开启的菜窖前,先用蜡烛做灯火实验
10.“神州六号”太空舱利用NiFe2O4将航天员呼出的CO2转化为O2,而NiFe2O4的质量和化学性质都不变化,在该过程中NiFe2O4是( )
A.反应物 B.生成物 C.催化剂 D.消毒剂
11.小红学习酸碱指示剂与常见酸、碱溶液作用后,归纳总结出如图

A.紫色 B.蓝色 C.红色 D.无色
12.用氯化钠配制100 g溶质质量分数为0.9%的生理盐水,现有下列操作:①配制溶液;②称取氯化钠固体;③过滤;④量取蒸馏水;⑤计算。正确的操作顺序是( )
A.①②③④ B.⑤②④① C.⑤①②④ D.③②④①
13.下图中所示实验操作不正确的是( )

14.将甲、乙两种金属片分别放入硫酸铜溶液中,甲表面析出金属铜,乙没有发生反应。据此判断,三种金属的活动性顺序是( )
A.甲>铜>乙 B.铜>甲>乙 C.乙>铜>甲 D.甲>乙>铜
15.下表列出了除去物质中所含少量杂质的方法,其中正确的是( )
选项
物质
所含杂质
除去杂质的方法
A
CO2
CO
通过足量氢氧化钠溶液,并干燥
B
H2
水蒸气
通过盛有浓硫酸的洗气瓶
C
N2
O2
通过炽热的木炭
D
NaOH溶液
Na2CO3
加入足量稀盐酸至不再产生气泡
16.化学基本概念是化学基础知识的重要组成部分。下列概念间的关系不正确的是( )
选项
概念X
概念Y
X与Y的关系
A
酸碱性
酸碱度
相同关系
B
酸式盐
碱式盐
并列关系
C
化合物
氧化物
包含关系
D
化合反应
氧化反应
交叉关系
17.2007年诺贝尔化学奖授予德国化学家Gerhard Ertl,以表彰他在表面化学领域研究所取得的开拓性成就。下图表示某反应在催化剂Pt/ Al2O3/Ba表面进行的过程(图中nitrate指硝酸盐)。判断下列说法中正确的是( )
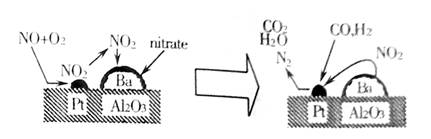
A.CO2、Al2O3属于金属氧化物 B.CO、H2O属于非金属氧化物
C.NO与O2生成NO2的反应属于置换反应 D.硝酸根离子中氮元素的化合价
18.小亮同学设计右图装置来制取并收集气体,你认为他能制得的气体是( )

A.用KMnO4粉末制取O2 B.用KClO3和MnO2制取O2
C.用Zn和稀硫酸制取H2 D.用石灰石和稀盐酸制取CO2
19.在密闭容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量如
下表:
物质
X
Y
Z
Q
反应前质量/g
8
2
20
5
反应后质量/g
待测
10
8
13
下列说法正确的是( )
A.反应后X的质量为
C.参加反应的X、Z的质量比是1:3 D.Y、Q的相对分子质量比一定为1:1
20.某研究性学习小组调查发现,甲、乙两工厂排放的污水各含下列离子H+、Cu2+、K+、NO3-、0H-中的三种离子(两厂含有一种相同的离子)。若将两厂的污水按一定比例混合,沉淀后污水会变成无色澄清中性溶液。下列关于污水的分析,正确的是( )
A.0H-和Cu2+来自同一工厂 B.H+和0H-来自同一工厂
C.Cu2+和K+来自同一工厂 D.H+和Cu2+来自同一工厂
第Ⅱ卷(非选择题 共60分)
注意:必须用蓝、黑色钢笔或圆珠笔答题,答案写在指定位置。
二、本题包括3小题(共30分)
21.(10分)全国人民期盼已久的奥运会即将在北京召开。请用所学知识回答与奥运会有关的下列问题。
(1)北京奥运会的许多方面需要大量材料。下列使用的材料(加黑点)中属于金属材料的是 (填序号,下同),属于有机合成材料的是 ,属于复合材料的是 。

(2)人类获得的能量绝大多数来自于天然气、 和煤等化石燃料。北京奥运会使用丙烷(C3H8)作火炬燃料,丙烷燃烧时生成水和二氧化碳,该反应的化学方程式为 。
(3)北京奥运会坚决反对运动员使用兴奋剂。某种兴奋剂的化学式为C16H16O3,该兴奋剂中碳:氢:氧元素的质量比为 。
(4)奥运会游泳、跳水等运动项目在“水立方”举行,比赛池中的水要定期进行消毒处理。按照物质的分类,下列某种消毒剂与其他三种消毒剂不属于同一类的是 (填序号)。
A.Cl2
B.KMnO
22.(11分)海水中镁的含量一般为
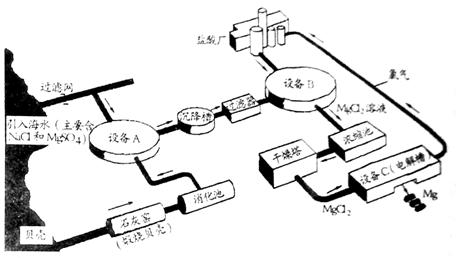
根据上述流程图,回答下列问题:
(1)石灰窑中发生反应的化学方程式为 。
(2)消化池中发生的反应CaO +H2O=====Ca(OH)2,其反应类型为 ,
消化池中温度升高的原因是 。
(3)写出设备A、B和C中反应的化学方程式
A: ;
B: ;
C: 。
⑷氯气不能排放到空气中,而要循环使用,其原因是是:
①氯气有毒,排入空气会污染环境;
② 。
23.(9分)潍坊某化工厂以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,其制备过程表示如下:

请回答:
⑴工业上生产的氯化铵属于 (填写序号)。
A.酸 B.碱 C.盐 D.氧气物
⑵在其它条件不变时,由下图可看出硫酸钠的溶解度与温度的关系为 。工业上从溶液中结晶析出氯化铵的温度范围约为 。

(3)设计实验验证硫酸钠中含有NH
三、本题包括2小题(共20分)
24.(8分)某校化学活动小组查阅资料发现,粗盐中除NaCl外,还含有MgCl2、CaCl2、MgSO4以及泥沙等杂质,他们要除去杂质得到精盐,设计了下列实验方案(序号①~⑧表示实验操作,用于沉淀的试剂稍过量):

根据上述方案,回答下列问题:
(1)操作①中玻璃棒的作用是 。
(2)第⑤步操作的名称是 。
(3)“蒸发结晶”用到的器材有:铁架台(铁圈)、坩埚钳、石棉网、火柴、玻璃棒、 、 。
(4)实验中加入“Na2CO3溶液”的目的是 。
(5)利用提供的沉淀试剂,再写出一种添加试剂的操作顺序(填序号): 。
25.(12分)已知某混合金属粉末,除铝外还含有铁、铜中的一种或两种,所含金属的量都在5%以上。请设计实验探究该粉末中铁、铜的存在。
资料在线:铝与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(2Al+2H2O+2NaOH=2NaAlO2+3H2↑),铁和铜不与氢氧化钠溶液反应。
可供选择的实验用品:烧杯、大试管、量筒、滴管、燃烧匙、药匙、磁铁;稀硫酸、稀盐酸、NaOH槠液、氨水。
请你参与并完成以下实验探究过程:
Ⅰ、提出假设
假设1:该混合金属粉末中除铝外还含有Fe。
假设2:该混合金属粉末中除铝外还含有 。
假设3:该混合金属粉末中除铝外还含有Fe、Cu。
Ⅱ、设计并实施实验方案
(1)基于假设1,不用化学试剂,证明金属铁的存在 。
(2)基于假设2,将混合金属粉末加入足量稀盐酸,你观察到的现象是 ,反应的化学方程式为 。
(3)基于假设3,请你完成实验操作,描述实验现象。
实验步骤
实验操作(说明仪器和试剂)
实验现象
结论
①
仅除去铝
②
证明含有铁
③
将大试管静置,弃去上层清液,加水,多次洗涤剩余固体
剩余固体呈紫红色
证明含有铜
四、本题包括1小题(10分)
26.(10分)某化学研究小组对当地的石灰石样品进行了研究。称取石灰石样品
实验序号
加入稀盐酸的质量/g
剩余物质的质量/g
第1次
10
5.5
第2次
10
3
第3次
10
1.6
第4次
10
m
(1)第4次剩余物质的质量m= g
(2)石灰石样品中CaCO3的质量分数为 。
(3)计算稀盐酸的溶质质量分数。