2007-2008学年度江苏省太仓市初三第一学期期末考试
化学试卷
可能用到的相对原子质量:H:l C:12 N:14 O:16 S:32 K:39 Ca:40 Fe:56
第Ⅰ卷(选择题共40分)
一、选择题(本题包括20小题,每小题2分,共40分。每小题只有一个选项符合题意,将正确答案的序号填在答题卷上)
1.下列变化属于化学变化的是
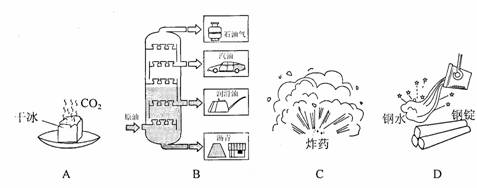
2.下列物质不属于溶液的是
A.碘酒 B.消毒酒精 C.生理盐水 D.液氮
3.下列各类食物中含有丰富蛋白质的是
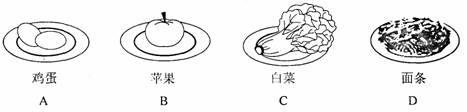
4.下列物质在空气中燃烧时,用干燥的烧杯罩在火焰上方,烧杯内壁没有水珠出现的是
A.一氧化碳燃烧 B.氢气燃烧 C.甲烷燃烧 D.蜡烛燃烧
5.下列洗涤过程中,利用了乳化作用的是
A.用稀盐酸除铁锈 B.用洗洁精除去碗上的油
C.用自来水冲洗水果 D.用超声波除去仪器上的污垢
6.在t℃时,取
A.
7.关于分子、原子、离子的说法,其中正确的是
A.原子是最小的粒子,不可再分
B.原子可以转化成离子,离子不能转化成原子
C.当二氧化碳气体变成干冰时,二氧化碳分子问不存在间隔
D.分子、原子、离子都可以直接构成物质
8.物质的用途与性质密切相关。下列说法不正确的是
A.铜用于制导线,是由于铜有良好的导电性
B.铁制品表面涂“银粉”(铝粉)防生锈,是由于铝的化学性质比铁稳定
C.二氧化碳用于灭火,是由于二氧化碳不可燃、不助燃且密度比空气大
D.氮气常用作保护气,是由于氮气的化学性质不活泼
9.下列灭火方法不恰当的是
A.酒精灯不慎打翻起火,立即用湿抹布扑灭
B.图书档案起火,用二氧化碳灭火器扑灭
C.炒菜时油锅中的油不慎着火,可用锅盖盖灭
D.石油油井着火,用大量水烧灭
10.下列说法不正确的是
A.高温煅烧石灰石可制取生石灰
B.生铁可完全溶解在稀盐酸中
C.合金的性能一般比组成它们的纯金属更优越
D.地壳中含量最多的金属元素是铝元素
11.晓晓同学需配制
A.在托盘上垫纸称量12gNaOH固体
B.称量时发现指针向右偏转,应调节游码使天平平衡
C.用100mL量简量取88mL水
D.用药匙搅拌,加速NaOH溶解
12.利用化学实验可以鉴别生活中的一些物质。下表中各组物质的鉴别方法不能将本组待鉴别的物质都区分出来的是
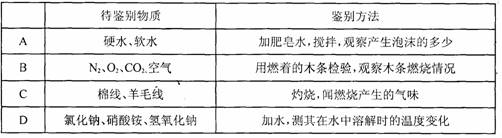
13.根据已配平的式子:4K2Cr2O7 4K2Cr2O4+2R+3O2↑,可以推断R的化学式为
4K2Cr2O4+2R+3O2↑,可以推断R的化学式为
A.CrO B.Cr2O
14.下列关于营养与健康的说法错误的是
A.人体内的脂肪储备着丰富的热量
B.如果蛋白质摄入量不足,会使人生长发育迟缓
C.摄入维生素不足,不会患营养缺乏症
D.低血糖的人会出现乏力、疲倦等症状,需尽快补充葡萄糖
15.在一密闭容器里放入四种物质,使其在一定条件下充分反应,测得数据如下
则下列表述正确的是
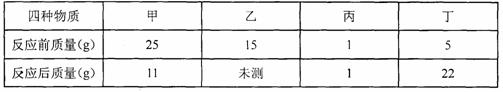
A.末测值为
B.丙一定是催化剂
C.乙全部发生了反应
D.甲与乙反应的质量比为14:3
16.己知某两种物质在光照条件下能发生化学反应,其微观示意图如下:
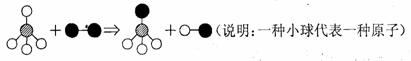
则下列说法正确的是
A.图示中的反应物都是单质 B.该反应属于置换反应
C.图示中共有4种分子 D.该图示不符合质量守恒定律
17.将一根洁净的铁钉放入稀硫酸中:①在铁钉表面有气泡产生②溶液由无色逐渐变为浅绿色③铁钉的质量减轻④溶液的质量增加。以上叙述正确的是
A.①②③ B.①③④ C.①④ D.①②③④
18.山茶油是一种绿色保健食品,其主要成分是柠檬醛,现从山茶油中提取7.
A.一定含碳、氢、氧元素
B.只含碳、氢元素
C.一定含碳、氢元素,可能含有氧元素
D.碳、氢、氧元素的质量比为10:16:1
19.通过下列实验可以得出的结论,其中不合理的是

A.甲实验中黄铜片能在铜片上刻画出痕迹,可以说明黄铜的硬度比铜片大
B.乙实验既可以说明分子在不停的运动着,又可以说明氨水显碱性
C.丙实验既可以说明二氧化碳易溶于水,又可以说明二氧化碳具有酸性
D.丁实验既可以说明一氧化碳具有还原性,又可以说明一氧化碳具有可燃性
20.从石灰浆抹的墙壁上掉下一块白色固体,为探究其成分,进行如下实验:
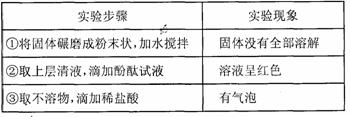
由此得出的结论正确的是
A.一定有CaCO3和Ca(OH)2 B.一定有Ca(OH) 2,可能有CaCO3
C.一定没有CaCO3和Ca(OH) 2 D.一定有CaCO3,可能有Ca(OH) 2
第1I卷(非选择题 共60分)
二、(本题包括3小题,共13分)
21.根据以下A、B、C三种微粒的结构示意图填空。
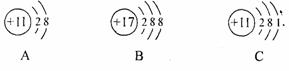
(1)请选用A、B、C序号填至:
①属于同一元素的不同微粒的是 。
②属于阳离子的是 ,属于阴离子的是 。
(2)上述三种微粒中,能形成化合物的化学式是 。
22.研究物质时常对物质进行分类,以便对同类物质的组成、性质等进行深入研究。请从下列物质中选出一种物质.写出该物质与其他物质不同的理由(一种物质可选用一次,也可选用多次)。

23.按要求写出下列化学反应方程式,并填写相关空格。
(1)铝片投入稀硫酸中
(2)向硫酸铜溶液中加入氢氧化钠溶液
,实验现象 。
(3)生石灰与水生成熟石灰的反应
,在此反应过程中 (选填“吸收”或“放出”)热量。
三、(本题包括4小题,共15分)
24.我们已经知道这样的事实:
①食盐易溶于水,难溶于植物油;②硝酸钾易溶于水,碳酸钙难溶于水;③蔗糖在热水中溶解的质量比在等质量的冷水中溶解的质量多。
请你回答下列问题:
(1)以上事实表明,固体物质的溶解能力与 、 、 三个因素有关。
(2)请你举出上述三个因素中的一个应用实例(要求与上面所列事实不同)。
。
25.应用所学化学知识回答下列问题:
(1)在严寒的冬季,厨房里的水、盐水、食醋最易结冰的是 ,原因是 。
(2)不能用铁制容器盛放硫酸铜,其原因是 。
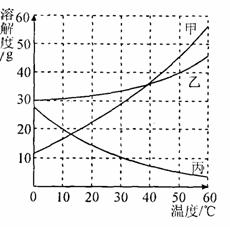
26.甲、乙、丙三种物质的溶解度如右图所示。据图回答:
(1)
(2)
(3)要使接近饱和的丙物质溶液变为饱和,可采取的一种措施是 .
(4)
27.根据下列实验示意图回答相关问题:
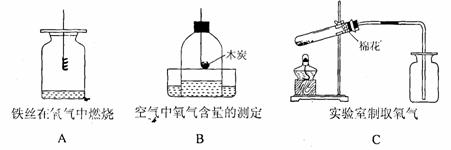
(1)A实验中未观察到明显现象的原因 ;
(2)B实验测定结果偏低的原因 ;
(3)指出C实验中的错误 。
四、(本题包括2小题,共12分)
28.(本题有a、b两小题,考生任选一题解答,不得两题都解,若两题都解,则以a小题计分)
a.油脂是重要的营养物质。油脂在人体内完全氧化时,每克放出约39.3kJ的能量,如果油脂的化学式为C57H110O6则:
(1)该油脂由 种元素组成,其相对分子质量为 ;
(2)正常人一般每天消耗9432kJ能量,如果能量的25%由油脂提供,那么我们每天大约需要摄入 g油脂,才能维持机体能量平衡。
b.无土栽培的某种营养液中,含硝酸钾的质量分数为7.1 0%。
(1)某蔬菜种植大户需配制该营养液
(2)这些硝酸钾中含氮元素的质量是
;(精确至0.
(3)硝酸钾属于 (在“单质”“化合物”“氧化物”中选填)。
(1)欲配制14.6%的稀盐酸

(2)取20.
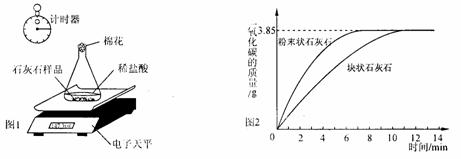
①图1所示实验中数据记录纸上应该连续记录的实验数据是 和 。
②由图2中曲线可以看出,固体物质与液体物质反应,当其他条件相同时,接触面积越 ,其反应速率越 。
③试求样品中碳酸钙的质量分数(假设样品中其他杂质不参加反应,不考虑水、氯化氢逸出)。
五、(本题包括3小题.共20分)
30.金属材料市现代生活和工业生产中应用极为普遍的一类物质。
(l)铁是一种最主要的金属材料,实验室里用一氧化碳还原氧化铁得到铁,实验过程中先通入一氧化碳的目的是 。
炼铁厂常以焦炭、赤铁矿、空气等主要原料炼铁,反应过程如下:
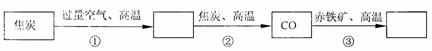
写出②③两步的化学方程式 、 。
(2)在学习了金属资源保护内容以后,兴趣小组同学对金属的锈蚀做了观察,发现残留水的铁锅在与水面接触的部位最易生锈;家用的铜质水龙头也生了一层绿色的铜锈。为了弄清铁锅生锈的原因,兴趣小组同学用相同的铁钉设计了如下安验。经过一周观察:试管A和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀。
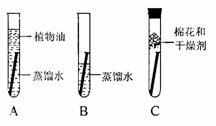
①通过探究发现:铁生锈是铁与 和 共同存在时发生化学反应的过程。
②A中加入的蒸馏水要事先煮沸,其目的是 。
③铜生锈的原因是什么?查阅有关资料:铜锈的主要成份是Cu2(OH)2CO3。他们除依照铁钉锈蚀条件的探究方法进行实验外,还补充做了铜锈蚀与 有关系的实验。请写出一种防止铁或铜等金属制品生锈的具体方法 。
31.某研究性学习小组没汁的实验装置(如图),既可用于制取气体,又可用于验证物质性质。
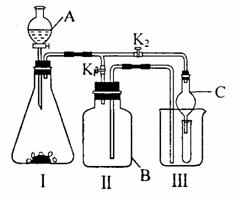
(1)写出仪器A和B的名称:
A: ;B: 。
(2)当打开K1、关闭K2时,利用I、II装置可直接进行的实验是 (填序号)。
①大理石与稀盐酸反应制取二氧化碳②锌与稀硫酸反应制取氢气
小颖认为在不改变I、II装置的仪器及位置的前提下,该装置可用于双氧水制取氧气,她的做法是 ;实验室还可以用高锰酸钾制取氧气,化学方程式为 。
(3)当打开K2、关闭K1时,利用I、III装置可验证二氧化碳与水反应,生成了碳酸,此时试管中盛放的物质是 ,可以观察到的现象是 (C为干燥管,用于防止液体倒吸);若试管中盛放的物质是澄清石灰水,发生化学反应的方程式为 。
32.甲、乙、丙三位同学在一起探究蜡烛燃烧,他们将短玻璃导管插入焰心,发现另一端也可以点燃。
(1)[提出问题] 导管里一定有可燃性气体,气体成分可能会是什么呢?
(2)[作出猜想] 甲同学认为:可能是蜡烛不完全燃烧时产生的CO;
乙同学认为:可能是蜡烛受热后产生的蒸气 ;
丙同学认为:可能上述两种情况都有。
(3)[设计实验]换一根长的导气管,并用湿毛巾包住导管,然后再在导管的另一端做点火试验。
(4)[现象与结论] 如果甲的猜想正确,现象应是:
如果乙的猜想正确,现象应是:
如果丙的猜想正确,现象应是:
(5)如果用CnH2n+2表示蜡烛的主要成分,则其燃烧的化学方程式为: