网址:http://m.1010jiajiao.com/timu_id_896500[举报]

(1)小明同学选用如图1所示的装置制取氧气.制取过程中所发生反应的化学反应方程式为:
| ||
| ||
(2)小雨阅读课外资料得知:双氧水分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是他对氧化铜产生了探究兴趣.
【提出问题】
氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】
小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略).
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | l | |
| ② | 1.2g | CuO 0.5g | |
| ③ | 1.2g | MnO2 0.5g |
②若实验②比实验①的“待测数据”更
③将实验②反应后的固体经提纯分离仍得到0.5克黑色粉末,再将黑色粉末放入试管中,
【评价设计】你认为小雨设计实验③和实验②对比的目的是
(3)小林同学对“过氧化氢溶液的浓度对反应速度有何影响”展开如下探究:取不同浓度的过氧化氢溶液,在其他条件相同的情况下进行实验,记录数据如下:
| 实验 | 1 | 2 | 3 | 4 | 5 |
| 过氧化氢溶液的浓度 | 1% | 3% | 5% | 10% | 15% |
| MnO2粉末用量/g | 0.5 | 0.5 | 0.5 | 0.5 | 0.5 |
| 收集到500mL气体时所用时间/秒 | 560 | 186 | 103 | 35 | 12 |
②小芳同学验证实验后二氧化锰的质量是否仍为0.5g,她取反应后的溶液进行如下操作:
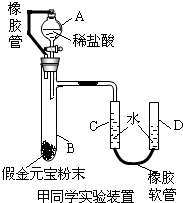 (2011?大庆)社会上曾经出现过有些不法分子用假金元宝骗取路人财物的案件.假设假金元宝为Cu和Zn的合金.甲、乙、丙三位同学为了测定假金元宝中锌的质量分数设计了如下实验步骤:
(2011?大庆)社会上曾经出现过有些不法分子用假金元宝骗取路人财物的案件.假设假金元宝为Cu和Zn的合金.甲、乙、丙三位同学为了测定假金元宝中锌的质量分数设计了如下实验步骤:①连接装置并检查装置的气密性;
②向试管B中加入假金元宝样品粉末;
③准确操作,记录C中液面刻度(C为带有刻度的量气管,D为可上下移动的水准管);
④由A向B中滴加稀盐酸至过量;
⑤B中不在有气体产生并恢复至室温后,准确操作,记录C中液面刻度,计算得到气体的体积为VmL(经查,该气体密度为ρ?g/L).
(1)B中发生的化学反应的化学方程式
(2)如何向试管B中加粉末状药品
(3)连接A、B的橡胶管的作用①
(4)甲同学在不改变实验装置的情况下,如何在加入试剂前检查装置的气密性
(5)甲同学发现试验中缺少某一步骤,导致缺少某一数据而无法计算,该步骤是:
| 13ρV |
| 4a |
| 13ρV |
| 4a |
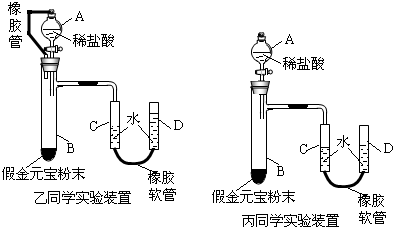
(6)以上是乙、丙两位同学做上述实验的装置,且在步骤⑤读数时装置所处的稳定状态图,则将会对实验结果产生的影响是(假设其余步骤完善且操作准确无误):乙
某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%。为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0 g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0 g,再把100 g稀盐酸平均分成四份依次加入样品中,每次均充分反应。实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是__________ g。
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(3)根据实验数据,在图所示的坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线。(不要求写出计算过程,只画出曲线即可)
某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%。为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0 g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0 g,再把100 g稀盐酸平均分成四份依次加入样品中,每次均充分反应。实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是__________ g。
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(3)根据实验数据,在图所示的坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线。(不要求写出计算过程,只画出曲线即可)

某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%。为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0 g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0 g,再把100 g稀盐酸平均分成四份依次加入样品中,每次均充分反应。实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是__________ g。
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(3)根据实验数据,在图所示的坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线。(不要求写出计算过程,只画出曲线即可)