2007-2008学年度潍坊市昌邑第一学期期末考试
九年级化学试题
(时间90分钟,满分100分)
相对原子质量;H―
一、选择题(本题包括20小题,每小题2分,共40分。每小题只有一个答案正确,多选、错选均不得分)
1.下列物质在寒冷的冬天最容易结冰的是( )
A.食醋 B.蒸馏水 C.酱油 D.自来水
2.下列说法中正确的是( )
A.把5mL98%的硫酸倒入20mL的水中就得到稀硫酸25mL.
B.24%的NaOH溶液取出一半,其溶质质量分数为12%
C.
D.饱和溶液升高温度一定变成不饱和溶液
3.下列对20%的氯化钠溶液的理解正确的是( )
A.该溶液中溶质与溶剂质量比为1:5 B.
C.该溶液中
4.炎热的夏天,当你打开冰箱,从
A.
B.室温下,b溶液一定是饱和溶液
C.蔗糖晶体的溶解度随温度的升高而降低
D.a溶液的溶质质量分数大于b溶液的溶质质量分数
5.氢氧化钾是我国古代纺织业常用的洗涤剂,古人将贝壳(主要成分是碳酸钙)灼烧后的固体,与草木灰在水中相互作用,生成氢氧化钾。在上述反应过程中没有涉及的化学反应基本类型是( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
6.将
A.溶液的质量 B.硝酸钾的溶解度 C.溶质的质量 D.硝酸钾的质量分数
7.1838年3月,纽卡斯尔的一些园艺家访问大物理学家法拉第,并向他请教一个奇特而有趣的问题:为什么别处生长的紫罗兰花都是紫色的,而生长在该市的紫罗兰花却是白色的?法拉第经过一番研究得出结论,该结论后来被化学家证实并在工业上广泛应用。请问法拉第的结论是( )
A.遗传变异 B.施化肥不当
C.纽卡斯尔市空气中SO2含量较高 D.纽卡斯尔市市民用自来水浇花
8.对下列物质用途的叙述不符合实际的是( )
A.熟石灰用于改良酸性土壤 B.硝酸用于制磷肥
C.胆矾可用于配波尔多液 D.食盐可用于制氢氧化钠
9.有X、Y、Z、W四种金属,已知用X制的容器不宜盛放Z的盐溶液。X跟Y的盐溶液不反应,只有W在自然界中能以单质形式存在,则这四种金属的活动性顺序是( )
A.Z>Y>X>W B.X>Z>Y>W C.Y>X>Z>W D.Y>Z>X>W
10.胃溃疡严重的病人的胃酸过多,可内服含有能跟胃酸起反应的物质成分的胃药,以减少胃酸的含量而又不造成胃穿孔。下列物质中,最适合作胃药成分的是( )
A.CaCO3 B.NaHCO
11.为了鉴别Na2CO3、Na2SO4、NaOH和H2SO4四种物质的水溶液,还需从下列试剂中另选一种物质才能达到鉴别的目的,不符合此条件的试剂是( )
A.紫色石蕊试液 B.氯化钠 C.酚酞试液 D.氯化钡溶液
12.配制10%的硝酸钾溶液时,不会引起溶液中硝酸钾的溶质质量分数偏小的是( )
A.用量筒量取水时仰视读数 B.配制溶液的烧杯用少量蒸馏水润洗
C.硝酸钾晶体不纯 D.转移已配好的溶液时,有少量溶液溅出
13.
A.大力推广使用一次性餐具 B.积极开发可再生能源
C.严格控制企业排污 D.尽量杜绝自来水的跑、冒、滴、漏现象
14.2008年北京奥运会主会场――国家体育场“鸟巢”的主体为钢结构,钢属于( )
A.复合材料 B.无机非金属材料 C.合成材料 D.金属材料
15.长期受电磁辐射可引起人头昏、头痛、失眠等症,科学家发现富含维生素的食物具有较好的防辐射损伤功能。下列食物中富含维生素C的是( )
A.油菜 B.牛奶 C.豆腐 D.米饭
16.食物在人体内的化学变化为生命活动提供物质和能量,下列做法你认为正确的是( )
A.蛋白质受热会失去原有的生理活性,因此变质肉类用高温处理后可以食用
B.为了节约粮食,将霉变的小麦通过
C.蔬菜和水果都含有不能被人体吸收的食物纤维,所以要少量食用
D.保健品能适当补充一些体内缺乏的元素,可以适当食用
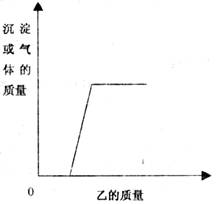
17.向下表的甲物质中逐渐加入相应的乙溶液至过量,反应过程中生成的气体或沉淀的质量与加入乙的质量关系,能用下图所示曲线表示的是( )
序号
甲
乙
A
铜锌的混合物
稀盐酸
B
硫酸和硫酸铜的混合溶液
氢氧化钠溶液
C
盐酸和稀硫酸的混合溶液
氯化钡溶液
D
铁钉
稀盐酸
18.汇源“真橙汁饮料”的配料如下:纯净水、蔗糖、橙浓缩汁、柠檬酸、维生素C。此饮料不含的营养素是( )
A.水 B.维生素 C.油脂 D.糖类
19.加酶洗衣粉易除去衣物上的汗渍、血迹及油渍。现有下列衣料①羊毛织品 ②棉花织物③化纤布料 ④蚕丝织品。其中不宜用加酶洗衣粉洗涤的是( )
A.①④ B.③④ C.①② D.②③
20.现有H2SO4、NaOH、CuO、Na2CO3四种物质,分别与其他物质反应,都有同一物质X生成,则X的化学式可能是下列物质中的( )
A.H2O B.CO
二、填空与简答题(共30分)
21.浓硫酸长期敞口存放会自动溢出,这是因为它具有_____________。氢氧化钠固体放置在敞口容器里,总质量会_____________,原因:①___________________________________;②_____________________________,其反应的化学方程式为__________________________。放置一段时间后,发现容器里有少量溶液,将此溶液与稀硫酸混合,有无色气体生成,这是因为(用化学方程式表示) _______________________________________。
22.现有三只试管,分别加入不同温度和体积的水,试管编号及相关数据如下表:
试管编号
A
B
C
水的体积/mL
5
10
10
水的温度/℃
20
20
50
(1)向三只试管中各加入
(2)再向B、C两只试管中分别加硫酸铜粉末至饱和,则B中溶液的颜色较C中的_________;
(3)由此实验可得出:①溶质的质量分数越大,有色溶液的颜色越______________________;
②_______________________________________。
23.如下图所示,A、B分别是两种固体物质的溶解度曲线。
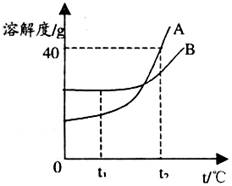
(1)A、B两种物质的溶解度受温度影响变化较大的是___________(填“A”或“B”)。
(2)在t
(3)在t
24.目前,上海已有不少住宅小区实行了生活垃圾分类收集箱。请将下列垃圾的编号填入相应的垃圾箱内。①家禽、鱼类内脏 ②果皮、菜皮 ③碎玻璃 ④废电池 ⑤废荧光灯管 ⑥废金属制品
有机垃圾箱______________;无机垃圾箱______________;有害物质垃圾箱______________。
25.下表为某品牌燕麦片标签中的一部分;
营养成分(每
蛋白质
糖类
油脂
钙
铁
钠
锌
维生素
206mg
19.2mg
37.8mg
10.1mg
18mg
(1)燕麦片中能为人体提供能量的营养素有__________________________________;
(2)燕麦片中含有的_________________元素可预防人体贫血;
(3)人体健康离不开钙元素。下列有关钙元素的叙述中,不正确的是(填序号) _____________;
①人体中钙元素大部分存在于骨骼和牙齿中 ②幼儿及青少年缺钙会得佝偻病和发育不良
③老年人缺钙会发生骨质疏松,容易骨折 ④成年人比幼儿和青少年需要摄入更多的钙
(4)钙片的有效成分是碳酸钙,虽然碳酸钙难溶于水,但服用后可转化为可溶性钙盐被人体吸收,其原因是_______________________________(用化学方程式表示);为了提高补钙效果,服用钙片时常需配合服用维生素D,据此可推知维生索D的功能是_________________。
(5)现有下列食物:①大米 ②豆油 ③鱼 ④鸡蛋 ⑤青菜 ⑥西瓜。其中能提供丰富蛋白质的有____________________________。
26.人体缺乏维生素C(简写“VC”)就会患坏血病,哥伦布探险时的许多船员就因此而死亡。下图所示为某种“维生索C”说明书的一部分。请你回答:
维生素C(白色)
化学式:C6H8O6
每片100mg,含VC10%
一日**次,每次2片
饭后服用
若发黄请勿食用
(1)“VC”中含有_____________种元素。
(2)若正常成人每天对“VC”的最低需要量为60mg。
①当“VC”完全来自右图的“维生素C”,则每天至少服用_____________次;
②当“VC”完全来自某种新鲜蔬菜(每
(3)取2片“维生素C”溶于水,滴入紫色石蕊试液变红色,说明“VC”的溶液显______性;加热该溶液至沸腾,红色消失,表明“VC”受热时易被破坏,那么在烹调新鲜蔬菜时要减少“VC”的损失,应采取的措施之一是_______________________________________。
三、实验探究题(共22分)
27.小明同学想弄清家里化肥的成分,他看到袋中化肥是原白色晶体,用少量肥料跟熟石灰一起研磨,有浓烈的刺激性气味,初步判定是一种氮肥。
为进一步证实肥料的成分,小明将少量肥料样品带到学校进行探究。
探究内容
现象
结论
实验1:取一定量的肥料放入水中,震荡
样品完全溶解
__________________________
实验2:取实验1中的部分溶液,滴加石蕊试剂
溶液呈红色
__________________________
实验3:另取实验1中的部分溶液,滴加氯化钡试剂和稀盐酸
有白色沉淀生成
该化肥为_______________
(1)小明家的化肥是一种铵盐,有同学认为盐的水溶液都呈中性,你同意他的观点吗?
请举例说明____________________________________________________。
(2)结合探究过程回答,施用该化肥时应注意_______________________________________。
28.有一包粉末,可能由KCl、K2SO4、K2CO3、CuCl2、MgCl2中的一种或几种物质组成。现做如下实验:
实验①:取少量粉末,加水溶解后得到无色透明溶液。
实验②:取①所得溶液少许,加入氢氧化钠溶液后看不到明显现象。
实验③:取①所得溶液少许,加入适量硝酸钡溶液后出现白色沉淀。过滤后,在沉淀中加入适量稀硝酸,沉淀全部溶解。
根据以上实验,请回答:
(1)原粉末中一定没有__________________________,一定有__________________________。
(2)原粉末中可能有_______________________________,为了验证可能含有的成分是否存在,请你设计实验证明:
操作
现象
结论
四、计算题(共8分)
29.某品牌香醋,其主要成分是醋酸,化学式为CH3COOH。测定该香醋中醋酸含量的原理是:CH3COOH+NaOH=CH3COONa+H2O。化学课外活动小组中和
(1)
(2)该香醋中醋酸的质量分数。