2006-2007学年度东营区中等学校招生第二次模拟考试
化学试卷
本试题分第I卷和第Ⅱ卷两部分。第I卷2页为选择题,18分;第Ⅱ卷4页为非选择题。32分。共50分。考试时间为60分钟。
可能用到的相对原子质量:
H=
第I卷(选择题共18分)
一、选择题(本题包括9小题,每题2分,共18分;下列每题中只有一个选项符合题意。)
1.
A.蒸馏 B.吸附沉淀 C.过滤 D.静置沉淀
2.去年5月31日是世界卫生组织发起的第18个“世界无烟日”。据报道,目前全球有13亿吸烟者,中国就有3.5亿人吸烟,每年有120万人因吸烟而死亡,占全球与吸烟有关疾病死亡人数的1/4。为了你和他人的健康,要远离烟草,养成良好的健康生活习惯。下列有关说法正确的是
A.香烟烟气中只有尼古丁有毒
B.市售香烟通常装有过滤嘴,所以吸烟对人体无害
C.吸烟只影响自己的健康,不影响他人的健康
D.香烟烟气中的一氧化碳比氧气更容易与血红蛋白结合
3.下列对塑料的认识正确的是
A.塑料属于天然有机高分子材料
B.废弃塑料是造成“白色污染”的主要物质
C.所有塑料都容易燃烧并产生有毒气体
D.塑料给人类带来了污染,因此要禁止生产和使用
4.目前我国生产的合成洗衣粉中的主要成份是下列几种物质,其中对环境有较严重影响的是
A.十二烷基苯磺酸钠(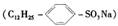 )
)
B.三聚磷酸钠(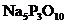 )
)
C.蛋白酶
D.硅酸钠(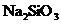 )
)
5.下图形象地表示了氯化钠的形成过程。下列相关叙述中不正确的是

A.钠原子易失去一个电子,氯原子易得到一个电子
B.钠跟氯气反应生成氯化钠
C.氯化钠是离子化合物
D.钠离子与钠原子有相似的化学性质
6.下图是气体分子的示意图,图中“●”和“○”分别表示质子数不同的原子,其中能表示化合物的是
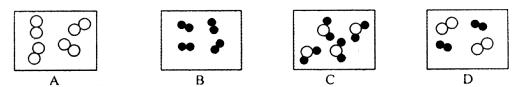
7.三氧化二碳(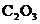 )是金星大气层的成分之一,化学性质与一氧化碳相似。下列有关三氧化二碳的说法不正确的是
)是金星大气层的成分之一,化学性质与一氧化碳相似。下列有关三氧化二碳的说法不正确的是
A.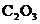 具有还原性 B.
具有还原性 B.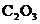 充分燃烧的产物是
充分燃烧的产物是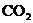
C.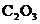 属于碱性氧化物 D.
属于碱性氧化物 D.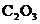 中碳元素的质量分数约为33.3%
中碳元素的质量分数约为33.3%
8.某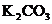 ,样品中含有
,样品中含有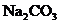 、
、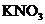 和
和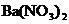 三种杂质中的一种或两种。现将
三种杂质中的一种或两种。现将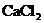 溶液,得到
溶液,得到
A.肯定有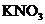 ,可能有
,可能有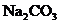
B.肯定有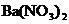 ,可能还含有
,可能还含有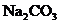
C.肯定没有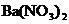 ,肯定有
,肯定有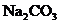
D.肯定没有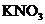 和
和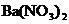
9.密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
物质
A
B
C
D
反应前质量/g
19.7
8.7
31.6
0.4
反应后质量/g
待测
17.4
0
3.6
下列说法正确的是
A.物质C一定是化合物,物质D可能是单质
B.反应后密闭容器中A的质量为
C.反应过程中,物质B与物质D变化的质量比为87∶36
D.若物质A与物质C的相对分子质量之比为197∶158,则反应中A与c的化学计量数之比为l∶3
第Ⅱ卷(非选择题共32分)
注意事项:
1.第Ⅱ卷共4页,用钢笔或圆珠笔直接答在试卷上。
2.答卷前将密封线内的项目填写清楚。
可能用到的相对原子质量:
H:
二、填空题(本题包括5小题,共19分)
10.(3分)当前发展较快,高效低毒的灭火剂叫“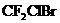 ,命名方法是按碳、氟、氯、溴的顺序分别以阿拉伯数字表示相应的原子数(末尾的“
,命名方法是按碳、氟、氯、溴的顺序分别以阿拉伯数字表示相应的原子数(末尾的“
2402 。
11.(3分)现有三种铁矿石:①含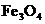 80%的磁铁矿石;②含
80%的磁铁矿石;②含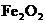 80%的赤铁矿石;③含
80%的赤铁矿石;③含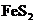 85%的黄铁矿石。若仅从铁的含量考虑,冶炼生铁的矿石应选用 (填序号)。在实际生产中,选用铁矿石还应综合考虑多种因素,如
等(至少答两种)。
85%的黄铁矿石。若仅从铁的含量考虑,冶炼生铁的矿石应选用 (填序号)。在实际生产中,选用铁矿石还应综合考虑多种因素,如
等(至少答两种)。
12.(3分)我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出的贡献。他以食盐、水、氨气、二氧化碳为原料,先制得碳酸氢钠和氯化铵,进而生产出纯碱。下表是几种物质在不同温度时的溶解度:
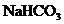
6.9
9.6
2.7
6.4
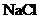
35.7
35.8
36.6
37.3
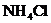
29.4
37.2
45.8
55.2
(1)从表中数据可以看出,温度对 的溶解度影响不大。
(2)要使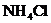 饱和溶液中的
饱和溶液中的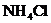 结晶析出,在
(填“较高”或“较低”)温度下进行比较合适。
结晶析出,在
(填“较高”或“较低”)温度下进行比较合适。
(3)“侯氏制碱法”制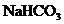 的方程式是
的方程式是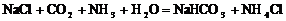 ,该反应能进行的原因是
。
,该反应能进行的原因是
。
13.(8分)水是宝贵的自然资源,在工农业生产和日常生活中有着极其广泛的应用。
(1)自来水的生产过程大体如下图:
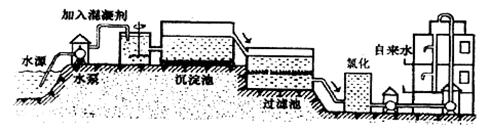
上图过滤池中有活性炭层,该过程中发生
变化。氯化时,通常通入一定量氯气,它与水反应生成盐酸和次氯酸。实验室配制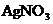 溶液时不宜使用自来水,其原因是(用化学方程式表示)
。高锰酸钾(
溶液时不宜使用自来水,其原因是(用化学方程式表示)
。高锰酸钾(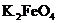 )是一种理想的水处理剂,高铁酸钾中铁元素的化合价是
。
)是一种理想的水处理剂,高铁酸钾中铁元素的化合价是
。
(2)电解水时,加入少量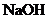 可以增强水的导电性。现将
可以增强水的导电性。现将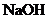 溶解在
溶解在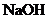 的质量分数变为0.2%时,有
水被分解。
的质量分数变为0.2%时,有
水被分解。
(3)在河旁有甲、乙、丙、丁四座工厂(位置如右图所示),每个工厂排出的废液只含有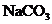 、
、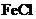 、
、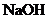 、
、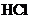 中的一种。某环保小组对河水监测时发现:甲处河水呈无色;乙处河水呈红褐色;丙处河水由浑变清;丁处产生气泡,河水澄清。请回答:
中的一种。某环保小组对河水监测时发现:甲处河水呈无色;乙处河水呈红褐色;丙处河水由浑变清;丁处产生气泡,河水澄清。请回答:
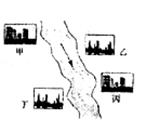
①甲工厂排出的废液是一种碱性物质,检验该物质呈碱性可选用的试剂是 。
②乙处河水呈红褐色的化学方程式是 。
③丁处产生气泡的化学方程式是 。
14.(2分)某学生为证明浓盐酸具有挥发性和碳酸具有不稳定性,设计了如下实验:
(1)将石灰石和浓盐酸反应产生的气体通入紫色石蕊试液,来证明浓盐酸的挥发性。
(2)将上述已变红的石蕊试液加热煮沸,就可证明碳酸已分解。
试分析实验设计的是否合理。并说明理由:
实验(1) 。
实验(2) 。
三、实验与探究题(本题包括2小题,共7分)
15.(3分)研究课上,小明同学为了探究氨气(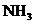 )的某些性质,做了以下实验:
)的某些性质,做了以下实验:
下图中从左向右依次是他做的实验及相应现象。

通过实验,小明同学可得出氨气的三点性质,分别是:① ;
② ;③ 。
16.(4分)取一片洗净晾干的鸡蛋壳(主要成分为碳酸钙。不考虑其他杂质)放在酒精灯火焰上灼烧一段时间后,放置冷却。某同学研究其在灼烧后残留固体的组成,请你参与此研究。
(1)根据你的知识和经验提出假设:残留固体可能组成为 ;
(2)请你设计实验验证假设:
步骤和方法
现象
结论
四、计算题(本题包括2小题,共6分)
17.(3分)小华同学为研究胆矾晶体加热后所得物质的组成,做了以下实验:取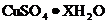 )加热使其分解,绘制出固体的质量随温度的变化关系图。如图到tl℃时该固体完全失去结晶水,化学方程式为:
)加热使其分解,绘制出固体的质量随温度的变化关系图。如图到tl℃时该固体完全失去结晶水,化学方程式为: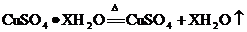 。
。
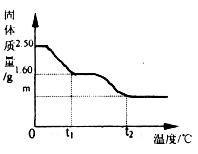
(1)胆矾晶体中X的值是 。
(2)升温到t
18.(3分)为测定标示质量分数为32%的盐酸(下图1)的实际质量分数,小明用pH测定仪组成实验装置(图2)。实验时先在烧杯中加入

(1)请以此次测定的结果,列式计算该盐酸的实际质量分数;
(2)请分析你的计算结果与标签标示的质量分数不一致的可能原因。