题目内容
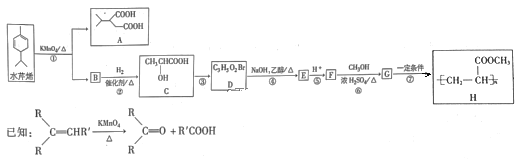
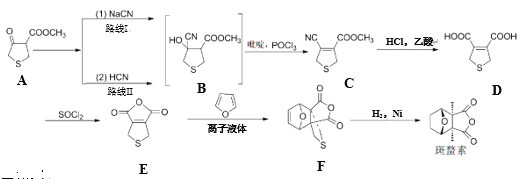
【题目】斑蝥素具有良好的抗肿瘤活性。下列是斑蝥素的一种合成路线:
已知:ⅰ.其它条件不变,通常反应物浓度越大速率越快,多步反应时速率由最慢反应决定;
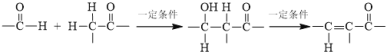
ⅱ.当用A1=B1和A2—B2分别表示分子中含有双键的有机化合物和试剂时,可用下面的式子来表示加成反应的一般结果:
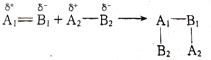
酮与HCN或NaCN加成历程表述如下:
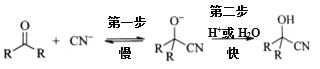
ⅲ.HCN为弱酸
(1)有机化合物A的分子式为______。
(2)A转化为B时,路线Ⅰ和路线Ⅱ均在水溶液中进行。实验发现:路线Ⅰ比路线Ⅱ所需时间短,试解释原因______。
(3)写出B→C的化学方程式______。
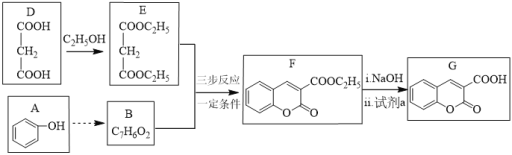
(4)D与乙二醇(HOCH2CH2OH)发生缩聚反应的化学方程式为______。
(5)①F的分子式为:C10H8O4S,则E→F的反应类型为______。
②下表研究了______对合成F的影响,合成F的较优条件为______(填编号)。
编号 | 离子液体 | 反应温度/℃ | 反应时间/h | E含量/% | F含量/% |
1 | [BPy] BF4 | 45 | 20 | 90 | 9 |
2 | [HMIM]PF6 | 35 | 20 | 5 | 93 |
3 | [BMIM]BF4 | 25 | 30 | 0 | 90 |
4 | [HMIM]BF4 | 35 | 20 | 38 | 57 |
5 | [BMIM]BF4 | 35 | 20 | 0 | 86 |
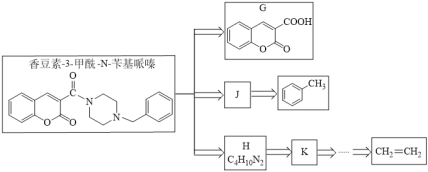
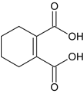
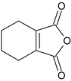
(6)请写出以![]() 为原料制备
为原料制备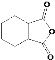 的合成路线流程图______(无机试剂任选,合成路线流程图示见本题题干)。
的合成路线流程图______(无机试剂任选,合成路线流程图示见本题题干)。
【答案】C6H8O3S HCN是弱酸水溶液中CN-的浓度远小于NaCN,路线Ⅰ的反应速度快,所需时间短 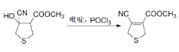 +H2O n
+H2O n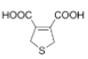 +nHOCH2CH2OH
+nHOCH2CH2OH![]()
![]() +(2n-1)H2O 加成反应 离子液体、反应温度 3
+(2n-1)H2O 加成反应 离子液体、反应温度 3 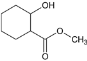
![]()

![]()
![]()
![]()
![]()
 。
。
【解析】
(1)根据有机化合物A的结构简式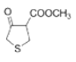 写出分子式;
写出分子式;
(2)HCN是弱酸水溶液中CN-的浓度远小于NaCN,速率慢;
(3)B→C相当于醇发生消去反应;
(4)二元酸和二元醇发生缩聚反应;
(5)从生产条件和产品纯度考虑;
(6)模仿题干A到E的合成过程设计。
(1)有机化合物A 的分子式为C6H8O3S。
的分子式为C6H8O3S。
(2)酮与HCN或NaCN加成历程中第一步是慢反应,决定反应速率,HCN是弱酸水溶液中CN-的浓度远小于NaCN,路线Ⅰ的反应速度快,所需时间短。
(3)B→C发生消去反应,化学方程式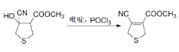 +H2O 。
+H2O 。
(4)D 与乙二醇(HOCH2CH2OH)发生缩聚反应的化学方程式为
与乙二醇(HOCH2CH2OH)发生缩聚反应的化学方程式为
n +nHOCH2CH2OH
+nHOCH2CH2OH![]()
![]() +(2n-1)H2O 。
+(2n-1)H2O 。
(5)①F的分子式为:C10H8O4S, +
+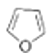 →
→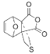 ,则E→F的反应类型为加成反应。
,则E→F的反应类型为加成反应。
②分析表中数据,研究了离子液体、反应温度对合成F的影响,合成F的较优条件为3,因3在[BMIM]BF4离子液体中,反应在常温下进行,得到F的含量高。
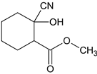
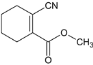
(6)模仿题干A到E的合成过程设计,先将 中醇羟基氧化,再利用NaCN加成,后消去得
中醇羟基氧化,再利用NaCN加成,后消去得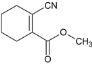 ,在酸性条件下水解生成二元酸,脱水即得产品,参考流程如下:
,在酸性条件下水解生成二元酸,脱水即得产品,参考流程如下:

![]()

![]()

![]()

![]()

![]()
 。
。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案