题目内容
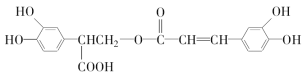
【题目】沐舒坦(结构简式为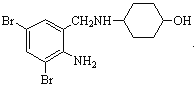 ,不考虑立体异构)是临床上使用广泛的。下图所示的其多条合成路线中的一条(反应试剂和反应条件均未标出)
,不考虑立体异构)是临床上使用广泛的。下图所示的其多条合成路线中的一条(反应试剂和反应条件均未标出)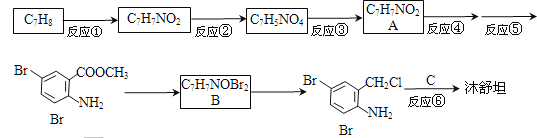
已知:![]()
完成下列填空:
(1)写出反应①所用试剂和反应条件 ,反应⑥的化学反应方程式 。
(2)写出反应类型
反应③ 反应⑤
(3)写出结构简式
A B
(4)反应⑥中除加入反应试剂C外,还需要加入K2CO3,其目的是为了 ;
(5)写出两种C的能发生水解反应,且只含3种不同化学环境氢原子的同分异构体的结构简式 、
(6)反应②,反应③的顺序不能颠倒,其原因是 。
【答案】(1)浓硝酸,浓硫酸,水浴加热;
2![]() +2
+2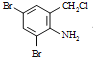 +K2CO3→2
+K2CO3→2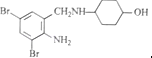 +2KCl+CO2↑+H2O
+2KCl+CO2↑+H2O
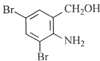
(2)还原反应,取代反应(各1分)(3)![]() 、
、
(4)生成的HCl,使平衡正向移动,防止产品不纯(1分)
(5)(CH3)3CCONHCH3、CH3CONHC(CH3)3(各1分)
(6)高锰酸钾氧化甲基的同时,也将氨基氧化、最终得不到A
【解析】
试题分析:结合产物的结构简式,利用流程图和起始原料的分子式知,起始原料为甲苯,所以反应①是甲苯和硝酸在浓硫酸作催化剂、加热条件下发生取代反应生成邻硝基甲苯,根据题意知,反应②是邻硝基甲苯和高锰酸钾在加热条件下发生氧化反应生成邻硝基苯甲酸,反应③为邻硝基苯甲酸经还原反应使硝基转化为氨基,所以A的结构简式为:![]() ,反应④是A和甲醇发生酯化反应生成
,反应④是A和甲醇发生酯化反应生成![]() ,然后
,然后![]() 在溴化铁作催化剂作用下,与溴发生取代反应(反应⑤),利用取代基的④定位效应知,溴原子取代氨基的邻、对位上氢原子,因此反应⑤生成物的结构简式为:
在溴化铁作催化剂作用下,与溴发生取代反应(反应⑤),利用取代基的④定位效应知,溴原子取代氨基的邻、对位上氢原子,因此反应⑤生成物的结构简式为: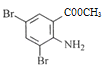 ,结合流程图中B物质反应前后物质的结构简式,利用B的分子式可推知B的结构简式为:
,结合流程图中B物质反应前后物质的结构简式,利用B的分子式可推知B的结构简式为: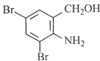 ,反应⑥中有HCl生成,而氯化氢与氨基可发生反应,可知反应⑥中加入碳酸钾的作用是中和反应生成的盐酸,同时防止盐酸和氨基发生反应,C物质的结构简式为:
,反应⑥中有HCl生成,而氯化氢与氨基可发生反应,可知反应⑥中加入碳酸钾的作用是中和反应生成的盐酸,同时防止盐酸和氨基发生反应,C物质的结构简式为:![]() ;
;
(1)反应①为在浓硫酸作催化剂、加热条件下,浓硝酸和甲苯发生取代反应生成邻硝基甲苯,所用试剂和反应条件是HNO3,浓硫酸、加热;根据上面的分析可知,反应⑥的化学反应方程式为
2![]() +2
+2 +K2CO3→2
+K2CO3→2 +2KCl+CO2↑+H2O;
+2KCl+CO2↑+H2O;
(2)根据上面的分析可知,反应③为还原反应,反应⑤为取代反应;
(3)通过以上知,A和B的结构简式分别是![]() 、
、 ;
;
(4)反应⑥中有HCl生成,而氯化氢与氨基可发生反应,可知反应⑥中加入碳酸钾的作用是中和反应生成的盐酸,同时防止盐酸和氨基发生反应;
(5)C物质的结构简式为:![]() ,分子式为C6H13NO,该物质可水解的同分异构体只能含有肽键,结合只含3种化学环境下不同的氢原子,可知肽键两端连接的烷基中都只含一种氢原子,因此两个烷基只能是甲基和﹣C(CH3)3,所以其同分异构体为:
,分子式为C6H13NO,该物质可水解的同分异构体只能含有肽键,结合只含3种化学环境下不同的氢原子,可知肽键两端连接的烷基中都只含一种氢原子,因此两个烷基只能是甲基和﹣C(CH3)3,所以其同分异构体为:
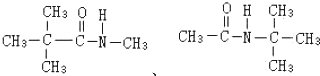 ;
;
(6)因氨基易被氧化,如果反应②③颠倒,再利用高锰酸钾、加热的条件下氧化甲基转化为羧基的同时也会将氨基氧化。

【题目】经测定乙醇的化学式是C2H6O,由于有机物普遍存在的同分异构现象,推测乙醇的结构可能是下列两种之一。
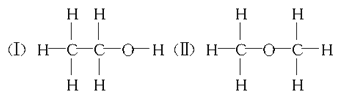
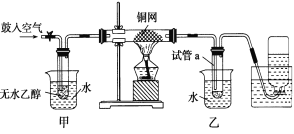
为测定其结构,应利用物质的特殊性进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,请甲、乙、丙、丁四名同学直接利用如图给定装置进行实验确定乙醇的结构。
(1)学生甲得到一组实验数据:
乙醇的物质的量(mol) | 氢气的体积(L) |
0.10 | 1.12(标准状况) |
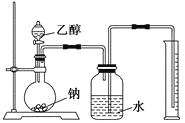
根据以上数据推断乙醇的结构应为________(用Ⅰ、Ⅱ表示),理由为_______________。
(2)同学乙分别准确称量4.60 g乙醇进行多次实验,结果发现以排到量筒内的水的体积作为生成的H2体积换算成标准状况后都小于1.12 L,如果忽略量筒本身及乙读数造成的误差,那么乙认为可能是由于样品中含有少量水造成的,你认为正确吗?________(填“正确”或“不正确”)如果你认为正确,请说明理由,如果你认为不正确,那产生这种情况的原因应该是什么?________________。
(3)同学丙认为实验成功的关键有:①装置气密性要良好
②实验开始前准确确定乙醇的量 ③钠足量 ④广口瓶内水必须充满 ⑤氢气体积的测算方法正确、数据准确。其中正确的有________。(填序号)
(4)同学丁不想通过称量乙醇的质量来确定乙醇的量,那么他还需知道的数据是_____________。
(5)实验后,四名同学从乙醇的可能结构分析入手对乙醇和钠的量的关系进行了讨论,如果乙醇的物质的量为n mol,那么对钠的物质的量的取值要求必须是_________________。
【题目】乙酸丁酯是重要的化工原料,具有水果香味。实验室制备乙酸丁酯的反应、装置示意图和有关信息如下:
CH3COOH+CH3CH2CH2CH2OH![]() CH3COOCH2CH2CH2CH3+H2O
CH3COOCH2CH2CH2CH3+H2O
乙酸 | 正丁醇 | 乙酸丁酯 | |
熔点/℃ | 16.6 | -89.5 | -73.5 |
沸点/℃ | 117.9 | 117 | 126.0 |
密度/g·cm-3 | 1.1 | 0.80 | 0.88 |
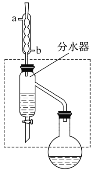
(1)乙酸丁酯粗产品的制备
在干燥的50 mL圆底烧瓶中,装入沸石,加入12.0 mL正丁醇和16.0 mL冰醋酸(过量),再加3~4滴浓硫酸。然后再安装分水器(作用:实验过程中不断分离除去反应生成的水)、冷凝管,然后小火加热。将烧瓶中反应后的混合物冷却与分水器的酯层合并。装置中冷水应从________(填“a”或“b”)口通入;通过分水器不断分离除去反应生成的水的目的是___________________________________________________。
(2)乙酸丁酯的精制
将乙酸丁酯粗产品用如下的操作进行精制:①水洗、②蒸馏、③用无水MgSO4干燥、④用10%碳酸钠洗涤。
①正确的操作步骤是________________(填标号)。
A.①②③④ B.③①④② C.④①③② D.③④①②
②在乙酸丁酯的精制中,用10%碳酸钠洗涤的主要目的是 。
③在洗涤、分液操作中,应充分振荡,然后静置,待分层后________(填标号)。
A.直接将乙酸丁酯从分液漏斗的上口倒出
B.直接将乙酸丁酯从分液漏斗的下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸丁酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸丁酯从上口倒出
(3)计算产率
测量分水器内由乙酸与丁醇反应生成的水体积为1.8 mL,假设在制取乙酸丁酯过程中反应物和生成物没有损失,且忽略副反应,乙酸丁酯的产率为________。