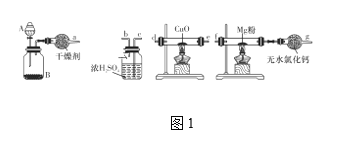
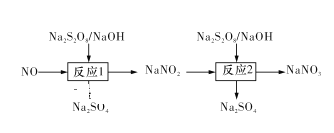
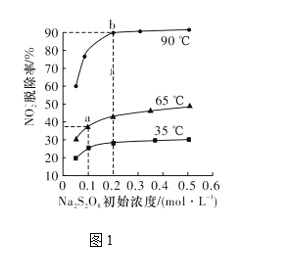
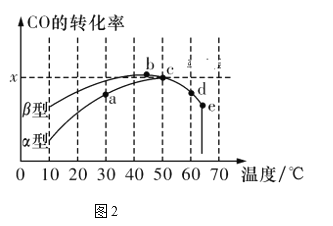
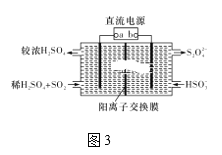
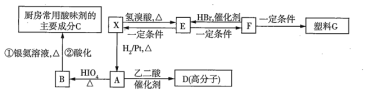
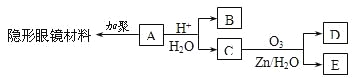
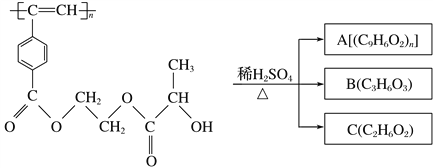
0 203352 203360 203366 203370 203376 203378 203382 203388 203390 203396 203402 203406 203408 203412 203418 203420 203426 203430 203432 203436 203438 203442 203444 203446 203447 203448 203450 203451 203452 203454 203456 203460 203462 203466 203468 203472 203478 203480 203486 203490 203492 203496 203502 203508 203510 203516 203520 203522 203528 203532 203538 203546 203614